1 . 铵明矾晶体的化学式为 ,以铵明矾为原料可实现如图转化。
,以铵明矾为原料可实现如图转化。 与题中阳离子不形成配合物,固体A为纯净物。
与题中阳离子不形成配合物,固体A为纯净物。
(1)铵明矾晶体“隔绝空气加热”分解产物中含硫化合物有___________ 。
(2)步骤III中生成白色沉淀C反应的化学方程式为___________ 。
(3)合成铵明矾过程中常使用过量的硫酸铵,一个作用是抑制硫酸铝水解,另一个重要作用是___________ 。
(4)设计实验验证固体A含有的金属元素:___________ 。
(5)步骤I中,铵明矾晶体在各温度段内受热“失重计算值”如表所示。(失重计算值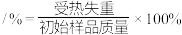 )
)
通过上述数据可判断,在温度区间___________ ℃,铵明矾基本上失去了结晶水。
 ,以铵明矾为原料可实现如图转化。
,以铵明矾为原料可实现如图转化。
 与题中阳离子不形成配合物,固体A为纯净物。
与题中阳离子不形成配合物,固体A为纯净物。(1)铵明矾晶体“隔绝空气加热”分解产物中含硫化合物有
(2)步骤III中生成白色沉淀C反应的化学方程式为
(3)合成铵明矾过程中常使用过量的硫酸铵,一个作用是抑制硫酸铝水解,另一个重要作用是
(4)设计实验验证固体A含有的金属元素:
(5)步骤I中,铵明矾晶体在各温度段内受热“失重计算值”如表所示。(失重计算值
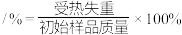 )
)| 温度区间/℃ | 18→190 | 190→430 | 430→505 | 505→900 |
| 失重计算值/% | 39.20 | 7.80 | 13.00 | 26.00 |
您最近一年使用:0次
名校
解题方法
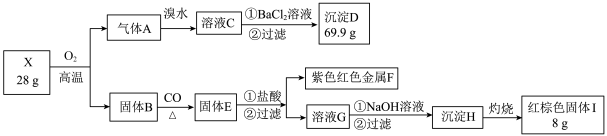
2 . 为探究某矿物X(含三种常见元素)的组成和性质,某兴趣小组设计了如下实验:已知实验中所用试剂均足量,固体B是一种单质和化合物的混合物,请回答如下问题:______ 。
(2)气体A与溴水反应的离子方程式:______ 。
(3)X在高温下与氧气充分反应的化学方程式:______ 。
(4)红棕色固体Ⅰ溶于HI溶液的离子方程式______ 。
(5)检验溶液G中的金属阳离子的实验方案:______ 。
(2)气体A与溴水反应的离子方程式:
(3)X在高温下与氧气充分反应的化学方程式:
(4)红棕色固体Ⅰ溶于HI溶液的离子方程式
(5)检验溶液G中的金属阳离子的实验方案:
您最近一年使用:0次
名校
3 . 三氧化二铬 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化:
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。
(1)写出溶液B中的所有阳离子__________ 。写出步骤Ⅱ中生成气体C的离子方程式__________ 。沉淀E的化学式为__________ 。
(2)下列说法正确的是__________。
(3)在碱性条件下, 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式__________ 。根据该反应原理,设计实验检验上述反应后溶液中生成的阴离子__________ 。
 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化: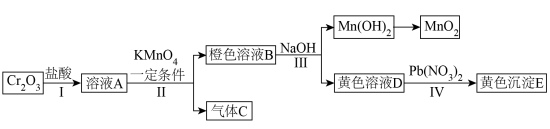
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数
 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。(1)写出溶液B中的所有阳离子
(2)下列说法正确的是__________。
| A.气体C在工业上可通过电解法制备 |
| B.在溶液B中加入乙醇,溶液变为绿色,再变为蓝色 |
| C.将步骤Ⅰ中的盐酸换成硫酸,仅影响步骤Ⅱ的反应 |
| D.在步骤Ⅲ中,溶液B加入纯碱溶液,也能分离出锰元素 |
(3)在碱性条件下,
 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式
您最近一年使用:0次
名校
解题方法
4 . 铬(Cr)广泛应用于冶金、化工、航天等领域。工业上以络铁矿(主要成分为FeCr2O4,含有少量Al2O3)为原料制备金属铬的工艺流程如图所示:
(1)FeCr2O4中Fe为+2价,Cr的化合价为______ ,“焙烧”中FeCr2O4反应的化学方程式为__________ 。
(2)“沉铝”中所得滤渣的成分为________ ,需控制pH=6~10的原因为_______________ 。
(3)“酸化”中反应的离子方程式为____________ ;若该反应的平衡常数K=4×1014,已知:“酸化”后溶液中c( )=1.6×10-3mol/L,则溶液中c(
)=1.6×10-3mol/L,则溶液中c( )=
)=_______ mol/L。
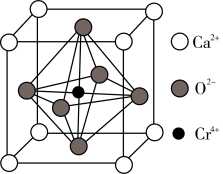
(4)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+、O2-采用面心立方最密堆积方式(处于面对角线上的钙离子与氧离子紧密相邻)。________ pm。

(1)FeCr2O4中Fe为+2价,Cr的化合价为
(2)“沉铝”中所得滤渣的成分为
(3)“酸化”中反应的离子方程式为
 )=1.6×10-3mol/L,则溶液中c(
)=1.6×10-3mol/L,则溶液中c( )=
)=(4)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+、O2-采用面心立方最密堆积方式(处于面对角线上的钙离子与氧离子紧密相邻)。
您最近一年使用:0次
2024-04-11更新
|
148次组卷
|
2卷引用:浙江省舟山中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
5 . 结晶水合物Fe(NO3)3·9H2O主要用作催化剂 某兴趣小组按如下流程进行实验:
某兴趣小组按如下流程进行实验:
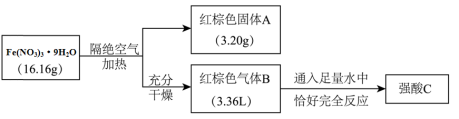
(1)混合气体B的成分为
(2)写出化合物Fe(NO3)3·9H2O隔绝空气加热分解生成A和B的化学反应方程式
(3)固体A溶于氢氰酸(弱酸,分子式为:HCN)溶液生成六配位阴离子,溶液显强酸性。写出该反应的离子方程式
(4)控制温度的条件下,加热FeCl3溶液所得固体成分为:Fe2O3或FeOCl或两者混合物(已知:FeOCl难溶于水,易溶于强酸),设计实验方案检验固体中有FeOCl:
您最近一年使用:0次
解题方法
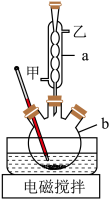
6 . 苯甲酸可用于合成纤维、树脂涂料等,也可作为药物或防腐制,有抑制真菌、细菌生长的作用。实验室利用高锰酸钾溶液氧化甲苯制备苯甲酸,实验装置如图所示:
对反应混合物进行分离提纯的流程如下:

已知:甲苯的沸点是110.6℃,苯的沸点约为80℃;苯甲酸微溶于冷水,易溶于热水。
请回答下列问题:
(1)仪器a的名称为_______ ,冷凝水从_______ 口流出(填“甲”或“乙”)。
(2)在三颈烧瓶中加入一定量的甲苯、水和稍过量高锰酸钾固体,通入冷凝水,维持反应温度90℃,开启电磁搅拌器,加热回流至回流液不再出现油珠。
①“回流液不再出现油珠”说明_______ 。
②已知反应过程中甲苯被氧化为苯甲酸钾,该反应的化学方程式为_______ 。
(3)为测定所得产品的纯度,称取1.220g粗产品,配成100mL溶液,取其中25.00mL溶液用0.080mol·L-1KOH溶液进行滴定。
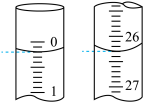
第一次滴定开始和结束时,碱式滴定管中的液面如图所示。重复实验2次,测得所用KOH溶液的体积分别为26.08mL、26.12mL,则该粗产品中苯甲酸的质量分数为_______ %。

对反应混合物进行分离提纯的流程如下:

已知:甲苯的沸点是110.6℃,苯的沸点约为80℃;苯甲酸微溶于冷水,易溶于热水。
请回答下列问题:
(1)仪器a的名称为
(2)在三颈烧瓶中加入一定量的甲苯、水和稍过量高锰酸钾固体,通入冷凝水,维持反应温度90℃,开启电磁搅拌器,加热回流至回流液不再出现油珠。
①“回流液不再出现油珠”说明
②已知反应过程中甲苯被氧化为苯甲酸钾,该反应的化学方程式为
(3)为测定所得产品的纯度,称取1.220g粗产品,配成100mL溶液,取其中25.00mL溶液用0.080mol·L-1KOH溶液进行滴定。
第一次滴定开始和结束时,碱式滴定管中的液面如图所示。重复实验2次,测得所用KOH溶液的体积分别为26.08mL、26.12mL,则该粗产品中苯甲酸的质量分数为

您最近一年使用:0次
解题方法
7 . “声名大振”学习小组围绕新型绿色消毒剂——高铁酸钠( )展开探究。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A为气态非金属单质,B为金属单质,E为生活中常见的调味品,F在标准状况下密度为
)展开探究。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A为气态非金属单质,B为金属单质,E为生活中常见的调味品,F在标准状况下密度为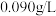 。
。

请回答:
(1)化合物D中的化学键类型是______ 。
(2) 的电子式是
的电子式是______ 。
(3)反应②的离子方程式是______ 。
(4)反应③,F在A中燃烧的反应现象是______ 。
(5)反应⑤的化学方程式是______ 。
(6)请在方框内填入相应物质的化学式,完成反应④的化学方程式,并标明电子转移的方向和数目:______ 。
2 +3
+3 +
+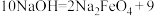
 +5
+5
 )展开探究。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A为气态非金属单质,B为金属单质,E为生活中常见的调味品,F在标准状况下密度为
)展开探究。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A为气态非金属单质,B为金属单质,E为生活中常见的调味品,F在标准状况下密度为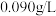 。
。
请回答:
(1)化合物D中的化学键类型是
(2)
 的电子式是
的电子式是(3)反应②的离子方程式是
(4)反应③,F在A中燃烧的反应现象是
(5)反应⑤的化学方程式是
(6)请在方框内填入相应物质的化学式,完成反应④的化学方程式,并标明电子转移的方向和数目:
2
 +3
+3 +
+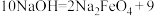
 +5
+5
您最近一年使用:0次
解题方法
8 . 为探究某矿物X(含三种常见元素)的组成和性质,某兴趣小组设计了如下实验:已知实验中所用试剂均足量,固体B是一种单质和化合物的混合物,请回答如下问题:
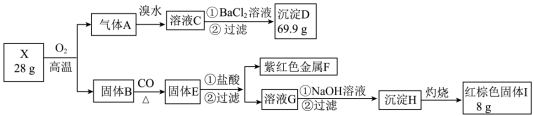
(1)X中所含元素为:___________ 。
(2)溴水是否可以用酸化的双氧水代替,若不可行,请说明理由,若可行,请写出反应的离子方程式:___________ 。
(3)检验溶液G中的金属阳离子的实验方案:___________ 。
(4)溶液G转化为沉淀H的现象___________ 。
(5)X在高温下与氧气充分反应的化学方程式:___________ 。

(1)X中所含元素为:
(2)溴水是否可以用酸化的双氧水代替,若不可行,请说明理由,若可行,请写出反应的离子方程式:
(3)检验溶液G中的金属阳离子的实验方案:
(4)溶液G转化为沉淀H的现象
(5)X在高温下与氧气充分反应的化学方程式:
您最近一年使用:0次
解题方法
9 . 燃煤火电厂产生的尾气(主要成分为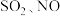 )可以按如下流程脱除或利用已知:混合气体X可直接排入空气。请回答:
)可以按如下流程脱除或利用已知:混合气体X可直接排入空气。请回答:

(1)写出过程I中 转化成
转化成 反应的化学方程式
反应的化学方程式_______ 。
(2)下列说法正确的是
(3)写出过程Ⅱ中 与
与 混合液反应的化学反应方程式
混合液反应的化学反应方程式_______ 。
(4) 的水溶液可以使品红褪色,其褪色原理如下
的水溶液可以使品红褪色,其褪色原理如下

该反应的反应类型为_______ 。
(5)设计实验方案检验 过程中硫元素是否完全被氧化
过程中硫元素是否完全被氧化_______ 。
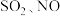 )可以按如下流程脱除或利用已知:混合气体X可直接排入空气。请回答:
)可以按如下流程脱除或利用已知:混合气体X可直接排入空气。请回答:
(1)写出过程I中
 转化成
转化成 反应的化学方程式
反应的化学方程式(2)下列说法正确的是
| A.煤的主要成分是碳单质 |
B.过程I中 的作用是还原剂 的作用是还原剂 |
| C.将副产品硫酸锌送往浸出车间电解可回收金属锌和产生可循环使用的硫酸 |
D.过程Ⅱ中的 也可用 也可用 代替 代替 |
(3)写出过程Ⅱ中
 与
与 混合液反应的化学反应方程式
混合液反应的化学反应方程式(4)
 的水溶液可以使品红褪色,其褪色原理如下
的水溶液可以使品红褪色,其褪色原理如下
该反应的反应类型为
(5)设计实验方案检验
 过程中硫元素是否完全被氧化
过程中硫元素是否完全被氧化
您最近一年使用:0次
名校
解题方法
10 . 生物炼铜技术是一种利用微生物开矿的湿式制铜技术,适用于从含铜量极低的矿石中冶炼出铜,具有环保、高效、低成本的优点。利用生物炼铜方法可以制备金属铜,同时生成副产品 ,相关转化过程如下图所示:
,相关转化过程如下图所示:

金属离子沉淀的 如下表。
如下表。
(1)请写出在硫化细菌作用下 转化生成
转化生成 的离子方程式
的离子方程式_____ 。,
(2)请选择合适的试剂X_____。
(3)调节 的范围在
的范围在_____ 之间,试剂是_____ (写出一种即可)
(4)测定 的纯度
的纯度
I.用分析天平称取 晶体,将其溶于硫酸后,加水稀释后用容量瓶配成
晶体,将其溶于硫酸后,加水稀释后用容量瓶配成 的待测液;
的待测液;
Ⅱ.取 的待测液置于锥形瓶中,用
的待测液置于锥形瓶中,用 的
的 标准液进行滴定,进行三次平行试验,消耗的
标准液进行滴定,进行三次平行试验,消耗的 标准液的体积如下表所示
标准液的体积如下表所示
① 标准液盛放在
标准液盛放在_____ (填“酸式”或“碱式”)滴定管中。
②滴定终点的现象是_____ 。
③该 晶体的纯度是
晶体的纯度是_____  (保留2位小数)。
(保留2位小数)。
④现测得该晶体纯度偏低,可能的原因是_____ 。
A.在配制待测液定容时仰视
B.原锥形瓶中有水
C.待测液配制过程中被氧气氧化
D.滴定前盛放 标准液的滴定管中滴定前有气泡,滴定后气泡消失
标准液的滴定管中滴定前有气泡,滴定后气泡消失
E.滴定终点时仰视读数
 ,相关转化过程如下图所示:
,相关转化过程如下图所示:
金属离子沉淀的
 如下表。
如下表。 |  |  | |
开始沉淀时的 | 1.5 | 4.2 | 6.3 |
完全沉淀时的 | 2.8 | 6.7 | 8.3 |
(1)请写出在硫化细菌作用下
 转化生成
转化生成 的离子方程式
的离子方程式(2)请选择合适的试剂X_____。
| A.新制氯水 | B.双氧水 | C.稀硝酸 | D.酸性高锰酸钾 |
(3)调节
 的范围在
的范围在(4)测定
 的纯度
的纯度I.用分析天平称取
 晶体,将其溶于硫酸后,加水稀释后用容量瓶配成
晶体,将其溶于硫酸后,加水稀释后用容量瓶配成 的待测液;
的待测液;Ⅱ.取
 的待测液置于锥形瓶中,用
的待测液置于锥形瓶中,用 的
的 标准液进行滴定,进行三次平行试验,消耗的
标准液进行滴定,进行三次平行试验,消耗的 标准液的体积如下表所示
标准液的体积如下表所示| 实验组 | 第一次 | 第二次 | 第三次 |
滴定前 溶液的体积 溶液的体积 | 0.05 | 0.20 | 1.10 |
滴定后 溶液的体积 溶液的体积 | 19.95 | 20.30 | 22.1 |
 标准液盛放在
标准液盛放在②滴定终点的现象是
③该
 晶体的纯度是
晶体的纯度是 (保留2位小数)。
(保留2位小数)。④现测得该晶体纯度偏低,可能的原因是
A.在配制待测液定容时仰视
B.原锥形瓶中有水
C.待测液配制过程中被氧气氧化
D.滴定前盛放
 标准液的滴定管中滴定前有气泡,滴定后气泡消失
标准液的滴定管中滴定前有气泡,滴定后气泡消失E.滴定终点时仰视读数
您最近一年使用:0次



