名校
解题方法
1 . 如图两圆相交部分A、B、C、D分别表示两物质间的反应。下列各对应反应的离子方程式书写不正确的是
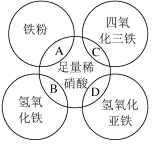

A.Fe+4H++ =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
| B.Fe3O4+8H+=Fe2++2Fe3++4H2O |
| C.Fe(OH)3+3H+=Fe3++3H2O |
D.3Fe(OH)2+10H++ =3Fe3++NO↑+8H2O =3Fe3++NO↑+8H2O |
您最近一年使用:0次
2022-08-24更新
|
128次组卷
|
14卷引用:山东省济南市第一中学2017届高三10月阶段测试化学试题
山东省济南市第一中学2017届高三10月阶段测试化学试题陕西省西安市第一中学2018届高三第三次月考化学试题(已下线)【艺体生百日捷进提升系列-技能方法】专题3.07 离子反应方面试题的解题方法与技巧(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第3讲 铁及其化合物【押题专练】(已下线)2019年8月2日 《每日一题》2020年一轮复习-“铁三角”及其应用(已下线)考点05 典型金属元素及其化合物——《备战2020年高考精选考点专项突破题集》福建省南安第一中学2020届高三上学期第二次月考化学试题2020届高三《新题速递·化学》1月第01期(考点01-06)湖南省岳阳市平江县第一中学2020-2021学年高二上学期10月联考化学试题宁夏石嘴山市平罗中学2022-2023学年高三上学期11月期中考试化学试题(已下线)新人教必修1第3章第一节第2课时铁的氧化物和氢氧化物(课中)云南省普洱市第一中学2021-2022学年高三下学期3月份考试理综化学试题黑龙江省牡丹江市第三高级中学2022-2023学年高三上学期第一次月考化学试题(已下线)BBWYhjhx1006.pdf
12-13高三上·浙江宁波·期中
名校
2 . NaNO2是一种食品添加剂,它能致癌。酸性KMnO4溶液与NaNO2反应的化学方程式是:  +
+ +____→Mn2++
+____→Mn2++ +H2O。下列叙述中正确的是
+H2O。下列叙述中正确的是
 +
+ +____→Mn2++
+____→Mn2++ +H2O。下列叙述中正确的是
+H2O。下列叙述中正确的是A.该反应中 被还原 被还原 |
| B.反应过程中溶液的pH减小 |
| C.生成1molNaNO3需消耗0.4molKMnO4 |
| D.横线中的粒子是OH- |
您最近一年使用:0次
2022-07-26更新
|
552次组卷
|
45卷引用:2013届浙江省宁波市效实中学高三上学期期中考试化学试卷
(已下线)2013届浙江省宁波市效实中学高三上学期期中考试化学试卷(已下线)2014届福建省南侨中学等五校高中毕业班期末摸底考试化学试卷(已下线)2014高考化学名师知识点精编 专题4氧化还原反应练习卷2016届湖南省益阳市箴言中学高三上学期第二次模拟测试化学试卷2017届新疆兵团农二师华山中学高三上学前考试化学试卷2016-2017学年河南省南阳一中高一上月考二化学卷2016-2017学年河南省南阳一中高一月考二化学卷天津市和平区2017-2018学年高一上学期期中质量调查化学试题辽宁省盘锦市高级中学2017-2018学年高二下学期期末考试化学试题2018-2019学年人教版高中化学必修一模块综合测评题(A)2018-2019学年苏教版高中化学必修一 模块综合测评(A)河南省安阳市第三十六中学2018-2019学年高二6月月考化学试题(已下线)专题2.3 氧化还原反应(练)-《2020年高考一轮复习讲练测》黑龙江省牡丹江市第一高级中学2019-2020学年高二上学期开学检测化学试题云南省漾濞二中2020届高三上学期开学考试化学试题江西省赣州市寻乌中学2020届高三上学期第一阶段考试化学试题(已下线)专题四 氧化还原反应(提分特训)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)衔接点09 氧化还原反应的表示-2020年【衔接教材·暑假作业】初高中衔接化学(已下线)第09讲 氧化还原反应的计算及方程式的配平(精练)——2021年高考化学一轮复习讲练测高一必修第一册(鲁科2019)考试帮 模块综合测评B卷人教版(2019)高一必修第一册 模块综合测评-B卷贵州省铜仁市思南中学2021届高三上学期第二次月考化学试题江西省上饶市万年中学2020-2021学年高一上学期期中考试化学试题湖南省武冈市第二中学2020-2021学年高一上学期第一次月考化学试题宁夏银川市第二中学2023-2024学年高三上学期统练二化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)衔接点09 氧化还原反应的表示-2021年初升高化学无忧衔接西藏拉萨市拉萨中学2022届高三上学期第一次月考理综化学试题黑龙江省哈尔滨市第六中学2021-2022学年高三上学期期中考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)4.2.2 氧化还原反应方程式的配平(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)黑龙江省哈尔滨市第九中学2021-2022学年高一上学期期中学业阶段性评价考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题01 物质及其变化-2023年高考化学一轮复习小题多维练(全国通用)黑龙江省佳木斯市第八中学2022-2023学年高三上学期第一次调研(开学考试)化学试题黑龙江省哈尔滨市香坊区第九中学校2021-2022学年高一上学期期中考试化学试题西藏林芝市第二高级中学2022-2023学年高三上学期第二次月考化学试题(已下线)第一章 化学物质及其变化 第5练 氧化还原反应的计算与方程式的配平(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)山东省枣庄市第三中学2022-2023学年高一上学期12月期中考试化学试题黑龙江省龙西北名校联合体2023-2024学年高三上学期期中考试化学试题黑龙江省齐齐哈尔市龙西北高中名校联盟2023-2024学年高三上学期10月联考化学试题江西省南昌市第十九中学2022-2023学年高一上学期12月第二次月考化学试卷
名校
解题方法
3 . 已知Mn2O 与S2-在酸性溶液中能发生反应: Mn2O
与S2-在酸性溶液中能发生反应: Mn2O +3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O
+3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O 中锰元素的化合价是
中锰元素的化合价是
 与S2-在酸性溶液中能发生反应: Mn2O
与S2-在酸性溶液中能发生反应: Mn2O +3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O
+3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O 中锰元素的化合价是
中锰元素的化合价是| A.+2 | B.+4 | C.+3 | D.+6 |
您最近一年使用:0次
2022-02-28更新
|
848次组卷
|
36卷引用:宁夏青铜峡市高级中学2020-2021学年高一12月月考化学试题
宁夏青铜峡市高级中学2020-2021学年高一12月月考化学试题河南省安阳市第三十六中学2017-2018学年高一上学期期中考试化学试题安徽省阜阳市第三中学2018-2019学年高一下学期开学考试化学试题夯基提能2020届高三化学选择题对题专练——氧化还原反应的实际应用广东省2020年普通高中学业水平考试化学合格性考试模拟试题(七)陕西省汉中市龙岗学校2019-2020学年高一上学期期末考试化学试题(已下线)【南昌新东方】江西省九江一中2013-2014学年高一上学期期中考试化学试题广东省珠海市第二中学2019-2020学年高一上学期期中考试化学试题广东省中山纪念中学2019-2020学年高一上学期第二次段考化学试题山东省济宁市邹城兖矿一中2020-2021学年度高一9月月考化学试题吉林公主岭范家屯一中2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】30湖南省岳阳市楚雄中学2020-2021学年高一上学期期中考试化学试题广东省湛江市第四中学2020-2021学年高一上学期期中考试化学试题北京市铁路第二中学2020-2021学年高一上学期期中考试化学试题(已下线)【南昌新东方】9. 2020 高一上 铁路一中 刘惠文 钟欣(已下线)【浙江新东方】双师 (55)河北衡水市第十四中学2020-2021学年高一上学期三调考试化学试题河北省衡水市武邑武罗学校2020-2021学年高一上学期期中考试化学试题河北省衡水市武强中学2020-2021学年高一上学期第一次月考化学试题黑龙江省鸡西市第一中学2020-2021学年高一上学期第一次月考化学试题云南省昆明市第八中学2020-2021学年高一上学期期中考试化学试题天津市滨海新区2020-2021学年高一上学期期末考试化学试题新疆巴音郭楞蒙古自治州第二中学2021届高三上学期第一次摸底考试化学试题云南省玉溪市江川区第二中学2020-2021学年高一下学期竞赛化学试题四川省成都市第七中学2021-2022学年高一上学期期中考试化学试题四川省攀枝花市第十五中学校2021-2022学年高一上学期期中考试化学试题安徽省安庆市第十中学2021-2022学年高一上学期10月月考化学试题江苏省宿迁市泗阳县实验高级中学2021-2022学年高一上学期第二次调研测试化学试题广东省梅州市兴宁市叶塘中学2021-2022学年高一上学期摸底考试化学试题浙江省绿谷联盟2022-2023学年高一上学期10月份考试化学试题 黑龙江省鹤岗市第一中学2022-2023学年高一上学期10月月考化学试题山西省晋城市第一中学校2022-2023学年高一上学期第二次调研考试化学试题四川省仁寿县铧强中学2021-2022学年高一上学期半期考试化学试题(已下线)专题七 氧化还原反应天津市宁河区2023-2024学年高一上学期期末考试化学试题
名校
4 . 工业上冶炼锡的第一步反应原理为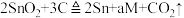 。下列说法中错误的是
。下列说法中错误的是
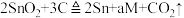 。下列说法中错误的是
。下列说法中错误的是A.该反应中 被还原 被还原 |
| B.a的值为3 |
| C.反应后有两种氧化产物 |
D.每生成1个 转移的电子数为8 转移的电子数为8 |
您最近一年使用:0次
2021-11-14更新
|
259次组卷
|
11卷引用:吉林省榆树一中2017-2018学年高一上学期期中考试化学试题
吉林省榆树一中2017-2018学年高一上学期期中考试化学试题广东省韶关市2017-2018学年高一化学上学期期中试题内蒙古通辽实验中学2017-2018学年高一上学期期末考试化学试题山西省灵丘县一中2017-2018学年高一上学期期中考试化学试卷云南省峨山彝族自治县第一中学2019-2020学年高一上学期期中考试化学试题云南省玉溪市华宁二中2019-2020学年高一上学期期中考试化学试题宁夏青铜峡市高级中学2021-2022学年高一上学期11月测试化学试题广东省八校2021-2022学年高一上学期期中调研考试 化学试题 河南省安阳县高级中学2021-2022学年高一上学期期中考试化学试题安徽师范大学附属中学2022-2023学年高一上学期10月选科诊断测试化学试题江苏省南京市第二十九中学2022-2023学年高一上学期10月月考化学试题
名校
5 . 现有下列10种物质:①铝,②纯醋酸,③CO2,④H2SO4,⑤Ba(OH)2,⑥红褐色的氢氧化铁胶体,⑦稀盐酸,⑧NaHSO4,⑨碳酸钙,⑩乙醇,请按要求书写离子方程式或化学方程式,
(1)上述物质中属于电解质的有_______ ,属于非电解质的有_______ ,既不属于电解质也不属于非电解质的有_______ (填序号)。
(2)写出⑧在水中的电离方程式为_______ 。
(3)向沸水中逐滴加入饱和FeCl3溶液,至液体呈透明的红褐色,写出化学方程式_______ 。
(4)已知酸性环境下,ClO-可将Mn2+氧化成MnO2,自身被还原成Cl-,该过程的离子反应方程式为_______ 。
(5)在酸性条件下,向含铬废水中加入FeSO4溶液,可将Cr2O 还原为Cr3+,该过程的离子方程式为
还原为Cr3+,该过程的离子方程式为_______ 。
(1)上述物质中属于电解质的有
(2)写出⑧在水中的电离方程式为
(3)向沸水中逐滴加入饱和FeCl3溶液,至液体呈透明的红褐色,写出化学方程式
(4)已知酸性环境下,ClO-可将Mn2+氧化成MnO2,自身被还原成Cl-,该过程的离子反应方程式为
(5)在酸性条件下,向含铬废水中加入FeSO4溶液,可将Cr2O
 还原为Cr3+,该过程的离子方程式为
还原为Cr3+,该过程的离子方程式为
您最近一年使用:0次
2021-10-29更新
|
212次组卷
|
2卷引用:黑龙江省鸡西市第一中学2020-2021学年高一上学期第一次月考化学试题
名校
解题方法
6 . 以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如图,下列叙述不正确的是

| A.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4 |
| B.向滤液中通入过量CO2、过滤、洗涤、灼烧沉淀可制得Al2O3 |
| C.隔绝空气焙烧时理论上反应消耗的n(FeS2)∶n(Fe2O3)=1∶5 |
| D.烧渣分离可以选择用磁铁将烧渣中的Fe3O4分离出来 |
您最近一年使用:0次
2021-09-30更新
|
1883次组卷
|
22卷引用:四川省成都市龙泉中学2021届高三上学期开学考试化学试题
四川省成都市龙泉中学2021届高三上学期开学考试化学试题(已下线)易错21 化学工艺流程类选择题-备战2021年高考化学一轮复习易错题宁夏回族自治区银川一中2023-2024学年高三上学期第五次月考理科综合试题河南省信阳市2021届高三上学期第二次教学质量检测化学试题江苏省苏州中学2020-2021学年度第二学期期中考试(已下线)难点1 化工流程微设计-2021年高考化学【热点·重点·难点】专练(新高考)(苏教版2019)必修第二册专题9 金属与人类文明 B 素养拓展区江苏省常熟市2021-2022学年高二学生暑期自主学习调查化学试题(已下线)第1周 周测卷-备战2022年高考化学周测与晚练(新高考专用)河北省石家庄市第二中学2022届高三上学期11月第三次考试化学试题(已下线)卷05 工艺流程型选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)专题14物质的反应和转化-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题13物质的反应和转化-2022年高考真题+模拟题汇编(全国卷)(已下线)专题14物质的反应和转化-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题八工艺流程图(讲)广东省广州市中山大学附属中学2021届高三下学期3月月考化学试题河北省部分重点高中2023-2024学年高三上学期第一次综合素养测评化学试题广东省河源中学2023-2024学年上学期高三年级一调考试化学试题河北省衡水中学2023-2024学年高三上学期一调考试化学试题河北省石家庄市部分名校2024届高三上学期一调考试化学试题2024届陕西省西安市第一中学高三上学期模拟测试理科综合试题-高中化学辽宁省部分重点中学协作体2024届高三下学期高考模拟考试化学试题
9-10高一·浙江·阶段练习
名校
解题方法
7 . 已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:Fe3+→Fe2+;MnO →Mn2+;Cl2→2Cl-;HNO2→NO,如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
→Mn2+;Cl2→2Cl-;HNO2→NO,如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
 →Mn2+;Cl2→2Cl-;HNO2→NO,如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
→Mn2+;Cl2→2Cl-;HNO2→NO,如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是| A.Fe3+ | B.MnO | C.Cl2 | D.HNO2 |
您最近一年使用:0次
2021-08-20更新
|
1213次组卷
|
25卷引用:09-10年瑞安中学高一提前招阶段性检测化学卷
(已下线)09-10年瑞安中学高一提前招阶段性检测化学卷安徽省淮南市第二中学2017-2018学年高一上学期第二次月考化学试题【全国百强校】甘肃省静宁县第一中学2019届高三上学期第一次模拟考试化学试题【全国百强校】北京市第四中学2018-2019学年高一上学期期末考试化学试题第2章《元素与物质世界》期中复习检测试卷黑龙江省鹤岗市第一中学2019-2020学年高一上学期期中考试化学试题黑龙江省大庆市第四中学2019-2020学年高一上学期第二次月考化学试题福建省泉州市泉港区第一中学2019-2020学年高一上学期第二次月考化学试题黑龙江省大庆市第一中学高中化学必修一第二章 第三节 氧化还原第3课时(习题课)江苏省启东中学2020年人教版高中化学必修1期末复习第二章 化学物质及其变化(三)湖北省武汉市部分重点中学2019-2020学年高一上学期期末考试化学试题(已下线)上海市十三校2012届高三第二次联考化学试题江西省南昌市进贤一中2019-2020学年高一上学期期末考试化学试题重庆市巴蜀中学2019-2020学年高一上学期期末考试化学试题黑龙江省双鸭山市第一中学2020-2021学年高一10月月考化学试题(已下线)福建省平和一中、南靖一中等五校2018-2019学年高一年上学期第二次联考化学试题山西省运城市新绛县第二中学2019-2020学年高一下学期6月月考化学试题(已下线)【浙江新东方】在线化学 (11)(已下线)【南昌新东方】13. 2020 高一上 莲塘二中 期中 程秀丽辽宁师范大学附属中学2020-2021学年高一10月模块考试 化学化学试题宁夏大学附属中学2020-2021学年高一上学期期末考试化学试题江西省南昌市进贤县第一中学2021届高三上学期第一次月考化学试题(已下线)专题2.3.1 物质的量的单位——摩尔(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)(已下线)2.3.1物质的量和摩尔质量-同步学习必备知识河北省张家口市宣化第一中学2022-2023学年高一上学期12月月考化学试题
名校
8 . 硝酸厂的烟气中含有大量的氮氧化物( ),将烟气与
),将烟气与 的混合气体通入
的混合气体通入 与
与 (
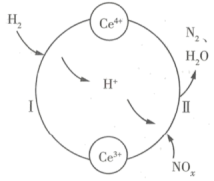
( 为铈元素)的混合溶液中实现无害化处理,其转化过程如图所示。下列说法正确的是
为铈元素)的混合溶液中实现无害化处理,其转化过程如图所示。下列说法正确的是
 ),将烟气与
),将烟气与 的混合气体通入
的混合气体通入 与
与 (
( 为铈元素)的混合溶液中实现无害化处理,其转化过程如图所示。下列说法正确的是
为铈元素)的混合溶液中实现无害化处理,其转化过程如图所示。下列说法正确的是
A.过程Ⅰ发生反应的离子方程式为 |
B. 时,过程Ⅱ中氧化剂与还原剂的物质的量之比为 时,过程Ⅱ中氧化剂与还原剂的物质的量之比为 |
C.处理过程中,混合溶液中 和 和 总数减少 总数减少 |
D.该转化过程的实质为 被 被 还原 还原 |
您最近一年使用:0次
2021-06-05更新
|
761次组卷
|
23卷引用:宁夏石嘴山市第三中学2021届高三上学期第一次月考化学试题
宁夏石嘴山市第三中学2021届高三上学期第一次月考化学试题北京市通州区2020届高三上学期期末摸底考试化学试题北京市2020届高三下学期周末测试化学试题天津市南开区2020届高三年级第二次模拟考试化学试题(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编(已下线)专题04 氧化还原反应-2020年高考真题和模拟题化学分项汇编(已下线)易错05 氧化还原反应概念及规律-备战2021年高考化学一轮复习易错题广东省广州市2021届高三年级阶段训练化学试题山西省运城市景胜中学2020-2021学年高一10月月考化学试题山东省潍坊市诸城一中2021届高三11月份模拟化学试题甘肃省武威第一中学2021届高三上学期第三次阶段性考试化学试题河南省顶级名校2021届高三年级上学期期中考试化学试题江西师范大学附属中学2020-2021学年高一下学期4月月考化学试题江苏省扬州中学2020-2021高一下学期5月月考化学试题江西省石城中学2020-2021学年高一下学期第二次月考化学试题(苏教版2019)必修第二册专题7 氮与社会可持续发展 C 高考挑战区黑龙江省八校2022届高三上学期期中联合考试化学试题江苏省连云港市赣榆第一中学2021-2022学年高三上学期10月月考化学试题(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-练习内蒙古海拉尔第二中学2021-2022学年高三上学期第三次阶段考化学试题云南省丽江市2021-2022学年高一下学期期末考试化学试题山东省枣庄滕州市2022-2023学年高三上学期期中考试化学试题山东省滕州市第二中学2022-2023学年高三上学期11月定时检测化学试题
名校
解题方法
9 . 做实验时不小心粘了一些高锰酸钾,皮肤上的斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为:MnO +C2O
+C2O +H+→CO2↑+Mn2++□,关于此反应的叙述正确的是
+H+→CO2↑+Mn2++□,关于此反应的叙述正确的是
 +C2O
+C2O +H+→CO2↑+Mn2++□,关于此反应的叙述正确的是
+H+→CO2↑+Mn2++□,关于此反应的叙述正确的是A.该反应的氧化剂是C2O |
| B.该反应右边方框内的产物是OH- |
| C.该反应中生成1molCO2电子转移总数是5NA |
| D.配平该反应式后,H+的系数是16 |
您最近一年使用:0次
2021-03-10更新
|
288次组卷
|
4卷引用:宁夏青铜峡市高级中学2020届高三上学期第一次月考化学试题
宁夏青铜峡市高级中学2020届高三上学期第一次月考化学试题河北省衡水市武邑武罗学校2020-2021学年高三上学期期中考试化学试题(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)
名校
解题方法
10 . HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是_______ (填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,能用来区分NaNO2和NaCl的是_______ (填序号)。
A.分别溶于水看溶解情况
B.在酸性条件下加入KI淀粉溶液来区别
C.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:_______ 。
(4)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是_______ (填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑,_____ ,若有1molFeSO4反应,则反应中转移____ mol电子。
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,能用来区分NaNO2和NaCl的是
A.分别溶于水看溶解情况
B.在酸性条件下加入KI淀粉溶液来区别
C.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
(4)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑,
您最近一年使用:0次



