名校
解题方法
1 . 金属及其化合物在生产中用途广泛。从含铜丰富的自然资源黄铜矿(CuFeS2)中冶炼铜的工艺流程如图:
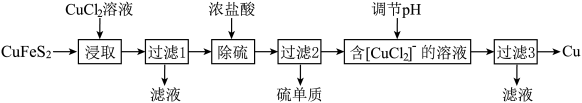
已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为___ 。
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为___ 。
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是___ 。(填离子符号)
(4)过滤3所得滤液中可以循环使用的物质有___ 和___ 。为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为___ 。
(5)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,发生的反应为6CuFeS2+13O2 3Cu2S+2Fe3O4+9O2,Cu2S+O2
3Cu2S+2Fe3O4+9O2,Cu2S+O2 2Cu+SO2。此工艺与前一工艺相比主要缺点有
2Cu+SO2。此工艺与前一工艺相比主要缺点有____ (任答一点)。

已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是
(4)过滤3所得滤液中可以循环使用的物质有
(5)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,发生的反应为6CuFeS2+13O2
 3Cu2S+2Fe3O4+9O2,Cu2S+O2
3Cu2S+2Fe3O4+9O2,Cu2S+O2 2Cu+SO2。此工艺与前一工艺相比主要缺点有
2Cu+SO2。此工艺与前一工艺相比主要缺点有
您最近一年使用:0次
2 . 用CuS、Cu2S处理酸性废水中的Cr2O ,发生反应如下:
,发生反应如下:
反应Ⅰ:CuS+Cr2O +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)
反应Ⅱ:Cu2S+Cr2O +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)
下列有关说法正确的是( )
 ,发生反应如下:
,发生反应如下:反应Ⅰ:CuS+Cr2O
 +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)反应Ⅱ:Cu2S+Cr2O
 +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)下列有关说法正确的是( )
A.反应Ⅰ和Ⅱ中Cu2+、SO 都是氧化产物 都是氧化产物 |
| B.反应Ⅱ中还原剂、氧化剂的物质的量之比为2∶5 |
C.处理1molCr2O 时反应Ⅰ、Ⅱ中消耗H+的物质的量相等 时反应Ⅰ、Ⅱ中消耗H+的物质的量相等 |
D.反应Ⅰ、Ⅱ中每处理1molCr2O ,转移电子的数目相等 ,转移电子的数目相等 |
您最近一年使用:0次
2020-10-03更新
|
153次组卷
|
2卷引用:宁夏银川一中2021届高三上学期第二次月考理综化学试题
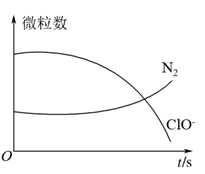
3 . 某离子反应涉及H2O、ClO-、 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
| A.该反应中Cl-为氧化产物 |
| B.消耗1个还原剂微粒,转移6e- |
C. 被ClO-氧化成N2 被ClO-氧化成N2 |
| D.反应后溶液的酸性减弱 |
您最近一年使用:0次
2020-10-02更新
|
1134次组卷
|
8卷引用:宁夏回族自治区石嘴山市平罗中学2020届高三上学期期中考试化学试题
4 . 过氧化氢H2O2(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是______ (填字母)。
(2)H2O2既体现氧化性又体现还原性的反应是_______ (填字母)。
(3)在稀硫酸中,KMnO4和H2O2能构成原电池。其中负极反应为:H2O2-2e-=2H++O2↑,正极反应: +5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:
+5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:___________ 。
(4)在K2Cr2O7+14HCl=2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3mol电子转移时生成Cl2的体积为______ (标准状况),被氧化的HCl的物质的量为___________ 。
(5)除去镁粉中混入的铝粉杂质用____ 溶解、___ 方法分离,化学反应方程式为___ 。
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是
(2)H2O2既体现氧化性又体现还原性的反应是
(3)在稀硫酸中,KMnO4和H2O2能构成原电池。其中负极反应为:H2O2-2e-=2H++O2↑,正极反应:
 +5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:
+5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:(4)在K2Cr2O7+14HCl=2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3mol电子转移时生成Cl2的体积为
(5)除去镁粉中混入的铝粉杂质用
您最近一年使用:0次
14-15高一上·浙江宁波·期中
名校
解题方法
5 . 羟胺( )是一种还原剂,能将某些氧化剂还原。现用25.00mL
)是一种还原剂,能将某些氧化剂还原。现用25.00mL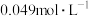 羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的
羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的 恰好与24.50mL
恰好与24.50mL '酸性
'酸性 溶液完全反应。已知:
溶液完全反应。已知: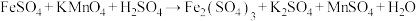 (未配平),则羟胺的氧化产物是
(未配平),则羟胺的氧化产物是
 )是一种还原剂,能将某些氧化剂还原。现用25.00mL
)是一种还原剂,能将某些氧化剂还原。现用25.00mL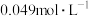 羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的
羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的 恰好与24.50mL
恰好与24.50mL '酸性
'酸性 溶液完全反应。已知:
溶液完全反应。已知: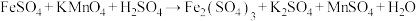 (未配平),则羟胺的氧化产物是
(未配平),则羟胺的氧化产物是A. | B. | C.NO | D. |
您最近一年使用:0次
2020-09-23更新
|
394次组卷
|
15卷引用:2014-2015浙江省宁波市效实中学高一上学期期中化学试卷
(已下线)2014-2015浙江省宁波市效实中学高一上学期期中化学试卷2014-2015浙江省杭州市西湖中学高一12月月考化学试卷2018-2019学年人教版高中化学必修一模块综合测评题(A)2018-2019学年苏教版高中化学必修一 模块综合测评(A)【全国百强校】吉林省实验中学2019届高三上学期期中考试化学试题江西省上饶中学2019届高三上学期期中考试化学试题2020届高三化学二轮复习 氧化还原反应过关检测(强化训练)(已下线)【南昌新东方】莲塘一中化学高一10月份高一必修第一册(鲁科2019)考试帮 模块综合测评B卷福建师范大学第二附属中学2020届高三上学期期中考试化学试题宁夏固原市第一中学2023届高三上学期第一次月考化学试题(已下线)【苏州新东方】 江苏省吴江中学2021-2022学年高二上学期开学检测化学试卷辽宁省沈阳市第一二〇中学2021-2022学年高一上学期期中考试化学试题(已下线)第一章 化学物质及其变化 第5练 氧化还原反应的计算与方程式的配平(已下线)第5讲 氧化还原反应方程式的配平与计算
2014高三·全国·专题练习
名校
6 . 已知反应:
①SO2+2Fe3++2H2O→SO +2Fe2++W
+2Fe2++W
②Cr2O +aFe2++bH+→Cr3++Fe3++H2O
+aFe2++bH+→Cr3++Fe3++H2O
下列有关说法正确的是( )
①SO2+2Fe3++2H2O→SO
 +2Fe2++W
+2Fe2++W②Cr2O
 +aFe2++bH+→Cr3++Fe3++H2O
+aFe2++bH+→Cr3++Fe3++H2O下列有关说法正确的是( )
| A.还原性: SO2>Cr3+ |
| B.方程式②中,a=6,b=7 |
C.Cr2O 能将Na2SO3氧化成Na2SO4 能将Na2SO3氧化成Na2SO4 |
| D.方程式①中W为OH- |
您最近一年使用:0次
2020-09-10更新
|
408次组卷
|
15卷引用:宁夏青铜峡市高级中学(吴忠中学分校)2020届高三上学期第二次月考化学试题
宁夏青铜峡市高级中学(吴忠中学分校)2020届高三上学期第二次月考化学试题(已下线)2014届高考化学二轮复习江苏专用 第3讲两种重要的化学反应练习卷江西省金溪县第一中学2018届高三9月(三周考)月考化学试题福建省莆田第六中学2018届高三上学期期中考试化学试题B卷福建省莆田第六中学2018届高三上学期期中考试化学试题(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第3讲 氧化还原反应【押题专练】陕西省渭南中学2019届高三上学期第三次质量检测化学试题陕西省西安市远东第一中学2019届高三上学期10月月考化学试题云南省泸西县一中2018-2019学年高一上学期期中考试化学试题(已下线)2019年7月18日 《每日一题》2020届高考一轮复习—— 氧化还原反应的配平甘肃省临夏回族自治州临夏中学2020届高三上学期期中考试化学试题陕西省渭南市澄城县城关中学2019-2020学年高二检测化学试题鲁科版(2019)高一必修第一册第2章 元素与物质世界 第3节 氧化还原反应 专题4 氧化还原反应的计算及方程式的配平黑龙江省伊春市伊美区第二中学2021届高三上学期开学考试化学试题河北省张家口市崇礼区第一中学2021届高三上学期期中考试化学试题
名校
7 . O3具有强氧化性,将O3通入KI溶液中发生反应: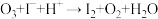 (未配平),下列说法正确的是
(未配平),下列说法正确的是
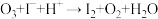 (未配平),下列说法正确的是
(未配平),下列说法正确的是A.配平后的离子方程式为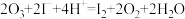 |
| B.每生成1分子I2,转移2个电子 |
| C.O2是还原产物之一 |
| D.该反应能说明O2的氧化性强于I2 |
您最近一年使用:0次
2020-09-04更新
|
618次组卷
|
7卷引用:2017届宁夏六盘山高级中学高三上第一次月考化学试卷
2017届宁夏六盘山高级中学高三上第一次月考化学试卷(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第3讲 氧化还原反应【押题专练】(已下线)衔接点09 氧化还原反应的表示-2020年【衔接教材·暑假作业】初高中衔接化学安徽省亳州市涡阳县育萃高级中学2019-2020学年高二下学期摸底考试化学试题人教版(2019)高一必修第一册第一章 物质及其变化 素养拓展区新疆伊犁奎屯市第一高级中学2020-2021学年高一上学期期末考试化学试题(已下线)衔接点09 氧化还原反应的表示-2021年初升高化学无忧衔接
名校
8 . 亚硝酸钠可使肉制品色泽粉红,外观上好看诱人,大量食用会致癌。
(1)NaNO2俗称“工业盐”,其外观与食盐相似,误食会中毒,可通过化学实验加以鉴别。如向NaNO2的酸性溶液中加入KI固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验 。
。
①该反应中被氧化的元素是________ 。
②完成下列反应的化学方程式并配平:NaNO2+KI+H2SO4= + +I2+NO↑+ ,________ 。
③标准状况下,该反应中每转移1mol e-,生成气体的体积是________ 。
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为:2NO2+Na2CO3=NaNO2+NaNO3+CO2↑。每产生33.6L(标准状况下)CO2,吸收液质量将增加________ g。
(1)NaNO2俗称“工业盐”,其外观与食盐相似,误食会中毒,可通过化学实验加以鉴别。如向NaNO2的酸性溶液中加入KI固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验
 。
。①该反应中被氧化的元素是
②完成下列反应的化学方程式并配平:NaNO2+KI+H2SO4= + +I2+NO↑+ ,
③标准状况下,该反应中每转移1mol e-,生成气体的体积是
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为:2NO2+Na2CO3=NaNO2+NaNO3+CO2↑。每产生33.6L(标准状况下)CO2,吸收液质量将增加
您最近一年使用:0次
名校
9 . MnO2在电池、玻璃、有机合成等工业生产中应用广泛。利用粗MnO2(含有杂质MnO和MnCO3)制取纯MnO2的流程如图:
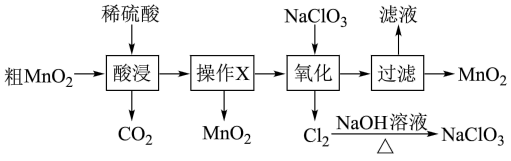
下列说法错误的是

下列说法错误的是
| A.酸浸过程中可以用浓盐酸代替稀硫酸 |
| B.操作X的名称是过滤 |
C.氧化过程发生反应的离子方程式为:5Mn2++2ClO +4H2O=5MnO2↓+Cl2↑+8H+ +4H2O=5MnO2↓+Cl2↑+8H+ |
| D.Cl2与NaOH溶液加热反应得到的NaClO3可以循环使用 |
您最近一年使用:0次
2020-08-24更新
|
1498次组卷
|
9卷引用:宁夏石嘴山市第三中学2021届高三上学期第二次月考化学试题
宁夏石嘴山市第三中学2021届高三上学期第二次月考化学试题广东省惠州市2021届高三上学期第一次调研考试化学试题湖南省长沙市雅礼中学2021届高三上学期第二次月考化学试题(已下线)学科网2020年高三11月大联考考后强化卷(新课标Ⅲ卷)(已下线)学科网2020年高三11月大联考考后强化卷(新课标Ⅱ卷)甘肃省嘉峪关市第一中学2021届高三上学期二模考试化学试题甘肃省民乐县第一中学2021-2022学年高三上学期10月诊断考试化学试题湖北省仙桃中学、天门中学(A班)2021-2022学年高二上学期期中考试化学试题新疆第二师八一中学2022-2023学年高三上学期第一次月考化学试题
名校
10 . 明矾[KAl(SO4)2·12H2O]在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、Al2O3及少量SiO2和FeO·xFe2O3)可制备明矾。工艺流程如图:

回答下列问题:
(1)明矾净水的原理是_______ (用离子方程式表示)。
(2)操作Ⅰ是_____ ,操作Ⅱ是蒸发浓缩、_____ 、过滤、____ 、干燥。
(3)检验滤液A中是否存在Fe2+的试剂是______ (只用一种试剂)。
(4)将铝灰投入氢氧化钠溶液中生成气体的化学方程式是______ ,在滤液A中加入高锰酸钾发生反应的离子方程式为(该条件下MnO 转化为Mn2+):
转化为Mn2+):_________ 。
(5)已知:在pH=3、加热条件下,MnO 可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:
可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:________ ,滤渣2含有的物质是_______ 。

回答下列问题:
(1)明矾净水的原理是
(2)操作Ⅰ是
(3)检验滤液A中是否存在Fe2+的试剂是
(4)将铝灰投入氢氧化钠溶液中生成气体的化学方程式是
 转化为Mn2+):
转化为Mn2+):(5)已知:在pH=3、加热条件下,MnO
 可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:
可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:
您最近一年使用:0次
2020-08-18更新
|
186次组卷
|
4卷引用:宁夏青铜峡市高级中学2021届高三12月月考理综化学试题
宁夏青铜峡市高级中学2021届高三12月月考理综化学试题黑龙江省哈尔滨师范大学青冈实验中学校2020届高三10月月考化学试题河南省洛阳市第一高级中学2021届高三9月月考化学试题(已下线)专题09 金属矿物的开发和利用(限时精练)-2022年高三毕业班化学常考点归纳与变式演练



