名校
解题方法
1 . 镍是一种常用的有机催化剂,且在电磁领域应用广泛。某工厂以含镍废料(主要含NiO、Fe2O3、FeO、Al2O3、SiO2、CaO)为原料制备镍单质的流程如图:
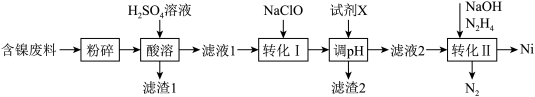
已知:ⅰ.Ni2+在弱酸性环境中易水解,氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度);
ⅱ.常温下,Ksp[Fe(OH)3]=4×10-38,Ksp[Fe(OH)2]=8×10-16,Ksp[Al(OH)3]=1×10-33,Ksp[Ni(OH)2]=2×10-15,离子浓度低于1×10-5 mol·L-1时,认为沉淀完全。
回答下列问题:
(1)“粉碎”的目的是___________ ;“滤渣1”的主要成分为___________ 、___________ 。
(2)“转化Ⅰ”的目的为___________ (用离子方程式表示)。
(3)为了更加环保,有人用H2O2代替NaClO进行“转化Ⅰ”,发现所用H2O2远远高于理论用量,分析造成这一结果的原因为___________ 。
(4)调pH的目的是沉淀溶液中的铁和铝,调节pH=5时,___________ (选填“能”或“不能”)达到目的,“试剂X”可以是___________ (填选项字母)。
A.FeO B.Fe2O3 C.NiO D.Al2O3
(5)N2H4的电子式为___________ ;“转化Ⅱ”中发生反应的离子方程式为___________ 。

已知:ⅰ.Ni2+在弱酸性环境中易水解,氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度);
ⅱ.常温下,Ksp[Fe(OH)3]=4×10-38,Ksp[Fe(OH)2]=8×10-16,Ksp[Al(OH)3]=1×10-33,Ksp[Ni(OH)2]=2×10-15,离子浓度低于1×10-5 mol·L-1时,认为沉淀完全。
回答下列问题:
(1)“粉碎”的目的是
(2)“转化Ⅰ”的目的为
(3)为了更加环保,有人用H2O2代替NaClO进行“转化Ⅰ”,发现所用H2O2远远高于理论用量,分析造成这一结果的原因为
(4)调pH的目的是沉淀溶液中的铁和铝,调节pH=5时,
A.FeO B.Fe2O3 C.NiO D.Al2O3
(5)N2H4的电子式为
您最近一年使用:0次
2020-12-24更新
|
282次组卷
|
2卷引用:辽宁省兴城市高级中学2022-2023学年高二上学期期末线上质量检测化学试题
2 . 二氧化氯(ClO2)是一种优良的消毒剂,可用氯酸钠和双氧水在酸性条件下制备,反应方程式为NaClO3H2O2H2SO4ClO2Na2SO4H2OO2(未配平)。下列说法不正确的是
| A.NaClO3做氧化剂,发生还原反应 |
| B.将该方程式配平后H2O的化学计量数应为2 |
| C.NaClO3与H2O2的化学计量系数之比为2:1 |
| D.反应过程中每生成2.24LO2转移0.2mol电子 |
您最近一年使用:0次
2020-11-10更新
|
833次组卷
|
7卷引用:辽宁省东北师范大学连山实验高中2022-2023学年高一上学期1月期末化学试题
辽宁省东北师范大学连山实验高中2022-2023学年高一上学期1月期末化学试题湖南省长沙市长郡教育集团2020-2021学年高一上学期期中考试化学试题湖南省长沙市长郡中学2020-2021学年高一上学期期中考试化学试题黑龙江省富锦市第一中学2022-2023学年高一上学期期末考试化学试题黑龙江省鹤岗市第一中学2022-2023学年高一上学期期末考试化学试题 (已下线)第二章 海水中的重要元素——钠和氯(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)黑龙江省鹤岗市第一中学2022-2023学年高一下学期开学考试化学试题
3 . 按要求回答问题
(1)有下列物质:①石墨;②氯水;③氢氧化钠固体;④稀硫酸;⑤熔融氯化钾;⑥醋酸;
⑦液态氯化氢;⑧硫酸钡;⑨液氨;⑩蔗糖。
其中属于电解质的有_____ ;属于非电解质的有______ .(填编号)
(2)某无色透明溶液中可能含有K+、Fe2+、Fe3+、Mg2+、Ba2+、 、Cl-、
、Cl-、 、
、 、
、 中的若干种离子。某同学取 50 mL 的溶液进行如下实验:
中的若干种离子。某同学取 50 mL 的溶液进行如下实验:
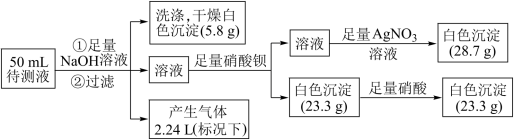
根据实验判断下列说法中正确的是_____
A.原溶液中一定只含有 、Mg2+、
、Mg2+、 、Cl-
、Cl-
B.原溶液中一定不存在 Fe2+、Fe3+、Ba2+、 、
、
C.原溶液中可能含有
D.原溶液中 c(K+)=2mol/L
(3)已知:Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;2SO2+SeO2+2H2O=Se+2 +4H+,则SeO2、H2SO4(浓)、SO2 的氧化性由强到弱的顺序是
+4H+,则SeO2、H2SO4(浓)、SO2 的氧化性由强到弱的顺序是_____ 。
(4)已知 4NO2+2CO(NH2)2→2CO2+4N2+4H2O+O2(已知尿素中 N 为-3 价),该反应的氧化产物为_____ ;若吸收 0.15mol NO2,则转移电子_____ mol。
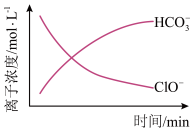
(5)处理某废水时,反应过程中部分离子浓度与反应进程 关系如图,反应过程中主要存在 N2、 、ClO−、CNO−(C+4 价)、Cl−等微粒。写出处理该废水时发生反应的离子方程式
、ClO−、CNO−(C+4 价)、Cl−等微粒。写出处理该废水时发生反应的离子方程式__ 。
(1)有下列物质:①石墨;②氯水;③氢氧化钠固体;④稀硫酸;⑤熔融氯化钾;⑥醋酸;
⑦液态氯化氢;⑧硫酸钡;⑨液氨;⑩蔗糖。
其中属于电解质的有
(2)某无色透明溶液中可能含有K+、Fe2+、Fe3+、Mg2+、Ba2+、
 、Cl-、
、Cl-、 、
、 、
、 中的若干种离子。某同学取 50 mL 的溶液进行如下实验:
中的若干种离子。某同学取 50 mL 的溶液进行如下实验:
根据实验判断下列说法中正确的是
A.原溶液中一定只含有
 、Mg2+、
、Mg2+、 、Cl-
、Cl-B.原溶液中一定不存在 Fe2+、Fe3+、Ba2+、
 、
、
C.原溶液中可能含有

D.原溶液中 c(K+)=2mol/L
(3)已知:Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;2SO2+SeO2+2H2O=Se+2
 +4H+,则SeO2、H2SO4(浓)、SO2 的氧化性由强到弱的顺序是
+4H+,则SeO2、H2SO4(浓)、SO2 的氧化性由强到弱的顺序是(4)已知 4NO2+2CO(NH2)2→2CO2+4N2+4H2O+O2(已知尿素中 N 为-3 价),该反应的氧化产物为
(5)处理某废水时,反应过程中部分离子浓度与反应进程 关系如图,反应过程中主要存在 N2、
 、ClO−、CNO−(C+4 价)、Cl−等微粒。写出处理该废水时发生反应的离子方程式
、ClO−、CNO−(C+4 价)、Cl−等微粒。写出处理该废水时发生反应的离子方程式
您最近一年使用:0次
解题方法
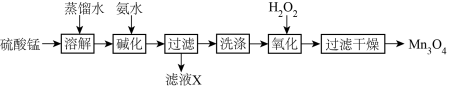
4 . 四氧化三锰既是磁性材料锰锌铁氧体(ZnaMnbFecO4,Fe元素为+3价,Zn、Mn元素化合价相同)的重要生产原料,也常被用作氮氧化物分解的催化剂。近年来对制备高品质四氧化三锰的研究越来越受到重视。以硫酸锰为原料制备四氧化三锰的工艺流程如图:
回答下列问题:
(1)“溶解”时需用玻璃棒,其作用为_____ 。
(2)“碱化”时反应离子方程式为______ 。
(3)滤液X中含有的溶质为_____ (填化学式)。
(4)简述“碱化”得到的沉淀是否洗涤干净的方法:_______ 。
(5)“氧化”时发生的化学反应方程式为_____ 。
(6)取30.2gMnSO4经上述工艺过程后,生成____ g Mn3O4(假设Mn元素不损失)。

回答下列问题:
(1)“溶解”时需用玻璃棒,其作用为
(2)“碱化”时反应离子方程式为
(3)滤液X中含有的溶质为
(4)简述“碱化”得到的沉淀是否洗涤干净的方法:
(5)“氧化”时发生的化学反应方程式为
(6)取30.2gMnSO4经上述工艺过程后,生成
您最近一年使用:0次
5 . 水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解氧。实验步骤及测定原理如下:
I.取样、氧的固定将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成 MnO(OH)2,实现氧的固定。
II.酸化将固氧后的水样酸化,MnO(OH)2 被 I- 还原为Mn2+
III.用标准 Na2S2O3溶液滴定生成的 I2(2S2O +I2=2I- + S4O
+I2=2I- + S4O )。
)。
回答下列问题:
(1)写出步骤 II 的离子反应方程式___________
(2)取 100 .00mL 水样经固氧、酸化后,用 a mol•L-1Na2S2O3溶液滴定,以淀粉溶液作指示剂,滴定终点的现象是___________ ,且半分钟内不变色。若消耗 Na2S2O3 溶液的体积为 b mL, 则水样中溶解氧的含量为__________ mg•L-1
I.取样、氧的固定将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成 MnO(OH)2,实现氧的固定。
II.酸化将固氧后的水样酸化,MnO(OH)2 被 I- 还原为Mn2+
III.用标准 Na2S2O3溶液滴定生成的 I2(2S2O
 +I2=2I- + S4O
+I2=2I- + S4O )。
)。回答下列问题:
(1)写出步骤 II 的离子反应方程式
(2)取 100 .00mL 水样经固氧、酸化后,用 a mol•L-1Na2S2O3溶液滴定,以淀粉溶液作指示剂,滴定终点的现象是
您最近一年使用:0次
解题方法
6 . 亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
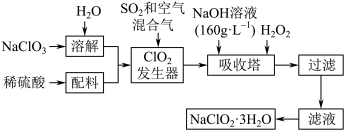
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO3•3H2O;
②纯ClO2易分解爆炸, 一般用稀有气体或空气稀释到 10% 以下较安全;
③HClO2 可看成是强酸;
④ClO2常温下为气态 。
(1)160 g•L-1 NaOH溶液的物质的量浓度为______________ mol•L-1,若要计算该溶液溶质的质量分数,还需要的一个条件是_______________________ 。
(2)在发生器中鼓入空气的作用可能是______________ (填序号)。
A. 将 SO2氧化成SO3,增强酸性
B. 稀释 ClO2以防止爆炸
C. 将 NaClO3氧化成ClO2
(3)ClO2 发生器中发生的化学反应方程式为_____ ,吸收塔内的反应的离子反应方程式为_______ ;
(4)吸收塔中为防止 NaClO2被 还原成 NaCl所用还原剂的还原性应适中。 除H2O2外,还可以选择的还原剂是_____ (填序号)。
A Na2O2 B Na2S C FeCl2 D O3

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO3•3H2O;
②纯ClO2易分解爆炸, 一般用稀有气体或空气稀释到 10% 以下较安全;
③HClO2 可看成是强酸;
④ClO2常温下为气态 。
(1)160 g•L-1 NaOH溶液的物质的量浓度为
(2)在发生器中鼓入空气的作用可能是
A. 将 SO2氧化成SO3,增强酸性
B. 稀释 ClO2以防止爆炸
C. 将 NaClO3氧化成ClO2
(3)ClO2 发生器中发生的化学反应方程式为
(4)吸收塔中为防止 NaClO2被 还原成 NaCl所用还原剂的还原性应适中。 除H2O2外,还可以选择的还原剂是
A Na2O2 B Na2S C FeCl2 D O3
您最近一年使用:0次
7 . 氮的氧化物和硫的氧化物是主要的大气污染物,烟气脱硫脱硝是环境治理的热点问题。回答下列问题:
(1)目前柴油汽车都用尿素水解液消除汽车尾气中的NO,水解液中的NH3将NO还原为无害的物质。该反应中氧化剂与还原剂物质的量之比为___ 。
(2)KMnO4/CaCO3浆液可协同脱硫,在反应中MnO4-被还原为MnO 。
。
①KMnO4脱硫(SO2)的离子方程式为___ 。
②KMnO4/CaCO3浆液中KMnO4与CaCO3最合适的物质的量之比为___ 。
(3)利用NaClO2/H2O2酸性复合吸收剂可同时对NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,n(H2O2)/n(NaClO2)、溶液pH对脱硫脱硝的影响如图所示:

图a和图b中可知脱硫脱硝最佳条件是___ 。
(1)目前柴油汽车都用尿素水解液消除汽车尾气中的NO,水解液中的NH3将NO还原为无害的物质。该反应中氧化剂与还原剂物质的量之比为
(2)KMnO4/CaCO3浆液可协同脱硫,在反应中MnO4-被还原为MnO
 。
。①KMnO4脱硫(SO2)的离子方程式为
②KMnO4/CaCO3浆液中KMnO4与CaCO3最合适的物质的量之比为
(3)利用NaClO2/H2O2酸性复合吸收剂可同时对NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,n(H2O2)/n(NaClO2)、溶液pH对脱硫脱硝的影响如图所示:

图a和图b中可知脱硫脱硝最佳条件是
您最近一年使用:0次
解题方法
8 . 酸性或碱性溶液中铝均可与NO 发生氧化还原反应,转化关系如图:
发生氧化还原反应,转化关系如图:
已知:气体D和A溶液反应生成白色沉淀,气体D和F反应可生成盐。

请回答下列问题:
(1)写出铝在碱性条件下与NO 反应的离子方程式
反应的离子方程式_________ 。
(2)在酸性条件下,被还原的NO 与Al的物质的量之比是
与Al的物质的量之比是_______ 。
(3)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C和E都转化为无毒的气态单质,请写出D和C反应的化学方程式:____________ 。
 发生氧化还原反应,转化关系如图:
发生氧化还原反应,转化关系如图:已知:气体D和A溶液反应生成白色沉淀,气体D和F反应可生成盐。

请回答下列问题:
(1)写出铝在碱性条件下与NO
 反应的离子方程式
反应的离子方程式(2)在酸性条件下,被还原的NO
 与Al的物质的量之比是
与Al的物质的量之比是(3)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C和E都转化为无毒的气态单质,请写出D和C反应的化学方程式:
您最近一年使用:0次
名校
解题方法
9 . 二氧化氯(ClO2)是世界卫生组织(WHO)公认的新时代绿色消毒剂,其特点是:无三致(致癌、致畸、致突变),有三效(广谱、高效、快速)。经大量实验研究表明,ClO2对细胞壁有较强的吸附和穿透能力,反应释放出的原子氧将细胞内的酶氧化,从而起到杀菌作用,研究表明,ClO2在浓度低于100mg·L−1时不会对人体产生任何的影响。在“新冠”疫情防控中ClO2也被广泛的用于公共场所的消杀。下列关于ClO2的说法正确的是
| A.ClO2能用于消毒是因为它是氯的最高价氧化物 |
| B.在进行消毒作业时使用的ClO2溶液浓度越大越好 |
| C.ClO2杀菌力强,是一种比“84”性能更优越的消毒剂 |
| D.ClO2可与NaOH在一条件下发生反应,产物只有NaClO3和H2O |
您最近一年使用:0次
2020-06-06更新
|
491次组卷
|
6卷引用:辽宁省铁岭市调兵山市第二高级中学2019~2020学年高一下学期期末考试化学试题
辽宁省铁岭市调兵山市第二高级中学2019~2020学年高一下学期期末考试化学试题湖北省黄冈市罗田县第一中学2019-2020学年高一下学期期中考试化学试题荆、荆、襄、宜四地七校考试联盟2019-2020学年高一下学期期中联考化学试题(已下线)1.3.4 氧化还原反应方程式的配平-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)(已下线)专题39 氯的氧化物、含氧酸及含氧酸盐-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)第12讲 富集在海水中的元素——卤素(讲)-2023年高考化学一轮复习讲练测(全国通用)
名校
解题方法
10 . 高锰酸钾是中学常用的试剂。工业上用软锰矿制备高锰酸钾流程。
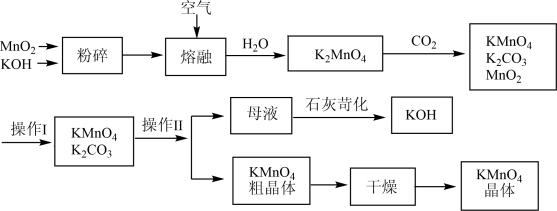
(1)上述流程中可以循环使用的物质有________ 、________ (写化学式)。
(2)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是________ (填代号)。
a.84消毒液(NaClO溶液) b.75%酒精c.苯酚
(3)理论上(若不考虑物质循环与制备过程中的损失)1molMnO2可制得________ molKMnO4。
(4)操作Ⅰ的名称是________ ;操作Ⅱ根据KMnO4和K2CO3两物质在________ (填性质)上的差异,采用________ (填操作步骤)、趁热过滤得到KMnO4粗晶体。

(1)上述流程中可以循环使用的物质有
(2)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是
a.84消毒液(NaClO溶液) b.75%酒精c.苯酚
(3)理论上(若不考虑物质循环与制备过程中的损失)1molMnO2可制得
(4)操作Ⅰ的名称是
您最近一年使用:0次
2020-04-27更新
|
441次组卷
|
2卷引用:辽宁省丹东市2017-2018学年高二下学期期末质量监测化学试题



