解题方法
1 . 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,已知K2FeO4在Fe3+催化下会分解,在强碱性条件下稳定。高铁酸钾(K2FeO4)生产流程如图:
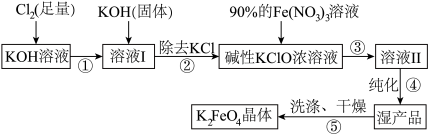
(1)在溶液Ⅰ中加入KOH固体的目的是 。
(2)写出③反应的离子方程式_______ 。
(3)制备K2FeO4时,将90%的Fe(NO3)3溶液缓缓滴加到碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是_______ 。
(4)K2FeO4在酸性或弱碱性条件下能与水反应生成一种胶体和一种氧化性气体单质,该气体单质为_______ (写出化学式)。
(5)K2FeO4净水时能吸附悬浮物的原因是_______ 。

(1)在溶液Ⅰ中加入KOH固体的目的是 。
| A.与溶液Ⅰ中过量的Cl2继续反应,生成更多的KClO |
| B.KOH固体溶解时会放出较多的热量,有利于提高KClO产率 |
| C.为下一步反应提供碱性的环境 |
| D.使KClO3转化为KClO |
(2)写出③反应的离子方程式
(3)制备K2FeO4时,将90%的Fe(NO3)3溶液缓缓滴加到碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是
(4)K2FeO4在酸性或弱碱性条件下能与水反应生成一种胶体和一种氧化性气体单质,该气体单质为
(5)K2FeO4净水时能吸附悬浮物的原因是
您最近一年使用:0次
名校
2 . 高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是一种新型多功能水处理剂。其生产工艺如图1所示:
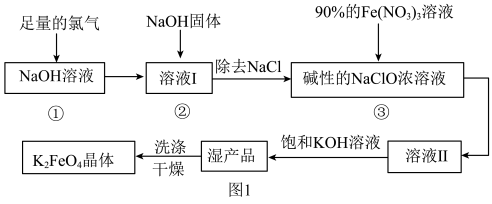
回答下列问题:
(1)Fe(NO3)3中 的空间结构名称为
的空间结构名称为_______ 氮原子的杂化轨道类型为_______
(2)反应①应在温度较低的情况下进行,因温度较高时NaOH与Cl2反应生成NaClO3,取某温度下反应液,测得ClO-与 的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被氧化的氯原子与被还原的氯原子的物质的量之比为
的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被氧化的氯原子与被还原的氯原子的物质的量之比为_______ 。
(3)反应③的离子方程式为_______ ,制备时,两溶液混合的操作为_______ 。
(4)往溶液II中加入饱和KOH溶液得到湿产品的原因是_______ 。该工艺流程中可循环使用的物质是_______ (填化学式)。
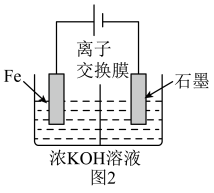
(5)高铁酸钾还可以通过电解法制备,其原理如图2所示:阳极的电极反应式为_______ 。

回答下列问题:
(1)Fe(NO3)3中
 的空间结构名称为
的空间结构名称为(2)反应①应在温度较低的情况下进行,因温度较高时NaOH与Cl2反应生成NaClO3,取某温度下反应液,测得ClO-与
 的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被氧化的氯原子与被还原的氯原子的物质的量之比为
的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被氧化的氯原子与被还原的氯原子的物质的量之比为(3)反应③的离子方程式为
(4)往溶液II中加入饱和KOH溶液得到湿产品的原因是
(5)高铁酸钾还可以通过电解法制备,其原理如图2所示:阳极的电极反应式为

您最近一年使用:0次
2023-01-18更新
|
269次组卷
|
3卷引用:辽宁省辽河油田第二高级中学2022-2023学年高三上学期期末考试化学试题
辽宁省辽河油田第二高级中学2022-2023学年高三上学期期末考试化学试题(已下线)北京市海淀区2022届高三一模(工业流程题)湖南省常德市汉寿县第一中学2023-2024学年高三上学期10月月考化学试题
名校
解题方法
3 . 碱式碳酸锰[Mn2(OH)2CO3]是一种不溶于水的固体,是制造其他含锰化合物的原料。工业上以方锰矿(主要成分为MnO,还含有少量的Fe3O4、Al2O3、CaO、SiO2)为原料制备碱式碳酸锰。
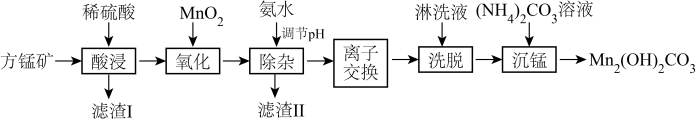
25℃时,相关物质的Ksp如表:
回答下列问题:
(1)“酸浸”时,滤渣I的成分是_____ (填化学式)。
(2)“氧化”时,该反应的离子方程式为_____ 。
(3)“除杂”时,使用氨水的目的是将Fe3+和Al3+转化为沉淀而除去,则应调节溶液的pH≥_____ ;若Al3+沉淀完全时,则溶液中Fe3+的物质的量浓度为_____ mol•L-1通常认为溶液中的离子浓度≤1×10-5mol•L-1沉淀完全)。
(4)“离子交换”和“洗脱”时,发生反应:Mn2++2HR MnR2+2H+(HR是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为
MnR2+2H+(HR是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为_____ (填“硫酸”、“氢氧化钠溶液”或“蒸馏水)。
(5)沉锰时,反应的离子方程式为_____ ,过滤、洗涤、干燥,得到Mn2(OH)2CO3,检验沉淀是否洗涤干净的操作是_____ 。

25℃时,相关物质的Ksp如表:
| 物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 |
| Ksp | 2×10-13 | 5×10-17 | 3×10-39 | 1×10-32 | 6×10-6 |
(1)“酸浸”时,滤渣I的成分是
(2)“氧化”时,该反应的离子方程式为
(3)“除杂”时,使用氨水的目的是将Fe3+和Al3+转化为沉淀而除去,则应调节溶液的pH≥
(4)“离子交换”和“洗脱”时,发生反应:Mn2++2HR
 MnR2+2H+(HR是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为
MnR2+2H+(HR是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为(5)沉锰时,反应的离子方程式为
您最近一年使用:0次
名校
解题方法
4 . 下列化学反应表示正确的是
| A.向碘化钾中通入过量氯气:2I- + Cl2 = 2Cl- + I2 |
| B.向稀硝酸中加入过量铁粉:3Fe + 8HNO3=3Fe(NO3)2 + 2NO↑ +4H2O |
| C.氯化亚铁溶液中加入少量过氧化钠:4Fe2+ + 4Na2O2 + 6H2O =4Fe(OH)3↓ + 8Na+ + O2↑ |
D.硫酸铵溶液和氢氧化钡溶液反应:NH + SO + SO + Ba2+ + OH−= BaSO4↓+NH3·H2O + Ba2+ + OH−= BaSO4↓+NH3·H2O |
您最近一年使用:0次
名校
解题方法
5 . 超细银粉在光学、生物医疗等领域有着广阔的应用前景。由含银废催化剂制备超细银粉的过程如下:
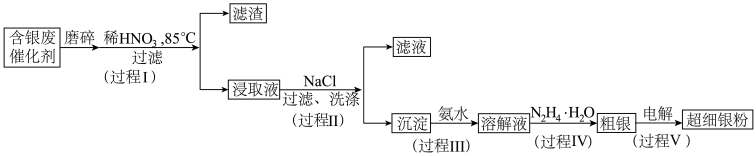
资料:
i.含银废催化剂成分:主要含Ag、 及少量MgO、
及少量MgO、 、
、 、
、 等
等
ii. 为载体,且不溶于硝酸
为载体,且不溶于硝酸
iii.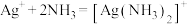
(1)预处理
过程I中,为提高银的浸取速率采取的措施有_______
(2)分离除杂
①过程Ⅱ中,检验沉淀表面的 已洗涤干净的操作是
已洗涤干净的操作是_______ 。
②过程Ⅲ中,请结合平衡移动原理解释沉淀溶解的原因_______ 。
③过程Ⅳ中, 被氧化为
被氧化为 ,同时获得粗银,该反应的离子方程式为
,同时获得粗银,该反应的离子方程式为_______ 。
(3)回收率测定
采用如下方法测定粗银中银的回收率:取m g粗银样品用硝酸溶解,以铁铵矾[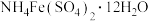 ]为指示剂,用c mol/L的KSCN标准溶液滴定,消耗标准溶液v mL。
]为指示剂,用c mol/L的KSCN标准溶液滴定,消耗标准溶液v mL。
已知:i. (白色)
(白色) 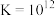
 (红色)
(红色) 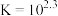
ii. 开始沉淀的pH为1.5,完全沉淀的pH为2.8
开始沉淀的pH为1.5,完全沉淀的pH为2.8
iii.AgSCN可溶于较浓硝酸判断已达滴定终点时的现象是_______ 。
(4)精炼
①精炼时粗银应连接电源_______ 极;
②电解质溶液中溶质为_______ 。

资料:
i.含银废催化剂成分:主要含Ag、
 及少量MgO、
及少量MgO、 、
、 、
、 等
等ii.
 为载体,且不溶于硝酸
为载体,且不溶于硝酸iii.
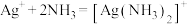
(1)预处理
过程I中,为提高银的浸取速率采取的措施有
(2)分离除杂
①过程Ⅱ中,检验沉淀表面的
 已洗涤干净的操作是
已洗涤干净的操作是②过程Ⅲ中,请结合平衡移动原理解释沉淀溶解的原因
③过程Ⅳ中,
 被氧化为
被氧化为 ,同时获得粗银,该反应的离子方程式为
,同时获得粗银,该反应的离子方程式为(3)回收率测定
采用如下方法测定粗银中银的回收率:取m g粗银样品用硝酸溶解,以铁铵矾[
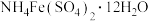 ]为指示剂,用c mol/L的KSCN标准溶液滴定,消耗标准溶液v mL。
]为指示剂,用c mol/L的KSCN标准溶液滴定,消耗标准溶液v mL。已知:i.
 (白色)
(白色) 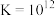
 (红色)
(红色) 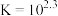
ii.
 开始沉淀的pH为1.5,完全沉淀的pH为2.8
开始沉淀的pH为1.5,完全沉淀的pH为2.8iii.AgSCN可溶于较浓硝酸判断已达滴定终点时的现象是
(4)精炼
①精炼时粗银应连接电源
②电解质溶液中溶质为
您最近一年使用:0次
2023-01-05更新
|
295次组卷
|
2卷引用:辽宁省沈阳市东北育才学校2022-2023学年高二上学期期末测试化学试题
名校
解题方法
6 . 某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体[ ]和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
]和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
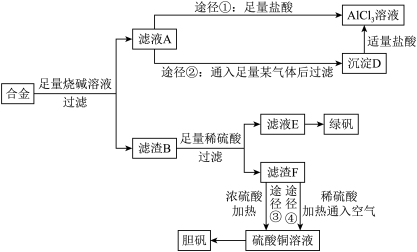
回答下列问题:
(1)写出合金与烧碱溶液反应的离子方程式_______ 。
(2)进行途径②时,该小组用下图所示装置及试剂,将制得的 气体通入滤液A中。一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是
气体通入滤液A中。一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是_______ (用离子方程式表示);为了避免沉淀D减少,应该在装置Ⅰ和装置Ⅱ之间增加一个盛有_______ 的洗气瓶。
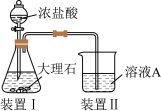
(3)通过途径④制取胆矾,必须进行的实验操作步骤:加硫酸、加热通氧气、过滤、蒸发浓缩、冷却结晶、过滤、自然干燥。其中“加热通氧气”所起的作用为_______ (用离子方程式表示)。
(4)白磷有剧毒,不慎沾到皮肤上,可取少量胆矾配制成 溶液冲洗解毒。白磷可与热的
溶液冲洗解毒。白磷可与热的 溶液反应生成
溶液反应生成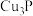 ,与冷溶液则析出Cu,反应方程式分别(均未配平)为:
,与冷溶液则析出Cu,反应方程式分别(均未配平)为:
①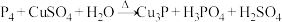
②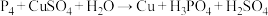
若上述两反应中被氧化的 的物质的量相等,则消耗的
的物质的量相等,则消耗的 的物质的量之比为
的物质的量之比为_______ 。
(5)将绿矾加热失去结晶水后的产物 ,进行如下转化(无关物质已略去)
,进行如下转化(无关物质已略去)
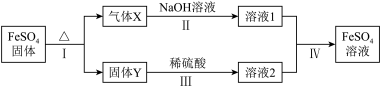
已知:X由两种化合物组成,将X通入氯水,溶液褪色;通入 溶液,产生白色沉淀。Y是红棕色的化合物。
溶液,产生白色沉淀。Y是红棕色的化合物。
①请写出X使氯水褪色所发生的反应的化学方程式_______ 。
②若经反应Ⅰ得到16g固体Y,产生的气体X恰好被0.4L1mol/L NaOH溶液完全吸收,则反应Ⅳ中生成 的离子方程式是
的离子方程式是_______ 。
 ]和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
]和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
回答下列问题:
(1)写出合金与烧碱溶液反应的离子方程式
(2)进行途径②时,该小组用下图所示装置及试剂,将制得的
 气体通入滤液A中。一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是
气体通入滤液A中。一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是
(3)通过途径④制取胆矾,必须进行的实验操作步骤:加硫酸、加热通氧气、过滤、蒸发浓缩、冷却结晶、过滤、自然干燥。其中“加热通氧气”所起的作用为
(4)白磷有剧毒,不慎沾到皮肤上,可取少量胆矾配制成
 溶液冲洗解毒。白磷可与热的
溶液冲洗解毒。白磷可与热的 溶液反应生成
溶液反应生成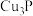 ,与冷溶液则析出Cu,反应方程式分别(均未配平)为:
,与冷溶液则析出Cu,反应方程式分别(均未配平)为:①
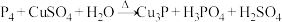
②
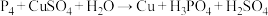
若上述两反应中被氧化的
 的物质的量相等,则消耗的
的物质的量相等,则消耗的 的物质的量之比为
的物质的量之比为(5)将绿矾加热失去结晶水后的产物
 ,进行如下转化(无关物质已略去)
,进行如下转化(无关物质已略去)
已知:X由两种化合物组成,将X通入氯水,溶液褪色;通入
 溶液,产生白色沉淀。Y是红棕色的化合物。
溶液,产生白色沉淀。Y是红棕色的化合物。①请写出X使氯水褪色所发生的反应的化学方程式
②若经反应Ⅰ得到16g固体Y,产生的气体X恰好被0.4L1mol/L NaOH溶液完全吸收,则反应Ⅳ中生成
 的离子方程式是
的离子方程式是
您最近一年使用:0次
名校
解题方法
7 . 某溶液仅含 、
、 、
、 、
、 、
、 、
、 、
、 中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变。下列说法错误的是
中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变。下列说法错误的是
 、
、 、
、 、
、 、
、 、
、 、
、 中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变。下列说法错误的是
中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变。下列说法错误的是| A.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 |
B.加入稀硫酸发生反应的离子方程式为: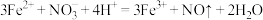 |
C.该溶液中一定有 |
| D.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g |
您最近一年使用:0次
解题方法
8 . 羟基氧化铁 是一种重要的化工原料,一种以工厂废料(含
是一种重要的化工原料,一种以工厂废料(含 、
、 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如下:
的工艺流程如下:
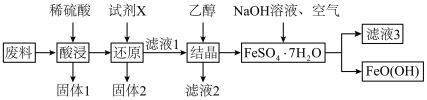
已知: 为酸性氧化物,不与硫酸等强酸反应;
为酸性氧化物,不与硫酸等强酸反应; 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。
(1)羟基氧化铁中铁元素的化合价是_______ ,“固体1”的主要成分是_______ 。
(2)“酸浸”时 与硫酸发生反应的离子方程式为
与硫酸发生反应的离子方程式为_______ 。“试剂X”宜选择的是_______ 。
A.双氧水 B.铁粉 C.铜粉 D.钠块
(3)“结晶”时加入乙醇即可析出 晶体,乙醇的作用是
晶体,乙醇的作用是_______ 。
(4)将 配制成一定浓度的溶液,恒温条件下边搅拌边按一定比例加入
配制成一定浓度的溶液,恒温条件下边搅拌边按一定比例加入 溶液,同时鼓入空气进行氧化,至反应液全部变为棕黄色悬浊液,即可得到
溶液,同时鼓入空气进行氧化,至反应液全部变为棕黄色悬浊液,即可得到 。该反应的离子方程式为
。该反应的离子方程式为_______ 。
(5)“滤液3”中,溶质的主要成分是_______ (写化学式)。
 是一种重要的化工原料,一种以工厂废料(含
是一种重要的化工原料,一种以工厂废料(含 、
、 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如下:
的工艺流程如下:
已知:
 为酸性氧化物,不与硫酸等强酸反应;
为酸性氧化物,不与硫酸等强酸反应; 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。(1)羟基氧化铁中铁元素的化合价是
(2)“酸浸”时
 与硫酸发生反应的离子方程式为
与硫酸发生反应的离子方程式为A.双氧水 B.铁粉 C.铜粉 D.钠块
(3)“结晶”时加入乙醇即可析出
 晶体,乙醇的作用是
晶体,乙醇的作用是(4)将
 配制成一定浓度的溶液,恒温条件下边搅拌边按一定比例加入
配制成一定浓度的溶液,恒温条件下边搅拌边按一定比例加入 溶液,同时鼓入空气进行氧化,至反应液全部变为棕黄色悬浊液,即可得到
溶液,同时鼓入空气进行氧化,至反应液全部变为棕黄色悬浊液,即可得到 。该反应的离子方程式为
。该反应的离子方程式为(5)“滤液3”中,溶质的主要成分是
您最近一年使用:0次
名校
解题方法
9 . 正高碘酸(H5IO6)是白色结晶性粉末,溶于水,主要用作氧化剂和分析试剂。由NaI制取H5IO6的实验流程如图所示:
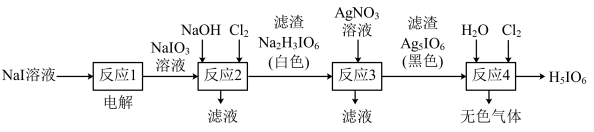
下列说法正确的是

下列说法正确的是
A.电解过程中阳极反应为:I-+6OH--6e-=IO +3H2O +3H2O |
| B.“反应2”中Cl2与NaIO3的物质的量之比为1∶1 |
| C.“反应3”的滤液中含有NaNO3,NaI等 |
| D.“反应4”为非氧化还原反应 |
您最近一年使用:0次
2022-12-17更新
|
189次组卷
|
3卷引用:辽宁省锦州市渤大附中2022-2023学年高三上学期期末考试化学试题
名校
解题方法
10 . 能正确表示下列反应的离子方程式的是
| A.向CuSO4溶液中加入金属钠:2Na+Cu2+=2Na++Cu |
B.向高锰酸钾溶液中滴加双氧水:2Mn +3H2O2+6H+=2Mn2++4O2↑+6H2O +3H2O2+6H+=2Mn2++4O2↑+6H2O |
C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使S 完全沉淀:N 完全沉淀:N +Al3++2S +Al3++2S +2Ba2++4OH-=Al(OH)3↓+NH3·H2O+2BaSO4↓ +2Ba2++4OH-=Al(OH)3↓+NH3·H2O+2BaSO4↓ |
| D.氢氧化铁与氢碘酸反应:Fe(OH)3+3H+=Fe3++3H2O |
您最近一年使用:0次
2022-12-13更新
|
171次组卷
|
3卷引用:辽宁省锦州市渤大附中2022-2023学年高三上学期期末考试化学试题



