名校
解题方法
1 . 在酸性条件下,黄铁矿 催化氧化的反应方程式为
催化氧化的反应方程式为 ,实现该反应的物质间转化如图所示。下列分析错误的是
,实现该反应的物质间转化如图所示。下列分析错误的是

 催化氧化的反应方程式为
催化氧化的反应方程式为 ,实现该反应的物质间转化如图所示。下列分析错误的是
,实现该反应的物质间转化如图所示。下列分析错误的是
A.反应Ⅰ的离子方程式为 |
B.反应Ⅱ的氧化剂是 |
| C.反应Ⅲ是氧化还原反应 |
D.黄铁矿催化氧化中 作催化剂 作催化剂 |
您最近一年使用:0次
名校
2 . 无水三氯化铬(CrCl3)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。通常是用不含水的三氧化二铬与卤化剂(如CCl4)在高温下反应,并使生成的三氯化铬在惰性气氛(如氮气)中升华来制取: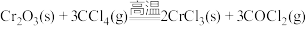 ,生成的COCl2(俗称光气)有毒,遇水发生水解,生成两种酸性气体,实验装置如图所示(夹持装置略)。
,生成的COCl2(俗称光气)有毒,遇水发生水解,生成两种酸性气体,实验装置如图所示(夹持装置略)。
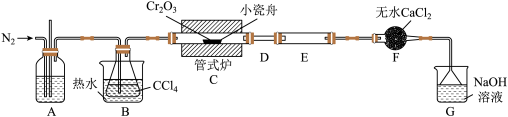
(1)A中的试剂为___________ ,长玻璃管的作用是___________ 。
(2)连接好装置后,先___________ ,再装入药品。在进行实验时,先___________ (填“通入N2”或“加热管式炉”);实验结束后,再持续通一段时间的N2,目的是___________ 。
(3)实验过程中若D处出现堵塞,应该采取的措施是___________ ,F中无水CaCl2的作用是___________ 。
(4)G装置的作用是___________ ,发生反应的离子方程式为___________ 。
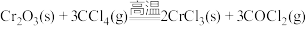 ,生成的COCl2(俗称光气)有毒,遇水发生水解,生成两种酸性气体,实验装置如图所示(夹持装置略)。
,生成的COCl2(俗称光气)有毒,遇水发生水解,生成两种酸性气体,实验装置如图所示(夹持装置略)。
(1)A中的试剂为
(2)连接好装置后,先
(3)实验过程中若D处出现堵塞,应该采取的措施是
(4)G装置的作用是
您最近一年使用:0次
2023-09-23更新
|
251次组卷
|
7卷引用:甘肃省张掖市高台县第一中学2023-2024学年高三上学期9月月考化学试题
名校
3 . 工业上以软锰矿(含MnO2和少量的Fe2O3、Al2O3、SiO2)为原料制备硫酸锰晶体的流程如图所示,下列有关说法不正确的是


A.酸浸过程发生的主要反应的离子方程式为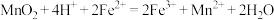 |
B.试剂A的目的是将过量 氧化为 氧化为 |
| C.试剂B可以是MnO或MnCO3 |
| D.滤渣1为H2SiO3,滤渣2为Fe(OH)3、Al(OH)3 |
您最近一年使用:0次
2023-09-23更新
|
461次组卷
|
8卷引用:甘肃省张掖市高台县第一中学2023-2024学年高三上学期9月月考化学试题
4 . 在离子方程式xR2++yH++O2=mR3++nH2O中,对系数m和R3+的判断正确的是
| A.m=4;R2+是氧化剂 |
| B.m=y;R3+是氧化产物 |
| C.m=2;R2+是氧化剂 |
| D.m=y;R3+是还原产物 |
您最近一年使用:0次
2023-08-25更新
|
314次组卷
|
2卷引用:甘肃省武威市凉州区部分校2023-2024学年高三上学期第二次模拟考试化学试题
名校
解题方法
5 . 实验室利用废弃旧电池的铜帽(主要成分为锌铜合金)回收Cu并制备ZnCl2的部分实验过程如图所示。下列说法不正确的是
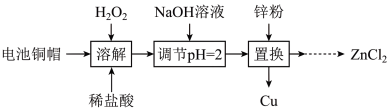

| A.“溶解”时Cu发生反应的离子方程式为Cu+H2O2+2H+=Cu2++2H2O, |
| B.因为升高温度可以加快反应速率,所以“溶解”时适宜采用高温 |
| C.“调节pH=2”后,溶液中大量存在的离子有Cu2+、Zn2+、H+、Cl-、Na+ |
| D.将ZnCl2溶液在HCl的气氛中加热蒸干即可获得无水ZnCl2 |
您最近一年使用:0次
2023-08-20更新
|
318次组卷
|
2卷引用:甘肃省民乐县第一中学2023-2024学年高三上学期第一次诊断考试化学试题
6 . 某化学兴趣小组通过查阅文献,设计了从阳极泥(成分为Cu2S、Ag2Se、Au、Pt)中回收贵重金属的工艺,其流程如图所示。已知:“酸溶”时Pt、Au分别转化为[PtCl6]2-和 [AuCl4]-,下列判断错误的是
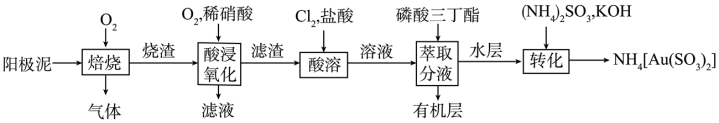

| A.“焙烧”时,Cu2S转化为CuO的反应中氧化剂与还原剂物质的量之比为1∶2 |
| B.“酸浸氧化”时,O2的作用之一是防止NO排放到空气中污染环境 |
| C.“酸溶”时,金溶解的离子方程式为2Au+3Cl2+2Cl-=2[AuCl4]- |
| D.有机层中回收的金属元素是Pt,萃取分液用到的玻璃仪器是分液漏斗和烧杯 |
您最近一年使用:0次
解题方法
7 . 天然气中含有有毒气体 ,用下图所示流程可实现天然气在“
,用下图所示流程可实现天然气在“ 菌”作用下的脱硫反应。下列说法正确的是
菌”作用下的脱硫反应。下列说法正确的是

 ,用下图所示流程可实现天然气在“
,用下图所示流程可实现天然气在“ 菌”作用下的脱硫反应。下列说法正确的是
菌”作用下的脱硫反应。下列说法正确的是
| A.过程①中硫元素被还原 |
B.过程②中氧化剂和还原剂的物质的量之比为 |
C.该脱硫过程中, 和 和 中的硫元素也参与脱硫反应 中的硫元素也参与脱硫反应 |
D.该脱硫过程的总反应为 |
您最近一年使用:0次
解题方法
8 . 空气吹出法是用于天然海水提溴的最成熟工业方法。海水中溴离子在酸化后,用氯气氧化成溴分子。游离溴被空气吹出,再用吸收剂吸收含溴空气中的溴。流程如下:
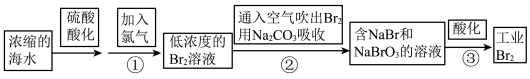
已知溴酸为强酸,下列说法不正确的是

已知溴酸为强酸,下列说法不正确的是
| A.步骤①发生的主要反应为:Cl2+2Br-=Br2+2Cl- |
| B.步骤②的吸收剂也可以是二氧化硫水溶液 |
| C.获得工业液溴(Br2)的方法是过滤 |
| D.步骤②发生的主要反应方程式为:3Br2+3Na2CO3=5NaBr+3CO2+NaBrO3 |
您最近一年使用:0次
2023-07-12更新
|
63次组卷
|
2卷引用:甘肃省兰州市等5地2022-2023学年高一下学期期末化学试题
名校
解题方法
9 . 工业上利用废铁屑(含少量Fe2O3、Al2O3)生产碱式硫酸铁的工艺流程如图:
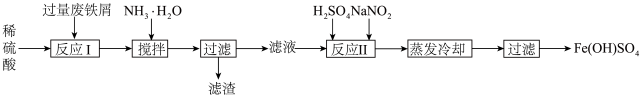
下列说法正确的是

下列说法正确的是
| A.该工艺流程符合绿色化学的理念 |
B.滤液中所含的阳离子主要为 、 、 、 、 |
| C.反应II加入H2SO4只是用于调节溶液酸碱性 |
D.蒸发过程中可以升高温度,在加快反应速率的同时还能让 充分水解 充分水解 |
您最近一年使用:0次
名校
解题方法
10 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。根据所学知识,回答下列问题:
(1)实验室加热亚硝酸铵(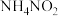 )的浓溶液可制得氮气,同时可得到一种无色无味的液体,则反应的化学方程式为
)的浓溶液可制得氮气,同时可得到一种无色无味的液体,则反应的化学方程式为________ ,被氧化的氮原子与被还原的氮原子的物质的量之比为________ 。
(2)氨气还原氧化铜也可制得氮气,实验装置如图。
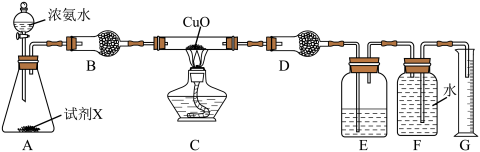
①试剂X为________ 。
②装置B的作用为________ 。
③氨气易溶于水,氨水呈碱性,其原因是________ (用离子方程式表示)。
④若在试管中进行氨气与红热的氧化铜反应的实验,可观察到的实验现象为________ ,反应的化学方程式为________ 。
(1)实验室加热亚硝酸铵(
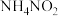 )的浓溶液可制得氮气,同时可得到一种无色无味的液体,则反应的化学方程式为
)的浓溶液可制得氮气,同时可得到一种无色无味的液体,则反应的化学方程式为(2)氨气还原氧化铜也可制得氮气,实验装置如图。

①试剂X为
②装置B的作用为
③氨气易溶于水,氨水呈碱性,其原因是
④若在试管中进行氨气与红热的氧化铜反应的实验,可观察到的实验现象为
您最近一年使用:0次



