名校
1 . 铜及其化合物有着广泛的应用。某实验小组探究 的性质。
的性质。
I.实验准备:
(1)由 固体配制
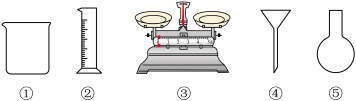
固体配制 溶液,下列仪器中需要使用的有
溶液,下列仪器中需要使用的有_________ (填序号)。
实验任务:探究 溶液分别与
溶液分别与 、
、 溶液的反应
溶液的反应
查阅资料:
已知:a.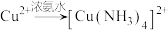 (深蓝色溶液)
(深蓝色溶液)
b. (无色溶液)
(无色溶液) (深蓝色溶液)
(深蓝色溶液)
设计方案并完成实验:
现象分析与验证:
(2)推测实验B产生的无色气体为 ,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到
,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到__________ 。
(3)推测实验B中的白色沉淀为 ,实验验证步骤如下:
,实验验证步骤如下:
①实验B完成后,立即过滤、洗涤。
②取少量已洗净的白色沉淀于试管中,滴加足量________ ,观察到沉淀溶解,得到无色溶液,此反应的离子方程式为__________ ;露置在空气中一段时间,观察到溶液变为深蓝色。
(4)对比实验A、B,提出假设: 增强了
增强了 的氧化性。
的氧化性。
①若假设合理,实验B反应的离子方程式为
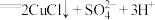 和
和__________ 。
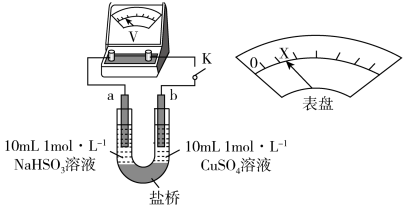
②下述实验C证实了假设合理,装置如图8(两个电极均为碳棒)。实验方案:闭合K,电压表的指针偏转至“X”处;向U形__________ (补全实验操作及现象)。
Ⅱ. 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。
(5)硫酸铜溶液呈蓝色的原因是溶液中存在配离子_________ (填化学式)。
(6)常见配合物的形成实验
 的性质。
的性质。I.实验准备:
(1)由
 固体配制
固体配制 溶液,下列仪器中需要使用的有
溶液,下列仪器中需要使用的有
实验任务:探究
 溶液分别与
溶液分别与 、
、 溶液的反应
溶液的反应查阅资料:
已知:a.
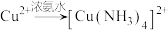 (深蓝色溶液)
(深蓝色溶液)b.
 (无色溶液)
(无色溶液) (深蓝色溶液)
(深蓝色溶液)设计方案并完成实验:
实验 | 装置 | 试剂x | 操作及现象 |
A |
| 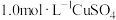 溶液 溶液 | 加入  溶液,得到绿色溶液, 溶液,得到绿色溶液, 未见明显变化。 未见明显变化。 |
B | 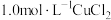 溶液 溶液 | 加入  溶液,得到绿色溶液, 溶液,得到绿色溶液, 时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 |
(2)推测实验B产生的无色气体为
 ,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到
,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到(3)推测实验B中的白色沉淀为
 ,实验验证步骤如下:
,实验验证步骤如下:①实验B完成后,立即过滤、洗涤。
②取少量已洗净的白色沉淀于试管中,滴加足量
(4)对比实验A、B,提出假设:
 增强了
增强了 的氧化性。
的氧化性。①若假设合理,实验B反应的离子方程式为

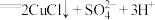 和
和②下述实验C证实了假设合理,装置如图8(两个电极均为碳棒)。实验方案:闭合K,电压表的指针偏转至“X”处;向U形

Ⅱ.
 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。(5)硫酸铜溶液呈蓝色的原因是溶液中存在配离子
(6)常见配合物的形成实验
实验操作 | 实验现象 | 有关离子方程式 |
| 滴加氨水后,试管中首先出现蓝色沉淀,氨水过量后沉淀逐渐 |  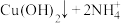   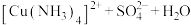 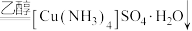 |
您最近一年使用:0次
2023-05-16更新
|
853次组卷
|
2卷引用:广东省梅州市2023届高三下学期第二次质检测试化学试题
解题方法
2 . 化学使生活更美好。下列物质使用时涉及的原理不正确的是
| 选项 | 物质用途 | 性质 |
| A | 聚乳酸用于手术缝合线 | 聚乳酸具有生物相容性和可吸收性 |
| B | 中秋节月饼包装袋中放入小袋铁粉 | 铁粉具有还原性 |
| C | 75%酒精溶液用于消毒 |  具有强氧化性 具有强氧化性 |
| D | 化妆品中添加甘油 | 丙三醇具有较强的吸水性能 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . H2O2在纸张漂白和废水处理等领域具有重要应用。一定条件下用H2和O2合成H2O2的反应过程示意图如图。下列说法错误的是


| A.O2在催化剂表面得到电子 |
| B.消耗H2和O2物质的量相等 |
| C.H2O2既有氧化性又有还原性 |
| D.H2O2与SO2的漂白原理相同 |
您最近一年使用:0次
名校
4 .  常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。
常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。 和
和 (亚氯酸钠)均具有漂白性,工业上由
(亚氯酸钠)均具有漂白性,工业上由 气体制取
气体制取 固体的工艺流程如图所示:
固体的工艺流程如图所示:

请回答下列问题:
(1)①吸收器中生成 的离子方程式为(补充完整):
的离子方程式为(补充完整):_______ 。
_______ +_______
+_______ +_______=
+_______= _______↑+_______
_______↑+_______
②此氧化还原反应中,双氧水表现_______ 性;若2mol 完全反应,
完全反应,_______ (填“得到”或“失去”)的电子数为_______ 个,生成的气体产物的体积为_______ (标况下)。
(2)为了探究 和
和 的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有:
的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有: 溶液、KI溶液、淀粉溶液、
溶液、KI溶液、淀粉溶液、 酸性溶液
酸性溶液
(3)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力(氧化能力相同,即有效氯生成氯离子时,转移电子数目相同)。
的氧化能力(氧化能力相同,即有效氯生成氯离子时,转移电子数目相同)。 的有效氯含量为
的有效氯含量为_______ (计算结果保留两位小数)。
 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。
常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。 和
和 (亚氯酸钠)均具有漂白性,工业上由
(亚氯酸钠)均具有漂白性,工业上由 气体制取
气体制取 固体的工艺流程如图所示:
固体的工艺流程如图所示:
请回答下列问题:
(1)①吸收器中生成
 的离子方程式为(补充完整):
的离子方程式为(补充完整):_______
 +_______
+_______ +_______=
+_______= _______↑+_______
_______↑+_______②此氧化还原反应中,双氧水表现
 完全反应,
完全反应,(2)为了探究
 和
和 的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有:
的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有: 溶液、KI溶液、淀粉溶液、
溶液、KI溶液、淀粉溶液、 酸性溶液
酸性溶液| 序号 | 实验操作 | 实验现象 | 实验结论 |
| ① | 将 通入足量KI溶液中,加入稀硫酸,再加入几滴淀粉溶液 通入足量KI溶液中,加入稀硫酸,再加入几滴淀粉溶液 | ||
| ② |  溶液 溶液 |  具有还原性 具有还原性 |
 的氧化能力(氧化能力相同,即有效氯生成氯离子时,转移电子数目相同)。
的氧化能力(氧化能力相同,即有效氯生成氯离子时,转移电子数目相同)。 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
2022-11-13更新
|
280次组卷
|
3卷引用:广东省广州市第七中学2022-2023学年高一上学期期中考试化学试题
名校
5 . 化学知识在生活中有广泛的应用,下列有关说法正确的是
| A.维生素C又名抗坏血酸,有较强的还原性,在食品中添加适量维生素C可以延长食品的保质期 |
| B.节日燃放的烟花所呈现的艳丽色彩,是利用了钠、镁、铝等金属元素的焰色反应 |
| C.碳酸钠溶液呈碱性能与盐酸反应,胃酸过多的病人可以在饮用水中加适量碳酸钠 |
D.使用氯气对自来水消毒时可能产生对人体有害的有机氯化物,因此使用 、 、 的同素异形体 的同素异形体 、 、 做为新的自来水消毒剂 做为新的自来水消毒剂 |
您最近一年使用:0次
2022-10-06更新
|
351次组卷
|
3卷引用:广东省广州市第六中学2022-2023学年高一上学期 (线上)期中考试化学试题
名校
6 . 研究有机物的结构和性质对生产生活意义深远。
 .已知A-F六种有机化合物,根据要求回答问题。
.已知A-F六种有机化合物,根据要求回答问题。___________ ,B物质的分子式为:___________ 。
(2)按官能团分类,D所属的类别是___________ 。
(3)1molE与足量的金属钠反应产生___________ L氢气(标况下)。
(4)实验室制取C的化学方程式___________ 。
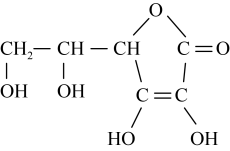
 .蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被
.蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被 等氧化剂氧化为脱氢维生素C.根据要求回答问题。
等氧化剂氧化为脱氢维生素C.根据要求回答问题。___________ (填名称)。
(6)脱氢维生素C中,键角①___________ 键角②(填“>”、“=”或“<”)。
(7)向碘和淀粉溶液中加入维生素C,可能观察到的现象是___________ 。
(8)标出维生素C中所有的手性碳原子(用*标注)___________ 。
 .已知A-F六种有机化合物,根据要求回答问题。
.已知A-F六种有机化合物,根据要求回答问题。A. 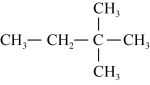 B.
B. 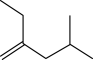 C.
C. D.
D. 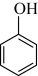 E.
E.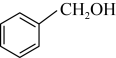
(2)按官能团分类,D所属的类别是
(3)1molE与足量的金属钠反应产生
(4)实验室制取C的化学方程式
 .蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被
.蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被 等氧化剂氧化为脱氢维生素C.根据要求回答问题。
等氧化剂氧化为脱氢维生素C.根据要求回答问题。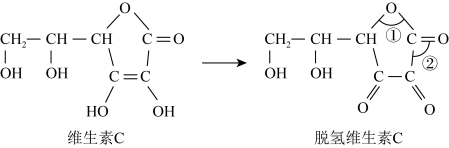
(6)脱氢维生素C中,键角①
(7)向碘和淀粉溶液中加入维生素C,可能观察到的现象是
(8)标出维生素C中所有的手性碳原子(用*标注)
您最近一年使用:0次
7 . 目前,汽车尾气系统中均安装了催化转化器,这种方法是处理 的“储存还原技术法”,简称
的“储存还原技术法”,简称 ,工作原理如图所示。下列说法中正确的是
,工作原理如图所示。下列说法中正确的是
 的“储存还原技术法”,简称
的“储存还原技术法”,简称 ,工作原理如图所示。下列说法中正确的是
,工作原理如图所示。下列说法中正确的是
A.在富氧氛围下喷入少量燃油可以生成 、 、 等还原性尾气 等还原性尾气 |
B. 系统中的只有一种催化剂 系统中的只有一种催化剂 |
C.存储阶段,氮元素被氧化,以 的形式被存储起来 的形式被存储起来 |
D.还原阶段,每生成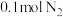 ,转移 ,转移 电子 电子 |
您最近一年使用:0次
2022-12-09更新
|
1064次组卷
|
5卷引用:广东省六校2023届高三第三次联考化学试题
广东省六校2023届高三第三次联考化学试题广东省六校联盟2022-2023学年高三上学期第三次联考化学试题广东省广州市第二中学等五校2022-2023学年高三上学期12月月考化学试题(已下线)2022年天津市普通高中学业水平等级性考试化学试题变式题(选择题5-8)安徽省马鞍山市第二中学2023-2024学年高二上学期12月阶段检测化学试题
8 . 下列关于化学品的使用错误的是( )
| A.阿司匹林是一种解热镇痛药,但长期大量服用会有一定毒副作用 |
| B.维生素C具有一定的还原性,常用作水果罐头中的抗氧化剂 |
| C.烘焙糕点所用的发酵粉主要成分之一是碳酸氢钠 |
| D.将硝酸铵和熟石灰混合使用,既能给农作物提供营养元素,又能降低土壤酸性 |
您最近一年使用:0次
解题方法
9 . 劳动创造美,下列有关劳动项目中的化学知识解读错误的是
| 选项 | 劳动项目 | 解读 |
| A | 用碳酸钠溶液洗涤餐具上的油污 | 碳酸钠易溶于水 |
| B | 用天然气烧开水 | 天然气燃烧时放出热量 |
| C | 用臭氧消毒柜给餐具消毒 | 臭氧具有强氧化性 |
| D | 将废弃电池送到专门回收点 | 废旧电池处理不当会污染环境 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . ClO2是一种新型消毒剂,以下反应均能制得ClO2。
Ⅰ.2NaCl+6H2O 2ClO2↑+5H2↑+2NaOH
2ClO2↑+5H2↑+2NaOH
Ⅱ.5NaClO3+6HCl=6ClO2↑+3H2O+5NaCl
Ⅲ.Cl2+2NaClO2=2ClO2↑+2NaCl
(1)请表示反应Ⅰ中电子转移的方向和数目___________ 。
(2)由反应②可知,氧化性NaClO3____ ClO2;
(3)通过反应Ⅱ和Ⅲ分别制备标准状况下2.24LClO2,转移电子物质的量之比为___________ 。
(4)从氯元素利用率的角度分析,以上三种方法中,制备ClO2的最佳方法是___________ 。(填序号)
Ⅰ.2NaCl+6H2O
 2ClO2↑+5H2↑+2NaOH
2ClO2↑+5H2↑+2NaOHⅡ.5NaClO3+6HCl=6ClO2↑+3H2O+5NaCl
Ⅲ.Cl2+2NaClO2=2ClO2↑+2NaCl
(1)请表示反应Ⅰ中电子转移的方向和数目
(2)由反应②可知,氧化性NaClO3
(3)通过反应Ⅱ和Ⅲ分别制备标准状况下2.24LClO2,转移电子物质的量之比为
(4)从氯元素利用率的角度分析,以上三种方法中,制备ClO2的最佳方法是
您最近一年使用:0次



 溶液
溶液