解题方法
1 . 氧化还原反应在工农业生产,日常生活中具有广泛应用。
(1)下列成语中,涉及有氧化还原反应的是___________。
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有___________ (填“氧化性”或“还原性”)。
(3)高温下铝粉与氧化铁的反应可用来焊接钢轨。其原理是:反应放出大量的热,置换出的铁呈熔融态,熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。该反应的化学方程式为___________ ,其中,氧化剂是___________ (填化学式,下同),被氧化的物质是___________ 。
(4)油画所用颜料含有某种白色铅化合物,久置于空气中就会变成黑色PbS,从而使油画色彩变暗。若用H2O2来“清洗”,则可将PbS转变成白色的PbSO4,从而使油画的色彩“复原”。上述“清洗”反应的化学方程式为 ,请用单线桥法标出该反应中电子转移情况
,请用单线桥法标出该反应中电子转移情况___________ 。
(5)宋代著名法医学家宋慈的《洗冤集录》中有关于银针验毒的记载。“银针验毒”的原理是 。X为只含两种元素的黑色固体,它的化学式是
。X为只含两种元素的黑色固体,它的化学式是___________ ,该反应的氧化剂与还原剂的质量比为___________ 。
(1)下列成语中,涉及有氧化还原反应的是___________。
| A.沙里淘金 | B.蜡炬成灰 | C.木已成舟 | D.铁杵成针 |
(3)高温下铝粉与氧化铁的反应可用来焊接钢轨。其原理是:反应放出大量的热,置换出的铁呈熔融态,熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。该反应的化学方程式为
(4)油画所用颜料含有某种白色铅化合物,久置于空气中就会变成黑色PbS,从而使油画色彩变暗。若用H2O2来“清洗”,则可将PbS转变成白色的PbSO4,从而使油画的色彩“复原”。上述“清洗”反应的化学方程式为
 ,请用单线桥法标出该反应中电子转移情况
,请用单线桥法标出该反应中电子转移情况(5)宋代著名法医学家宋慈的《洗冤集录》中有关于银针验毒的记载。“银针验毒”的原理是
 。X为只含两种元素的黑色固体,它的化学式是
。X为只含两种元素的黑色固体,它的化学式是
您最近一年使用:0次
名校
解题方法
2 . 某化学兴趣小组设计一种从硫矿石(主要成分为硫黄及少量FeS2)中提取硫黄的方法如下:
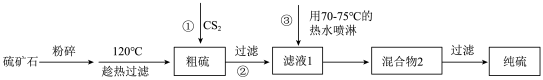
查阅资料:S的熔点为115.2℃; 的沸点为46.2℃。
的沸点为46.2℃。
下列说法错误的是

查阅资料:S的熔点为115.2℃;
 的沸点为46.2℃。
的沸点为46.2℃。下列说法错误的是
| A.单质硫是分子晶体 |
B.过程①中 可用乙醇代替 可用乙醇代替 |
C.过程③的目的是使 挥发,同时使硫从水中析出 挥发,同时使硫从水中析出 |
D.将趁热过滤所得滤渣煅烧: ,反应中每生成1 mol ,反应中每生成1 mol  ,转移电子的物质的量为5.5 mol ,转移电子的物质的量为5.5 mol |
您最近一年使用:0次
2023-03-08更新
|
478次组卷
|
3卷引用:河南省焦作市博爱县第一中学2022-2023学年高三下学期5月月考化学试题
3 . 某学习小组拟研究FeSO4的分解实验探究,请你利用所学知识帮该小组完成以下实验方案。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2 ;
假设2:FeO、SO3、SO2;
假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
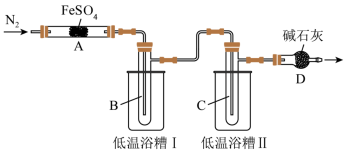
回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是_______ 。
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是_______ ,(只填操作),当A处固体完全分解后通入N2的目的是_______ 。
(3)实验室用饱和氯化铵溶液和亚硝酸钠溶液共热制备N2,该反应的离子方程式为_______ 。
(4)低温浴槽Ⅰ收集的物质是_______ (填化学式),低温浴槽Ⅱ控制的温度范围为_______ 。
(5)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
甲组实验中A装置得到固体产物是_______ (填化学式)。
(6)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是_______ 。
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(7)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案_______ (填“1”或“2”)可行。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2 ;
假设2:FeO、SO3、SO2;
假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
| 物质 | SO3 | SO2 | O2 | N2 |
| 熔点/℃ | 16.8 | - 72.4 | -218.4 | -209.9 |
| 沸点/℃ | 44.8 | - 10 | -182.9 | - 195.8 |

回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是
(3)实验室用饱和氯化铵溶液和亚硝酸钠溶液共热制备N2,该反应的离子方程式为
(4)低温浴槽Ⅰ收集的物质是
(5)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
| 实验 | A处温度/℃ | FeSO4质量/g | 低温浴槽Ⅰ净增质量/g | 低温浴槽Ⅱ净增质量/g |
| 甲 | T1 | 3.04 | 0.80 | 0.64 |
| 乙 | T2 | 4.56 | 1.60 | 0.64 |
(6)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(7)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案
您最近一年使用:0次
解题方法
4 . 下列物质应用,可用对应性质解释的是
| 选项 | 应用 | 性质 |
| A | 氧化铝用于工业冶炼铝 | 熔点低 |
| B | 重铬酸钾用于检查酒驾 | 强氧化性 |
| C | 氢氟酸用于刻制玻璃仪器刻度线 | 强酸性 |
| D | 离子液体用于电池的离子导体 | 密度小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 铁元素是重要的过渡元素,在工农业生产和生活中占有重要的地位。
(1)铁的原子结构示意图为__________ ;工业上用磁铁矿与一氧化碳反应冶炼铁,反应所得氧化产物的电子式为__________ 。
(2)正常人体内铁元素以Fe2+和Fe3+的形式存在,Fe2+易被吸收,食用含有微量颗粒细小的还原铁粉的麦片可以防治贫血,原因是__________ (结合必要的离子方程式解释);服用维生素C(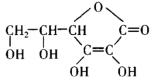 )可以将食物中的Fe3+还原成Fe2+,有利于人体吸收,维生素C中含氧官能团的名称为
)可以将食物中的Fe3+还原成Fe2+,有利于人体吸收,维生素C中含氧官能团的名称为____________________ 。
(3)向工业上用FeCl3溶液刻蚀铜质线路板所得废液中加入足量铁,被还原的元素一定有__________ (填元素符号),废液中加入足量酸性KMnO4溶液,氧化产物为__________ (写名称)。
(4)药用FeSO4可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用FeSO4配制成溶液,并取2 mL FeSO4溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向FeSO4溶液和Fe2(SO4)3溶液中分别通入NO2,观察到FeSO4溶液变为深棕色,Fe2(SO4)3溶液无明显变化。
①溶液变为深棕色的原因是__________ 。
②实验小组改进实验,观察到溶液变为黄色的实验操作是__________ 。
(1)铁的原子结构示意图为
(2)正常人体内铁元素以Fe2+和Fe3+的形式存在,Fe2+易被吸收,食用含有微量颗粒细小的还原铁粉的麦片可以防治贫血,原因是
 )可以将食物中的Fe3+还原成Fe2+,有利于人体吸收,维生素C中含氧官能团的名称为
)可以将食物中的Fe3+还原成Fe2+,有利于人体吸收,维生素C中含氧官能团的名称为(3)向工业上用FeCl3溶液刻蚀铜质线路板所得废液中加入足量铁,被还原的元素一定有
(4)药用FeSO4可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用FeSO4配制成溶液,并取2 mL FeSO4溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向FeSO4溶液和Fe2(SO4)3溶液中分别通入NO2,观察到FeSO4溶液变为深棕色,Fe2(SO4)3溶液无明显变化。
①溶液变为深棕色的原因是
②实验小组改进实验,观察到溶液变为黄色的实验操作是
您最近一年使用:0次
6 . 下列说法不正确 的是
| A.自嗨锅的发热包主要成分是生石灰,其与水反应放热从而使食材加热 |
| B.抗坏血酸(即维生素C)是水果罐头中常用的抗氧化剂,是因为其具有较强的氧化性 |
| C.在食品包装袋内放入铁系保鲜剂可以防止食品因氧化而变质 |
| D.臭氧是饮用水的理想消毒剂之一,因为它杀菌能力强且不影响水质 |
您最近一年使用:0次
2022-03-09更新
|
206次组卷
|
2卷引用:河南省中原名校2021-2022学年高二下学期第一次联考化学试题
7 . 下列加点物质的用途与其氧化性有关的是
| A.维生素C作为抗氧化剂,防止富脂食品氧化变质 |
B.葡萄糖与 溶液反应用于玻璃镀银 溶液反应用于玻璃镀银 |
| C.铁红与铝粉混合物在高温下反应用于焊接钢轨 |
| D.小苏打作为膨松剂,用于糕点制作 |
您最近一年使用:0次
8 . NaClO2·3H2O具有强氧化性,在消毒和果蔬保鲜等方面有广泛应用。一种制备NaClO2·3H2O的流程如图,下列有关说法错误的是


A.“合成”中发生反应的离子方程式为SO2+2ClO =SO =SO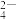 +2ClO2 +2ClO2 |
| B.生成ClO2时,NaClO3作氧化剂,被还原 |
| C.“转化”过程中,H2O2作氧化剂,参加反应的ClO2和H2O2的物质的量之比为2:1 |
| D.“一系列操作”为蒸发浓缩,冷却结晶,过滤洗涤 |
您最近一年使用:0次
2021-12-23更新
|
485次组卷
|
5卷引用:河南省部分重点高中2021-2022学年高三上学期12月调研考试化学试题
名校
9 . 某大型企业利用含 、
、 的废液净化含有
的废液净化含有 的工业废气的工艺如图所示,既避免了空气污染又回收了硫黄,大大提高了生产效益。下列说法错误的是
的工业废气的工艺如图所示,既避免了空气污染又回收了硫黄,大大提高了生产效益。下列说法错误的是

 、
、 的废液净化含有
的废液净化含有 的工业废气的工艺如图所示,既避免了空气污染又回收了硫黄,大大提高了生产效益。下列说法错误的是
的工业废气的工艺如图所示,既避免了空气污染又回收了硫黄,大大提高了生产效益。下列说法错误的是
A.步骤①中 是还原剂 是还原剂 | B.总反应为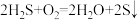 |
C.氧化性: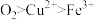 | D.步骤③中每生成 消耗 消耗 |
您最近一年使用:0次
2022-02-25更新
|
1653次组卷
|
5卷引用:河南省平顶山市2021-2022学年高一上学期期末调研考试化学试题



