1 . 某小组同学探究溶液中的 能否被金属钠还原,进行实验:
能否被金属钠还原,进行实验:
①在干燥试管中加入绿豆大小的金属钠,逐滴滴加 溶液,产生无色气体,溶液由紫红色变为浅绿色
溶液,产生无色气体,溶液由紫红色变为浅绿色 。
。
②向 溶液中持续通入
溶液中持续通入 ,水浴加热,溶液颜色无明显变化。
,水浴加热,溶液颜色无明显变化。
③向 溶液中加入
溶液中加入 固体,溶液由紫红色变为浅绿色。
固体,溶液由紫红色变为浅绿色。
下列说法不正确 的是
 能否被金属钠还原,进行实验:
能否被金属钠还原,进行实验:①在干燥试管中加入绿豆大小的金属钠,逐滴滴加
 溶液,产生无色气体,溶液由紫红色变为浅绿色
溶液,产生无色气体,溶液由紫红色变为浅绿色 。
。②向
 溶液中持续通入
溶液中持续通入 ,水浴加热,溶液颜色无明显变化。
,水浴加热,溶液颜色无明显变化。③向
 溶液中加入
溶液中加入 固体,溶液由紫红色变为浅绿色。
固体,溶液由紫红色变为浅绿色。下列说法
| A.实验①中还可能观察到钠块浮在溶液表面,剧烈燃烧,发出黄色火焰 |
| B.实验②中的现象说明实验①中溶液变色的原因与产生的气体无关 |
C.实验③中的现象说明实验①中可能发生的反应: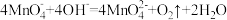 |
D.上述实验能证明溶液中的 可以被金属钠还原 可以被金属钠还原 |
您最近一年使用:0次
2023-05-07更新
|
1684次组卷
|
7卷引用:T12-化学反应及限度
(已下线)T12-化学反应及限度(已下线)第4讲 钠及其重要化合物(已下线)选择题11-14(已下线)选择题6-10北京市海淀区2022-2023学年高三第二次模拟(下学期期末)考试化学试题北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题湖南省邵阳市第二中学2023-2024学年高二上学期基础知识竞赛化学试题
名校
2 . 硅是大数据时代的关键材料。工业上常在1800—2000℃时,用碳单质还原的方法制取单质硅。涉及反应的相关数据如表所示。下列相关说法正确的是
| 反应 | △H/(kJ•mol-1) | △S/(J•K-1•mol-1) |
| 反应(1):SiO2(s)+2C(s)=Si(s)+2CO(g) | 687.27 | 359.04 |
| 反应(2):SiO2(s)+C(s)=Si(s)+CO2(g) | 514.85 | 183.35 |
| A.反应(1)可证明Si的还原性大于C |
| B.生活中利用单晶硅良好的导光性能做光导纤维 |
| C.工业生产条件下反应(2)无法自发进行发生 |
| D.C(s)+CO2(g)=2CO(g) △H=-172.42kJ·mol-1 |
您最近一年使用:0次
2022-01-08更新
|
1342次组卷
|
6卷引用:专题04氧化还原反应-五年(2018~2022)高考真题汇编(全国卷)
(已下线)专题04氧化还原反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题04氧化还原反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题04氧化还原反应-三年(2020~2022)高考真题汇编(全国卷)河南省郑州市2022届高三上学期第一次质量预测(1月)化学试题河南省郑州市第四高级中学2021-2022学年高二下学期第二次调研考试西藏班化学试题吉林省通化市梅河口市第五中学2023-2024学年高二上学期第三次月考化学试题
3 . 某同学为验证Fe3+的氧化性进行了如下实验:
已知相同条件下AgCl的溶解度小于Ag2SO4.下列说法不正确的是
| 序号 | 操作 | 现象 |
| 实验I | 将2 mL 2 mol∙L−1Fe(NO3)3溶液加入有银镜的试管中 | 银镜消失 |
| 实验II | 将2 mL1 mol∙L−1 Fe2(SO4)3溶液加入有银镜的试管中 | 银镜减少,未消失 |
| 实验III | 将2mL2 mol∙L−1FeCl3溶液加入有银镜的试管中 | 银镜消失 |
| 实验IV | 将2mL 1 mol∙L−1 AgNO3溶液加入到1 mL 1 mol∙L−1 FeSO4溶液中 | 产生白色沉淀,随后有黑色固体产生 |
| A.实验I不能说明Fe3+氧化了Ag |
B.实验II和III说明溶液中存在平衡: Fe3++Ag Fe2++ Ag+ Fe2++ Ag+ |
| C.实验IV中产生白色沉淀,说明Ag+氧化了Fe2+ |
| D.欲证明实验IV中产生了Fe3+,可以取上层清液滴加KSCN溶液 |
您最近一年使用:0次
4 . 某课外小组为探究金属铜的还原性,进行如下实验:①将金属铜投入用 酸化的
酸化的 的
的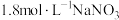 溶液中,现象不明显②将金属铜投入用盐酸酸化的
溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
的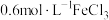 溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的
酸化的 的
的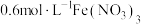 溶液中,铜粉溶解,溶液变为深棕色[经检验含
溶液中,铜粉溶解,溶液变为深棕色[经检验含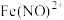 ],无气泡生成。下列分析正确的是
],无气泡生成。下列分析正确的是
 酸化的
酸化的 的
的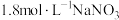 溶液中,现象不明显②将金属铜投入用盐酸酸化的
溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
的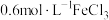 溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的
酸化的 的
的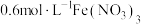 溶液中,铜粉溶解,溶液变为深棕色[经检验含
溶液中,铜粉溶解,溶液变为深棕色[经检验含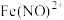 ],无气泡生成。下列分析正确的是
],无气泡生成。下列分析正确的是A.①说明 的 的 溶液不与铜粉反应 溶液不与铜粉反应 |
B.②证明氧化性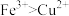 还原性 还原性 |
C.③中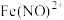 的生成速率一定小于 的生成速率一定小于 被还原的速率 被还原的速率 |
| D.在①中加入少量绿矾,铜粉可溶解,溶液变为深棕色 |
您最近一年使用:0次
2024高三下·全国·专题练习
5 . 8月1日起,为了国家信息安全,我国禁止镓和锗的出口,锗是一种重要的半导体材料,工业上用精硫锗矿(主要成分为GeS2)制取高纯度锗的工艺流程如图所示:

(1)COCl2分子中各原子均达到8电子稳定结构,其结构式为___________ 。
(2)800℃升华时通入N2的目的是:___________ 、___________ 。
(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:___________ ,酸浸时温度不能过高的原因是___________ 。
(4)GeCl4易水解生成GeCl4·n H2O,证明GeCl4·n H2O沉淀洗涤干净的方法是___________ 。

(1)COCl2分子中各原子均达到8电子稳定结构,其结构式为
(2)800℃升华时通入N2的目的是:
(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:
(4)GeCl4易水解生成GeCl4·n H2O,证明GeCl4·n H2O沉淀洗涤干净的方法是
您最近一年使用:0次
名校
解题方法
6 . 某同学欲探究H2O2的氧化还原性:
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,探究H2O2的氧化性可以选取的物质是:___________ (填序号)
①淀粉KI溶液(酸性) ②酸性KMnO4溶液 ③Cl2 ④HNO3溶液
任选一个你所选的物质进行实验,观察到___________ 现象,证明H2O2有氧化性,反应的离子方程式为___________ 。
(2)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。反应的离子方程式为___________ 。
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有___________ 性,能与H2O2反应产生MnO2
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
iii是ii和i的对照实验。
①X是___________ 。
②a是___________ 、b是___________ 。
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,探究H2O2的氧化性可以选取的物质是:
①淀粉KI溶液(酸性) ②酸性KMnO4溶液 ③Cl2 ④HNO3溶液
任选一个你所选的物质进行实验,观察到
(2)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。反应的离子方程式为
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
| 序号 | 实验 | 试剂 | 现象 |
| i | 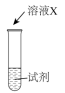 | a | 生成棕褐色固体,产生大量气泡 |
| ii | b | 有少量气泡 | |
| iii | H2O2溶液 | 有少量气泡 |
①X是
②a是
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
您最近一年使用:0次
名校
解题方法
7 . 下列由实验现象所得结论不正确 的是
A.向 溶液中滴加氢硫酸,立即产生淡黄色沉淀,证明 溶液中滴加氢硫酸,立即产生淡黄色沉淀,证明 具有氧化性 具有氧化性 |
B.向酸性 溶液中加入 溶液中加入 粉末,紫色褪去,证明 粉末,紫色褪去,证明 中含Fe(Ⅱ) 中含Fe(Ⅱ) |
C.向某溶液中滴加盐酸酸化的氯化钡溶液,有白色沉淀生成,证明溶液存在 |
D.向 溶液中加入几滴氯水振荡,再加 溶液中加入几滴氯水振荡,再加 萃取,下层呈紫色,上层无色,证明还原性 萃取,下层呈紫色,上层无色,证明还原性 |
您最近一年使用:0次
2023-05-27更新
|
372次组卷
|
4卷引用:考点45 物质的分离、提纯和检验(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
(已下线)考点45 物质的分离、提纯和检验(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)北京市中国人民大学附属中学2023届高三三模化学试题黑龙江省肇东市第四中学校2023-2024学年高三上学期第二次月考化学试卷天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高三上学期第二次阶段检测(期中)化学试题
8 . 某小组探究 溶液与KI溶液的反应及其速率,实验过程和现象如表。
溶液与KI溶液的反应及其速率,实验过程和现象如表。
已知:ⅰ. 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;
ⅱ.淀粉检测 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝;
即可快速变蓝;
ⅲ. 可与
可与 发生反应:
发生反应: 。
。
(1)实验1-1的目的是________________________ 。
(2) 与KI反应的离子方程式为
与KI反应的离子方程式为________________________ 。
为了研究 与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
(3)实验2-1不能用于测定 与KI反应的速率,原因有无
与KI反应的速率,原因有无 时反应生成少量
时反应生成少量 后淀粉立即变蓝,无法确定
后淀粉立即变蓝,无法确定 与
与 反应的浓度变化外,还有
反应的浓度变化外,还有____________ 。
(4)加入 溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
猜想1: 先与
先与 反应,使
反应,使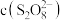 降低;
降低;
猜想2: 先与KI反应,
先与KI反应, ,
,
①甲同学提出猜想1的依据:由信息ⅲ推测, 的还原性
的还原性______ (填“强于”或“弱于”)KI的。
②乙同学根据现有数据证明猜想1不成立,理由是__________________ 。
③补全猜想2:________________________________________________ 。
(5)查阅文献表明猜想2成立。根据实验2-2的数据,计算30s内的平均反应速率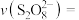
____________  (写出计算式)。
(写出计算式)。
(6)实验2-2中,30s内未检测到 与
与 反应,可能原因是
反应,可能原因是______ 。(写出2条)。
 溶液与KI溶液的反应及其速率,实验过程和现象如表。
溶液与KI溶液的反应及其速率,实验过程和现象如表。已知:ⅰ.
 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;ⅱ.淀粉检测
 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝;
即可快速变蓝;ⅲ.
 可与
可与 发生反应:
发生反应: 。
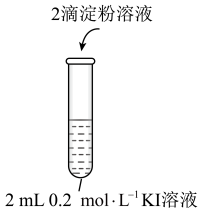
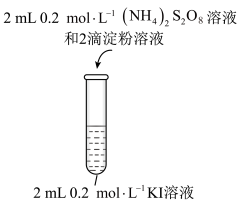
。编号 | 1-1 | 1-2 |
实验操作 |
|
|
现象 | 无明显现象 | 溶液立即变蓝 |
(2)
 与KI反应的离子方程式为
与KI反应的离子方程式为为了研究
 与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。
与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,如表。编号 |
|
| 蒸馏水/mL | 0.4%的淀粉溶液/滴 |
| 变色时间/s |
2-1 | 2 | 0 | 2.8 | 2 | 0.2 | 立即 |
2-2 | 2 | 0.8 | 0.2 | 2 | 2 | 30 |
 与KI反应的速率,原因有无
与KI反应的速率,原因有无 时反应生成少量
时反应生成少量 后淀粉立即变蓝,无法确定
后淀粉立即变蓝,无法确定 与
与 反应的浓度变化外,还有
反应的浓度变化外,还有(4)加入
 溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。猜想1:
 先与
先与 反应,使
反应,使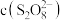 降低;
降低;猜想2:
 先与KI反应,
先与KI反应, ,
,①甲同学提出猜想1的依据:由信息ⅲ推测,
 的还原性
的还原性②乙同学根据现有数据证明猜想1不成立,理由是
③补全猜想2:
(5)查阅文献表明猜想2成立。根据实验2-2的数据,计算30s内的平均反应速率
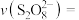
 (写出计算式)。
(写出计算式)。(6)实验2-2中,30s内未检测到
 与
与 反应,可能原因是
反应,可能原因是
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
9 . 完成下列实验设计题:
(1)证明CO2中含有CO___________
(2)证明SO2中含有CO2___________
(3)证明SO 中含有SO
中含有SO
___________
(4)①证明H2C2O4是弱酸;②证明草酸的酸性强于碳酸;③证明草酸是二元酸___________ (提供的试剂:0.1 mol·L-1 NaHCO3溶液、0.1 mol·L-1草酸溶液、0.1 mol·L-1 NaOH溶液、Na2C2O4晶体、甲基橙、酚酞、pH试纸)
(5)设计一个实验方案证明酸性条件下NaNO2具有氧化性___________ (提供的试剂:0.10 mol·L-1 NaNO2溶液、KMnO4溶液、0.10 mol·L-1 KI溶液、淀粉溶液、稀硝酸、稀硫酸)
(1)证明CO2中含有CO
(2)证明SO2中含有CO2
(3)证明SO
 中含有SO
中含有SO
(4)①证明H2C2O4是弱酸;②证明草酸的酸性强于碳酸;③证明草酸是二元酸
(5)设计一个实验方案证明酸性条件下NaNO2具有氧化性
您最近一年使用:0次
名校
10 . 实验室可用NaClO3制取ClO2气体,再由ClO2制得NaClO2,实验装置如图所示:回答下列问题:
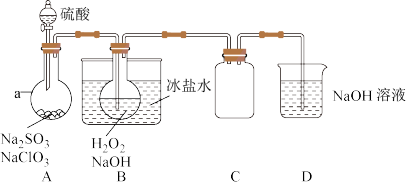
(1)仪器a的名称为___________ ;装置C的作用是___________ 。
(2)B中发生反应的化学方程式为___________ 。
(3)该实验必须使NaClO3稍微过量,目的是___________ 。
(4)证明NaClO2具有氧化性的方法是:取少量将B中溶液于试管中,先___________ ,再加入___________ (填序号,下同)酸化,最后加入___________ 检验。
①稀HNO3②稀H2SO4③K2SO3溶液④BaCl2溶液⑤FeCl2溶液⑥KSCN溶液

(1)仪器a的名称为
(2)B中发生反应的化学方程式为
(3)该实验必须使NaClO3稍微过量,目的是
(4)证明NaClO2具有氧化性的方法是:取少量将B中溶液于试管中,先
①稀HNO3②稀H2SO4③K2SO3溶液④BaCl2溶液⑤FeCl2溶液⑥KSCN溶液
您最近一年使用:0次

 KI溶液/mL
KI溶液/mL


