1 . 在处理NO废气的过程中,催化剂 会逐渐失活变为
会逐渐失活变为 。
。
某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:i.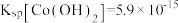 ;
;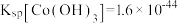 。
。
ii.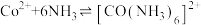
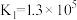 ;
;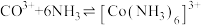
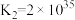 。
。
iii. 和
和 在酸性条件下均能生成
在酸性条件下均能生成 。
。
(1)探 的还原性
的还原性
实验I 粉红色的 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。
实验Ⅱ 向 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。
实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。 可以被酸性
可以被酸性 溶液氧化。乙同学补充实验IV,
溶液氧化。乙同学补充实验IV,_______ (补全实验操作及现象),否定了该观点。
②探究碱性条件下 的还原性,进行实验。
的还原性,进行实验。_______ 。
③根据氧化还原反应规律解释还原性 :
: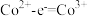 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使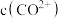 和
和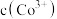 均降低,但
均降低,但_______ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验Ⅲ和IV推测氧化性: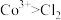 ,设计实验证明:向V中得到的棕褐色沉淀中,
,设计实验证明:向V中得到的棕褐色沉淀中,_______ (补全实验操作及现象),反应方程式为_______ 。
②向V中得到的棕褐色沉淀中,滴加 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是_______ 。
(3)催化剂 的失活与再生
的失活与再生
①结合数据解释 能被氧化为
能被氧化为 而失活的原因:
而失活的原因:_______ 。
②根据以上实验,设计物质转化流程图 实现 的再生:
的再生:_______ 。示例:
 会逐渐失活变为
会逐渐失活变为 。
。某小组为解决这一问题,实验研究
 和
和 之间的相互转化。
之间的相互转化。资料:i.
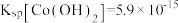 ;
;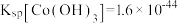 。
。ii.
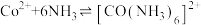
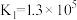 ;
;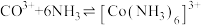
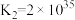 。
。iii.
 和
和 在酸性条件下均能生成
在酸性条件下均能生成 。
。(1)探
 的还原性
的还原性实验I 粉红色的
 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。实验Ⅱ 向
 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。
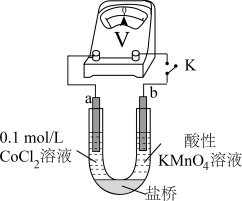
 可以被酸性
可以被酸性 溶液氧化。乙同学补充实验IV,
溶液氧化。乙同学补充实验IV,②探究碱性条件下
 的还原性,进行实验。
的还原性,进行实验。实验V: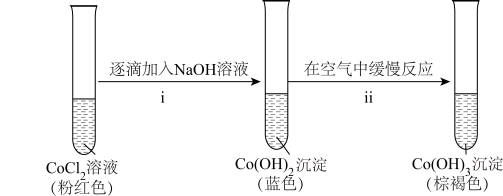
③根据氧化还原反应规律解释还原性
 :
: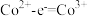 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使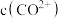 和
和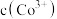 均降低,但
均降低,但(2)探究
 的氧化性
的氧化性①根据实验Ⅲ和IV推测氧化性:
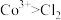 ,设计实验证明:向V中得到的棕褐色沉淀中,
,设计实验证明:向V中得到的棕褐色沉淀中,②向V中得到的棕褐色沉淀中,滴加
 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是(3)催化剂
 的失活与再生
的失活与再生①结合数据解释
 能被氧化为
能被氧化为 而失活的原因:
而失活的原因:②根据以上实验,设计物质转化
 的再生:
的再生:
您最近一年使用:0次
2 . 某同学为研究浓硝酸与KSCN溶液的反应,进行如下实验:
资料:SCN-能被氧化为(SCN)2,(SCN)2迅速聚合为红色的(SCN)x.
(1)KSCN中,C、N元素的化合价分别为 价和
价和 分价,则S元素的化合价为
分价,则S元素的化合价为______ 。
(2)Ⅰ中溶液立即变红是因为生成了______ (填化学式)。
(3)研究 SCN-的最终转化产物。
①取少量Ⅱ中试管内的溶液,______ (填操作和现象),证明SCN-中S元素的转化产物是 。
。
②经检验Ⅱ中“红棕色气体”含有NO2,但不能说明NO2一定是SCN-中N元素的转化产物,原因是______ 。
③在Ⅲ中NO2转化为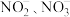 。将Ⅲ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量KMnO4溶液,不褪色。证明了红棕色气体中不含SO2。综合上述实验,SCN-的最终转化产物中一定有
。将Ⅲ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量KMnO4溶液,不褪色。证明了红棕色气体中不含SO2。综合上述实验,SCN-的最终转化产物中一定有______ 。
(4)Ⅱ中,“静置一段时间后,突然剧烈反应”的可能原因是______ (写出一条即可)。
| 实验操作 | 实验现象 |
| Ⅰ.取1支试管,加入2mL浓硝酸,滴加5滴1mol/LKSCN溶液 | 溶液立即变红 |
| Ⅱ.将试管静置一段时间 | 突然剧烈反应,红色迅速褪去,放出大量红棕色气体 |
| Ⅲ.将Ⅱ中的气体通入Ba(OH)2和NaOH的混合溶液中 | 有白色沉淀生成 |
(1)KSCN中,C、N元素的化合价分别为
 价和
价和 分价,则S元素的化合价为
分价,则S元素的化合价为(2)Ⅰ中溶液立即变红是因为生成了
(3)研究 SCN-的最终转化产物。
①取少量Ⅱ中试管内的溶液,
 。
。②经检验Ⅱ中“红棕色气体”含有NO2,但不能说明NO2一定是SCN-中N元素的转化产物,原因是
③在Ⅲ中NO2转化为
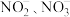 。将Ⅲ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量KMnO4溶液,不褪色。证明了红棕色气体中不含SO2。综合上述实验,SCN-的最终转化产物中一定有
。将Ⅲ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量KMnO4溶液,不褪色。证明了红棕色气体中不含SO2。综合上述实验,SCN-的最终转化产物中一定有(4)Ⅱ中,“静置一段时间后,突然剧烈反应”的可能原因是
您最近一年使用:0次
3 . 某小组同学探究硫代硫酸钠(Na2S2O3)溶液与某些常见金属离子的反应。
已知:i.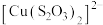 (淡绿色)、
(淡绿色)、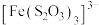 (紫黑色)、
(紫黑色)、 (无色)
(无色)
ii. 在酸性溶液中转化为
在酸性溶液中转化为 、S和SO2。
、S和SO2。
iii.BaS4O6可溶于水、BaS2O3微溶于水。
(1)将S粉加入沸腾的Na2SO3溶液中可制得Na2S2O3,离子方程式是___________ 。
(2)研究 Na2S2O3与某些常见金属离子的反应,进行如下实验。
①取I中的浊液,离心分离,经检验,沉淀是Cu2S和S的混合物,清液中存在 。
。
i.补全I中生成黑色沉淀的总反应的离子方程式:___________
 □___________
□___________ □___________
□___________ □___________
□___________ □___________+
□___________+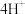
ii.查阅资料可知,常温时,生成黑色沉淀反应的平衡常数很大,但仍需水浴加热至50℃以上才出现沉淀,原因是___________ 。
②Ⅱ中, 被Fe3+氧化的主要产物是
被Fe3+氧化的主要产物是 ,还有很少量的
,还有很少量的 。取Ⅱ中的无色溶液进行如下实验证实了此结论。
。取Ⅱ中的无色溶液进行如下实验证实了此结论。
i.仅由溶液1中加入足量的盐酸后得到沉淀2,不能说明Ⅱ中生成了 ,理由是
,理由是___________ 。
ii.补全实验方案证实上述结论:将沉淀1洗净,___________ 。
③向Ⅲ的无色溶液中继续加入0.5mL 0.1mol·L-1AgNO3溶液,产生白色沉淀Ag2S2O3。静置,得到黑色沉淀Ag2S,同时生成强酸。生成Ag2S的化学方程式是___________ 。
(3)软硬酸碱原理认为,Ⅲ中, Ag+为软酸, 为软碱, S2-是比
为软碱, S2-是比 更软的碱,可解释
更软的碱,可解释 与Ag+反应的最终产物为Ag2S。由此推测,Ⅰ中, Cu+和Cu2+,
与Ag+反应的最终产物为Ag2S。由此推测,Ⅰ中, Cu+和Cu2+,___________ 是更软的酸。
已知:i.
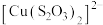 (淡绿色)、
(淡绿色)、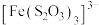 (紫黑色)、
(紫黑色)、 (无色)
(无色)ii.
 在酸性溶液中转化为
在酸性溶液中转化为 、S和SO2。
、S和SO2。iii.BaS4O6可溶于水、BaS2O3微溶于水。
(1)将S粉加入沸腾的Na2SO3溶液中可制得Na2S2O3,离子方程式是
(2)研究 Na2S2O3与某些常见金属离子的反应,进行如下实验。
| 序号 | X溶液 | 现象 |
| I | CuCl2溶液 | 溶液变为淡绿色,水浴加热至50℃以上,逐渐析出黑色沉淀 | |
| Ⅱ | FeCl3溶液 | 溶液变为紫黑色,片刻后溶液变为无色 | |
| Ⅲ | AgNO3溶液 | 逐滴加入AgNO3溶液,生成白色沉淀,振荡后沉淀溶解,得无色溶液 |
 。
。i.补全I中生成黑色沉淀的总反应的离子方程式:
 □___________
□___________ □___________
□___________ □___________
□___________ □___________+
□___________+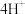
ii.查阅资料可知,常温时,生成黑色沉淀反应的平衡常数很大,但仍需水浴加热至50℃以上才出现沉淀,原因是
②Ⅱ中,
 被Fe3+氧化的主要产物是
被Fe3+氧化的主要产物是 ,还有很少量的
,还有很少量的 。取Ⅱ中的无色溶液进行如下实验证实了此结论。
。取Ⅱ中的无色溶液进行如下实验证实了此结论。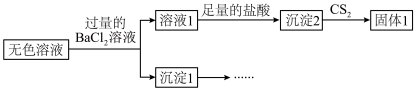
i.仅由溶液1中加入足量的盐酸后得到沉淀2,不能说明Ⅱ中生成了
 ,理由是
,理由是ii.补全实验方案证实上述结论:将沉淀1洗净,
③向Ⅲ的无色溶液中继续加入0.5mL 0.1mol·L-1AgNO3溶液,产生白色沉淀Ag2S2O3。静置,得到黑色沉淀Ag2S,同时生成强酸。生成Ag2S的化学方程式是
(3)软硬酸碱原理认为,Ⅲ中, Ag+为软酸,
 为软碱, S2-是比
为软碱, S2-是比 更软的碱,可解释
更软的碱,可解释 与Ag+反应的最终产物为Ag2S。由此推测,Ⅰ中, Cu+和Cu2+,
与Ag+反应的最终产物为Ag2S。由此推测,Ⅰ中, Cu+和Cu2+,
您最近一年使用:0次
4 . 某同学研究浓硝酸的氧化性,做了如下实验:
资料:
i. 中
中 、
、 、
、 元素的化合价依次为:
元素的化合价依次为: 价、
价、 价、
价、 价。
价。
ii. 的性质类似卤素离子,能被氧化为黄色的
的性质类似卤素离子,能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。
(1)写出实验Ⅰ中铜和浓硝酸反应的离子方程式______ 。
(2)甲同学对实验Ⅱ中红色褪去的原因提出猜想,浓硝酸氧化了 ,其理论依据是
,其理论依据是______ 。
甲同学为证明猜想,做了如下实验Ⅲ
实验Ⅲ: 溶液,溶液立即变红是因为生成了
溶液,溶液立即变红是因为生成了______ (填化学式)。推测红棕色气体是______ (填化学式)。
(4)研究 的转化产物:
的转化产物:
实验Ⅳ:
a.将实验Ⅲ 中的气体通入
中的气体通入 和
和 的混合溶液中,有白色沉淀生成。
的混合溶液中,有白色沉淀生成。
b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量 溶液,不褪色。
溶液,不褪色。
c.另取少量实验Ⅲ中反应后的溶液,加入 溶液,产生大量白色沉淀。
溶液,产生大量白色沉淀。
①通过 证实了红棕色气体中不含
证实了红棕色气体中不含 ,证据是
,证据是______ 。
② 中,
中, 溶液中加入
溶液中加入 溶液以增大
溶液以增大 浓度的目的是
浓度的目的是______ 。
③由上述实验现象可知: 转化的最终产物中一定有
转化的最终产物中一定有______ 。
序号 | 实验Ⅰ | 实验Ⅱ |
操作 | 1:2 | 1:2 |
实验现象 | 铜片迅速溶解,产生大量红棕色气体,溶液变成绿色 | 滴入硝酸后,溶液变为红色,一段时间后,溶液褪为无色。 |
i.
 中
中 、
、 、
、 元素的化合价依次为:
元素的化合价依次为: 价、
价、 价、
价、 价。
价。ii.
 的性质类似卤素离子,能被氧化为黄色的
的性质类似卤素离子,能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。(1)写出实验Ⅰ中铜和浓硝酸反应的离子方程式
(2)甲同学对实验Ⅱ中红色褪去的原因提出猜想,浓硝酸氧化了
 ,其理论依据是
,其理论依据是甲同学为证明猜想,做了如下实验Ⅲ
实验Ⅲ:
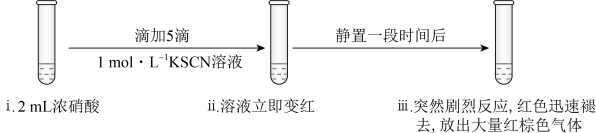
 溶液,溶液立即变红是因为生成了
溶液,溶液立即变红是因为生成了(4)研究
 的转化产物:
的转化产物:实验Ⅳ:
a.将实验Ⅲ
 中的气体通入
中的气体通入 和
和 的混合溶液中,有白色沉淀生成。
的混合溶液中,有白色沉淀生成。b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量
 溶液,不褪色。
溶液,不褪色。c.另取少量实验Ⅲ中反应后的溶液,加入
 溶液,产生大量白色沉淀。
溶液,产生大量白色沉淀。①通过
 证实了红棕色气体中不含
证实了红棕色气体中不含 ,证据是
,证据是②
 中,
中, 溶液中加入
溶液中加入 溶液以增大
溶液以增大 浓度的目的是
浓度的目的是③由上述实验现象可知:
 转化的最终产物中一定有
转化的最终产物中一定有
您最近一年使用:0次
名校
5 . 某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和
混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和 ,
,
①浓盐酸与 混合加热生成氯气的离子方程式为
混合加热生成氯气的离子方程式为______ ;
②电极反应式:
ⅰ.还原反应:
ⅱ.氧化反应:____________ 。
③根据电极反应式,分析A中仍存在盐酸和 的原因。
的原因。
ⅰ.随 降低或
降低或 升高,
升高, 氧化性减弱。
氧化性减弱。
ⅱ.随 降低,
降低,____________ 。
④补充实验证实了③中的分析。
a是______ ,b是______ 。
(2)利用 对
对 氧化性的影响,探究卤素离子的还原性。
氧化性的影响,探究卤素离子的还原性。
相同浓度的KCl、KBr和KI溶液,能与 反应所需的最低
反应所需的最低 由大到小的顺序是
由大到小的顺序是____________ ,从原子结构角度说明理由____________ 。
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将 氧化为
氧化为 。经实验证实了推测。该化合物是
。经实验证实了推测。该化合物是____________ 。
(4)总结:物质氧化性和还原性变化的一般规律是____________ 。
(1)浓盐酸与
 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和
混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和 ,
,①浓盐酸与
 混合加热生成氯气的离子方程式为
混合加热生成氯气的离子方程式为②电极反应式:
ⅰ.还原反应:

ⅱ.氧化反应:
③根据电极反应式,分析A中仍存在盐酸和
 的原因。
的原因。ⅰ.随
 降低或
降低或 升高,
升高, 氧化性减弱。
氧化性减弱。ⅱ.随
 降低,
降低,④补充实验证实了③中的分析。
序号 | 实验 | 加入试剂 | 现象 |
Ⅰ |
| 较浓硫酸 | 有氯气 |
Ⅱ | a | 有氯气 | |
III | a和b | 无氯气 |
(2)利用
 对
对 氧化性的影响,探究卤素离子的还原性。
氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与
 反应所需的最低
反应所需的最低 由大到小的顺序是
由大到小的顺序是(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将
 氧化为
氧化为 。经实验证实了推测。该化合物是
。经实验证实了推测。该化合物是(4)总结:物质氧化性和还原性变化的一般规律是
您最近一年使用:0次
名校
6 . 实验小组探究溶液酸碱性对锰化合物和Na2S2O3氧化还原反应的影响。
资料:i. MnO 呈绿色,MnO2为棕黑色沉淀,Mn2+几乎无色。
呈绿色,MnO2为棕黑色沉淀,Mn2+几乎无色。
ii. MnO 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为MnO
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为MnO 和MnO2。
和MnO2。
iii. BaS2O3为微溶物。
(1)用离子方程式解释实验I中出现乳白色浑浊的原因___________ 。
(2)已知,实验I、Ⅱ、Ⅲ中S2O 均被氧化为SO
均被氧化为SO 。针对实验I、Ⅱ、Ⅲ进行分析:
。针对实验I、Ⅱ、Ⅲ进行分析:
① 能得出“pH对KMnO4还原产物有影响”的证据是___________ 。
② 实验Ⅱ所得溶液中SO 的检验方法为
的检验方法为___________ 。
(3)针对实验Ⅲ、Ⅳ进行分析:
① 实验Ⅲ中“溶液变为绿色”相应反应的离子方程式为___________ 。
② 实验Ⅳ中“静置5 min,有棕黑色沉淀生成”的可能原因(写出2点):___________
(4)针对实验Ⅲ、Ⅳ继续探究:
① 实验V:向实验Ⅲ的试管中继续滴加足量H2SO4,振荡,溶液立即变为紫红色,产生棕黑色沉淀。
② 实验Ⅵ:向实验Ⅳ的试管中继续滴加足量H2SO4,振荡,绿色溶液迅速变为无色,棕黑色沉淀逐渐减少直至消失。静置一段时间后,出现乳白色浑浊。
对比实验V、Ⅵ,结合方程式分析实验VI滴加H2SO4后溶液未见紫红色的可能原因___________ 。
(5)综合上述实验,在下图中用连线的方式补充完善实验I~Ⅵ已证实的锰化合物转化关系___________ 。
资料:i. MnO
 呈绿色,MnO2为棕黑色沉淀,Mn2+几乎无色。
呈绿色,MnO2为棕黑色沉淀,Mn2+几乎无色。ii. MnO
 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为MnO
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为MnO 和MnO2。
和MnO2。iii. BaS2O3为微溶物。
| 实验 | 序号 | 试剂 | 现象 |
|
| I | a:10滴3 mol·L−1 H2SO4 溶液 b:20滴 0.002mol·L−1 Na2S2O3溶液 | 溶液紫色变浅至接近无色,静置一段时间后出现乳白色浑浊。 |
| Ⅱ | a:10滴蒸馏水 b:20滴 0.002mol·L−1 Na2S2O3溶液 | 紫色溶液逐渐褪色,产生棕黑色沉淀。 | |
| Ⅲ | a:10滴6 mol·L−1 NaOH 溶液 b:2滴0.002mol·L−1 Na2S2O3溶液和18滴蒸馏水 | 溶液变为绿色,无沉淀生成;静置5 min,未见明显变化。 | |
| Ⅳ | a:10滴6mol·L−1 NaOH 溶液 b:20滴 0.002mol·L−1 Na2S2O3溶液 | 溶液变为绿色,无沉淀生成;静置5 min,绿色变浅,有棕黑色沉淀生成。 |
(1)用离子方程式解释实验I中出现乳白色浑浊的原因
(2)已知,实验I、Ⅱ、Ⅲ中S2O
 均被氧化为SO
均被氧化为SO 。针对实验I、Ⅱ、Ⅲ进行分析:
。针对实验I、Ⅱ、Ⅲ进行分析:① 能得出“pH对KMnO4还原产物有影响”的证据是
② 实验Ⅱ所得溶液中SO
 的检验方法为
的检验方法为(3)针对实验Ⅲ、Ⅳ进行分析:
① 实验Ⅲ中“溶液变为绿色”相应反应的离子方程式为
② 实验Ⅳ中“静置5 min,有棕黑色沉淀生成”的可能原因(写出2点):
(4)针对实验Ⅲ、Ⅳ继续探究:
① 实验V:向实验Ⅲ的试管中继续滴加足量H2SO4,振荡,溶液立即变为紫红色,产生棕黑色沉淀。
② 实验Ⅵ:向实验Ⅳ的试管中继续滴加足量H2SO4,振荡,绿色溶液迅速变为无色,棕黑色沉淀逐渐减少直至消失。静置一段时间后,出现乳白色浑浊。
对比实验V、Ⅵ,结合方程式分析实验VI滴加H2SO4后溶液未见紫红色的可能原因
(5)综合上述实验,在下图中用连线的方式补充完善实验I~Ⅵ已证实的锰化合物转化关系

您最近一年使用:0次
7 . 硫代硫酸钠(Na2S2O3)是重要的化工原料易溶于水,在中性或碱性环境下稳定,在酸性溶液水,分解产生S、SO2。
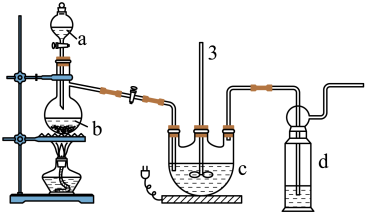
Ⅰ.Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示,其C中试剂为Na2S和Na2SO3的混合液。
(1)b中反应的离子方程式为_____ 。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是_____ 。
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2,不能过量,原因是_____ 。
(4)制备得到的Na2S2O3中可能含有Na2SO3、Na2SO4等杂质。设计实验,检测产品中是否存在Na2SO4:取少量产品_____ 。
Ⅱ.探究Na2S2O3与金属阳离子的氧化还原反应。
资料:ⅰ.Fe3++3S2O
 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)
ⅱ.Ag2S2O3为白色沉淀,Ag2S2O3可溶于过量的S2O
(5)根据实验①的现象,初步判断最终Fe3+被S2O 还原为Fe2+,通过
还原为Fe2+,通过_____ (填操作、试剂和现象),进一步证实生成了Fe2+。从化学反应速率和平衡的角度解释实验Ⅰ的现象:_____ 。
(6)同浓度氧化性:Ag+>Fe3+。实验②中Ag+未发生氧化还原反应的原因是_____ 。
(7)进一步探究Ag+和S2O 反应。
反应。
实验③中白色絮状沉淀最后变为黑色沉淀(Ag2S)的化学方程式如下,填入合适的物质和系数:_____ 。
Ag2S2O3+_____=Ag2S+_____
(8)根据以上实验,Na2S2O3与金属阳离子发生氧化还原反应和_____ 有关(写出两条)。

Ⅰ.Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示,其C中试剂为Na2S和Na2SO3的混合液。
(1)b中反应的离子方程式为
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2,不能过量,原因是
(4)制备得到的Na2S2O3中可能含有Na2SO3、Na2SO4等杂质。设计实验,检测产品中是否存在Na2SO4:取少量产品
Ⅱ.探究Na2S2O3与金属阳离子的氧化还原反应。
资料:ⅰ.Fe3++3S2O

 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)ⅱ.Ag2S2O3为白色沉淀,Ag2S2O3可溶于过量的S2O

| 装置 | 编号 | 试剂X | 实验现象 |
 | ① | Fe(NO3)3溶液 | 混合后溶液先变成紫黑色,30s后溶液几乎变为无色 |
| ② | AgNO3溶液 | 先生成白色絮状沉淀,振荡后,沉淀溶解,得到无色溶液 |
(5)根据实验①的现象,初步判断最终Fe3+被S2O
 还原为Fe2+,通过
还原为Fe2+,通过(6)同浓度氧化性:Ag+>Fe3+。实验②中Ag+未发生氧化还原反应的原因是
(7)进一步探究Ag+和S2O
 反应。
反应。| 装置 | 编号 | 试剂X | 实验现象 |
 | ② | AgNO3溶液 | 先生成白色絮状沉淀,沉淀很快变成黄色、棕色,最后为黑色沉淀。 |
Ag2S2O3+_____=Ag2S+_____
(8)根据以上实验,Na2S2O3与金属阳离子发生氧化还原反应和
您最近一年使用:0次
名校
解题方法
8 . 合成氨工业产生的钻钼废催化剂(主要成分MoS2、CoO、Fe2O3等)是一种相当宝贵的二次资源。用碱浸法处理钻钼废催化剂的工艺流程如图:
i.氧化钼(MoO3):熔点795℃。易升华(即使在低于熔点情况下,也有显著的升华现象)。
ii.钼酸(H2MoO4):难溶于水和酸的黄色晶体,可通过酸化钼酸盐溶液而制得。
(1)焙烧:
①将废催化剂在空气中焙烧可生成氧化钼,写出反应的化学方程式_______ 。
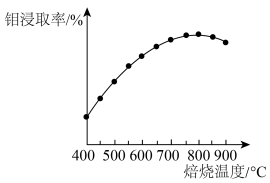
②解释钼浸取率随焙烧温度变化的原因是_______ 。
碱浸时杂质钴元素以Co(OH)2的形式浸出,加入双氧水可将其氧化为Co(OH)3沉淀。写出反应的化学方程式_______ 。
(3)酸沉:
传统工艺中酸沉多在不锈钢离心机中进行。文献记载,选用浓硝酸比用硫酸和盐酸效果更佳,可避免Mo(VI)还原成低价态,利用了浓硝酸的_______ 性。
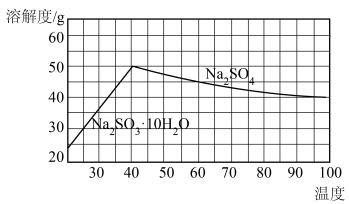
(4)从母液中获得无水Na2SO4的操作是_______ 。

i.氧化钼(MoO3):熔点795℃。易升华(即使在低于熔点情况下,也有显著的升华现象)。
ii.钼酸(H2MoO4):难溶于水和酸的黄色晶体,可通过酸化钼酸盐溶液而制得。
(1)焙烧:
①将废催化剂在空气中焙烧可生成氧化钼,写出反应的化学方程式
②解释钼浸取率随焙烧温度变化的原因是
碱浸时杂质钴元素以Co(OH)2的形式浸出,加入双氧水可将其氧化为Co(OH)3沉淀。写出反应的化学方程式
(3)酸沉:
传统工艺中酸沉多在不锈钢离心机中进行。文献记载,选用浓硝酸比用硫酸和盐酸效果更佳,可避免Mo(VI)还原成低价态,利用了浓硝酸的
(4)从母液中获得无水Na2SO4的操作是
您最近一年使用:0次
名校
解题方法
9 . 资料显示, 能还原
能还原 、
、 ,某小组对此进行探究。
,某小组对此进行探究。
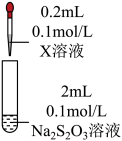
实验:将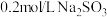 溶液滴入到物质a中,记录如下:
溶液滴入到物质a中,记录如下:
(1)用化学用语解释 溶液呈碱性的原因
溶液呈碱性的原因___________ 。
(2)经检验,I中白色沉淀是 。用酸性
。用酸性 溶液证实白色沉淀中含有
溶液证实白色沉淀中含有 ,现象是
,现象是___________ 。
(3)重新设计实验(III),证实了: 能还原
能还原 ,装置如下图所示。
,装置如下图所示。
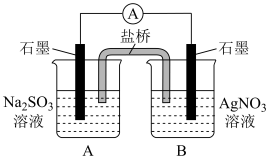
现象:i.电流表指针偏转。
ii.B中石墨电极上析出白色固体。
取出少量白色固体,洗涤后,___________ (填操作和现象),证明白色固体中含有Ag。
(4)经检验,II中的棕黄色沉淀不含 ,含有
,含有 、
、 和
和 。
。
资料: ,
, 。
。
①用稀 溶解沉淀,析出红色固体,说明棕黄色沉淀中含有
溶解沉淀,析出红色固体,说明棕黄色沉淀中含有___________ 。
②通过下列实验证实,沉淀中含有 和上层清液中仍检出了
和上层清液中仍检出了 (忽略空气的影响)。
(忽略空气的影响)。
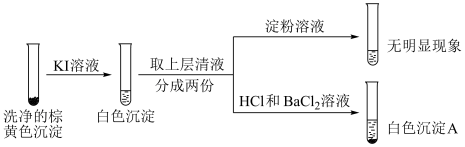
i.白色沉淀A是 。
。
ii.根据资料,上层清液加入淀粉后应该变蓝。分析现象与资料不符的原因:
原因一:KI未被氧化。则将 氧化的微粒是
氧化的微粒是___________ 。
原因二:KI被氧化,由于___________ (用离子方程式表示),所以无明显现象。
③当加入的KI过量且反应充分时,白色沉淀中不含Cu单质,上层清液中仍检出了 。结合物质组成、化学反应等解释上层清液中检出
。结合物质组成、化学反应等解释上层清液中检出 的原因
的原因___________ 。
小结:I中: 未能还原
未能还原 的原因与反应速率、离子浓度变化等因素有关。
的原因与反应速率、离子浓度变化等因素有关。
 能还原
能还原 、
、 ,某小组对此进行探究。
,某小组对此进行探究。实验:将
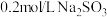 溶液滴入到物质a中,记录如下:
溶液滴入到物质a中,记录如下:| 序号 | 装置 | 物质a | 现象 |
| I | 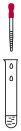 2 mL 物质a | 饱和 溶液 溶液 | 产生白色沉淀 |
| II | 0.2 mol/L  溶液 溶液 | 溶液变绿,继续滴加产生棕黄色沉淀 |
(1)用化学用语解释
 溶液呈碱性的原因
溶液呈碱性的原因(2)经检验,I中白色沉淀是
 。用酸性
。用酸性 溶液证实白色沉淀中含有
溶液证实白色沉淀中含有 ,现象是
,现象是(3)重新设计实验(III),证实了:
 能还原
能还原 ,装置如下图所示。
,装置如下图所示。
现象:i.电流表指针偏转。
ii.B中石墨电极上析出白色固体。
取出少量白色固体,洗涤后,
(4)经检验,II中的棕黄色沉淀不含
 ,含有
,含有 、
、 和
和 。
。资料:
 ,
, 。
。①用稀
 溶解沉淀,析出红色固体,说明棕黄色沉淀中含有
溶解沉淀,析出红色固体,说明棕黄色沉淀中含有②通过下列实验证实,沉淀中含有
 和上层清液中仍检出了
和上层清液中仍检出了 (忽略空气的影响)。
(忽略空气的影响)。
i.白色沉淀A是
 。
。ii.根据资料,上层清液加入淀粉后应该变蓝。分析现象与资料不符的原因:
原因一:KI未被氧化。则将
 氧化的微粒是
氧化的微粒是原因二:KI被氧化,由于
③当加入的KI过量且反应充分时,白色沉淀中不含Cu单质,上层清液中仍检出了
 。结合物质组成、化学反应等解释上层清液中检出
。结合物质组成、化学反应等解释上层清液中检出 的原因
的原因小结:I中:
 未能还原
未能还原 的原因与反应速率、离子浓度变化等因素有关。
的原因与反应速率、离子浓度变化等因素有关。
您最近一年使用:0次
名校
解题方法
10 . 物质类别与元素化合价是研究物质性质的两个视角,下列是硫元素及其化合物的“价类二维图”.根据要求回答下列问题:

(1)写出图中A的化学式:______ .
(2) 属于
属于______ 氧化物,因此可与 、
、______ (写出与 不同类别的一个具体物质)等反应.当:
不同类别的一个具体物质)等反应.当: 与足量
与足量 溶液反应时,写出反应的离子方程式
溶液反应时,写出反应的离子方程式______ .
(3)小艾同学预测 具有还原性,其理论依据是
具有还原性,其理论依据是______ ,将 通入
通入 溶液中,下列实验事实能够证实
溶液中,下列实验事实能够证实 具有还原性的是
具有还原性的是______ .
①反应后溶液由黄色变为浅绿色
②取反应后的溶液少许,加入 溶液,产生白色沉淀
溶液,产生白色沉淀
③取反应后的溶液少许,加入 溶液,产生白色沉淀.
溶液,产生白色沉淀.
(4) 与酸性高锰酸钾反应时,后者的产物是
与酸性高锰酸钾反应时,后者的产物是 ,试写出该反应的离子方程式
,试写出该反应的离子方程式______ 其中 是
是______ (填“氧化剂”或“还原剂”)

(1)写出图中A的化学式:
(2)
 属于
属于 、
、 不同类别的一个具体物质)等反应.当:
不同类别的一个具体物质)等反应.当: 与足量
与足量 溶液反应时,写出反应的离子方程式
溶液反应时,写出反应的离子方程式(3)小艾同学预测
 具有还原性,其理论依据是
具有还原性,其理论依据是 通入
通入 溶液中,下列实验事实能够证实
溶液中,下列实验事实能够证实 具有还原性的是
具有还原性的是①反应后溶液由黄色变为浅绿色
②取反应后的溶液少许,加入
 溶液,产生白色沉淀
溶液,产生白色沉淀③取反应后的溶液少许,加入
 溶液,产生白色沉淀.
溶液,产生白色沉淀.(4)
 与酸性高锰酸钾反应时,后者的产物是
与酸性高锰酸钾反应时,后者的产物是 ,试写出该反应的离子方程式
,试写出该反应的离子方程式 是
是
您最近一年使用:0次