1 . 设阿伏加德罗常数的值为 ,则下列说法正确的是
,则下列说法正确的是
 ,则下列说法正确的是
,则下列说法正确的是A.标准状况下, 个 个 分子占据空间的体积约为22.4 L 分子占据空间的体积约为22.4 L |
B.将含0.6 mol HCl溶质的浓盐酸与足量 共热,生成 共热,生成 的分子数为 的分子数为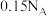 |
C.常温常压下,16 g 中含有的C-H共价键个数为 中含有的C-H共价键个数为 |
D.在0.1 mol/L  溶液中, 溶液中,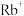 的数量为 的数量为 |
您最近一年使用:0次
解题方法
2 . 下列关于各实验装置的描述中,不恰当的是
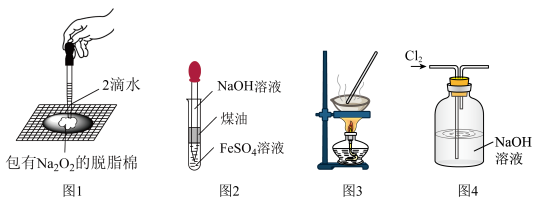
| A.图1的实验可以证明过氧化钠与水反应放热 |
B.图2中的溶液要提前驱除溶解的氧气,以制备 |
| C.图3的装置可以用于去除碳酸钠中的碳酸氢钠 |
| D.图4的装置可能发生倒吸,需要改进 |
您最近一年使用:0次
名校
解题方法
3 . 下列装置可以用于相应实验的是
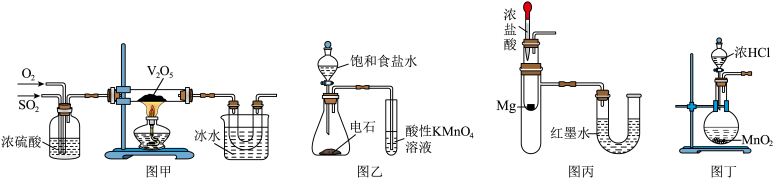
| A.图甲制取并收集SO3 | B.图乙检验乙炔具有还原性 |
| C.图丙中红墨水左高右低 | D.图丁装置制取Cl2 |
您最近一年使用:0次
2024-05-08更新
|
484次组卷
|
2卷引用:2024年辽宁省抚顺市普通高中高三下学期模拟考试化学试卷
4 . 空气吹出法工艺,是目前“海水提溴”的最主要方法之一、其工艺流程如下:___________ 。
(2)步骤④利用了SO2的还原性,反应的离子方程式:___________ 。
(3)从含溴海水中吹出的溴也可用纯碱吸收,纯碱吸收溴的主要反应是3Na2CO3+3Br2=NaBrO3+5NaBr+3CO2;吸收1 mol Br2时,转移的电子为___________ mol。纯碱吸收后再用硫酸酸化,单质溴又从溶液中析出。

(2)步骤④利用了SO2的还原性,反应的离子方程式:
(3)从含溴海水中吹出的溴也可用纯碱吸收,纯碱吸收溴的主要反应是3Na2CO3+3Br2=NaBrO3+5NaBr+3CO2;吸收1 mol Br2时,转移的电子为
您最近一年使用:0次
解题方法
5 . 用下列实验装置完成对应实验,能达到实验目的的是
选项 | A | B | C | D |
实验装置 |
|
|
|
|
实验目的 | 验证浓硫酸具有脱水性和氧化性 | 制取氨气 | 干燥 | 喷泉实验 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 如图所示,从左侧通入干燥的氯气,若打开止水夹Ⅰ,关闭止水夹Ⅱ,红色布条不褪色;若关闭止水夹Ⅰ,打开止水夹Ⅱ,红色布条褪色。甲瓶中所盛的试剂可能是

| A.Ba(OH)2溶液 | B.浓硫酸 | C.饱和食盐水 | D. NaBr溶液 |
您最近一年使用:0次
7 . 某化学实验小组同学为探究氯水的漂白性,设计了如图实验装置(夹持装置已略去)。
回答下列问题:
(1)装置Ⅰ中发生反应的化学方程式为 :
:
① 中
中 元素的化合价为
元素的化合价为_____ 。
②实验进行一段时间后,可观察到装置Ⅱ中的品红溶液褪色,其中 属于
属于_____ (填“酸”或“碱”)性氧化物。
③仪器 的名称为
的名称为_______ 。
④从其组成的阳离子来看, 属于
属于____ 盐。
(2)在装置Ⅳ和装置Ⅴ中:
①装置Ⅴ中发生反应的离子方程式为____ 。
②装置Ⅴ中可观察到的现象为____ 。
③实验进行一段时间后,可观察到装置Ⅳ中的品红溶液褪色,下列说法正确的是____ (填标号)。
A.起漂白作用的一定是
B.反应结束后,装置Ⅳ中溶液的 小于7
小于7
C.装置Ⅳ可能观察到 生成速率的快慢
生成速率的快慢
(3)装置Ⅲ中生成硫酸盐反应的化学方程式为______ 。

回答下列问题:
(1)装置Ⅰ中发生反应的化学方程式为
 :
:①
 中
中 元素的化合价为
元素的化合价为②实验进行一段时间后,可观察到装置Ⅱ中的品红溶液褪色,其中
 属于
属于③仪器
 的名称为
的名称为④从其组成的阳离子来看,
 属于
属于(2)在装置Ⅳ和装置Ⅴ中:
①装置Ⅴ中发生反应的离子方程式为
②装置Ⅴ中可观察到的现象为
③实验进行一段时间后,可观察到装置Ⅳ中的品红溶液褪色,下列说法正确的是
A.起漂白作用的一定是

B.反应结束后,装置Ⅳ中溶液的
 小于7
小于7C.装置Ⅳ可能观察到
 生成速率的快慢
生成速率的快慢(3)装置Ⅲ中生成硫酸盐反应的化学方程式为
您最近一年使用:0次
解题方法
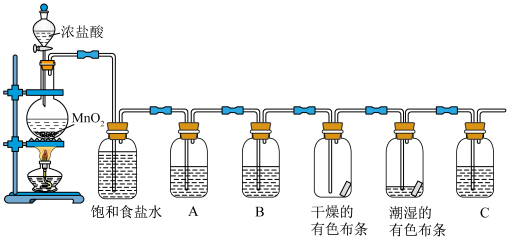
8 . 某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如图装置进行实验:
(1)圆底烧瓶中制氯气的离子方程式是__________________ 。
(2)若干燥的有色布条不褪色,潮湿的有色布条褪色,则B中盛放______ 。
(3)若A中盛放紫色石蕊溶液,则观察到现象为________________ 。
(4)饱和食盐水的作用是______________ 。
(5)C装置的作用为_______________ ,发生反应的化学方程式为___________ 。
(6)用下列两种方法制取氯气①用含146g的浓盐酸与足量的二氧化锰反应②用87g二氧化锰与足量的浓盐酸反应,则所得氯气______。
(1)圆底烧瓶中制氯气的离子方程式是
(2)若干燥的有色布条不褪色,潮湿的有色布条褪色,则B中盛放
(3)若A中盛放紫色石蕊溶液,则观察到现象为
(4)饱和食盐水的作用是
(5)C装置的作用为
(6)用下列两种方法制取氯气①用含146g的浓盐酸与足量的二氧化锰反应②用87g二氧化锰与足量的浓盐酸反应,则所得氯气______。
| A.②比①多 | B.①比②多 | C.一样多 | D.无法比较 |
您最近一年使用:0次
9 . 下列说法中正确的有几项
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
| A.6项 | B.5项 | C.4项 | D.3项 |
您最近一年使用:0次











