1 . 已知 与浓盐酸在加热条件下反应可制取
与浓盐酸在加热条件下反应可制取 。工业上,向500~600℃的铁屑中通入氯气生产无水氯化铁。现用如图所示装置模拟上述过程进行实验。
。工业上,向500~600℃的铁屑中通入氯气生产无水氯化铁。现用如图所示装置模拟上述过程进行实验。
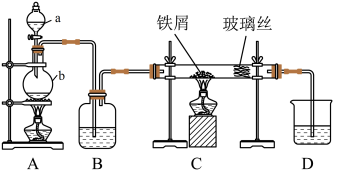
(1)写出仪器的名称:a___________ ,b___________ 。
(2)A 中反应的化学方程式为___________ ,C中反应的化学方程式为___________ 。
(3)装置B中加入的试剂是___________ 。
(4)已知:向热铁屑中通入氯化氢气体可以生产无水氯化亚铁。为防止有杂质 生成,可在装置
生成,可在装置___________ 和___________ (填字母)间增加一个盛有___________ 的洗气瓶。
(5)装置D的作用是___________ 。
 与浓盐酸在加热条件下反应可制取
与浓盐酸在加热条件下反应可制取 。工业上,向500~600℃的铁屑中通入氯气生产无水氯化铁。现用如图所示装置模拟上述过程进行实验。
。工业上,向500~600℃的铁屑中通入氯气生产无水氯化铁。现用如图所示装置模拟上述过程进行实验。
(1)写出仪器的名称:a
(2)A 中反应的化学方程式为
(3)装置B中加入的试剂是
(4)已知:向热铁屑中通入氯化氢气体可以生产无水氯化亚铁。为防止有杂质
 生成,可在装置
生成,可在装置(5)装置D的作用是
您最近一年使用:0次
解题方法
2 . 下列各组物质在反应时生成大量白烟的是
| A.氢气在氯气中燃烧 | B.金属钠在氯气中燃烧 |
| C.铁丝在氯气中燃烧 | D.铜丝在氯气中燃烧 |
您最近一年使用:0次
3 . 如图中B为开关,在A处通入氯气。打开B阀时,C中干燥红色布条颜色褪去;当关闭B阀时,C中红色布条颜色无变化。则D瓶中盛有的溶液不可能是
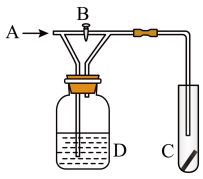

A.浓 | B.饱和NaCl溶液 | C.浓NaOH溶液 | D.浓KI溶液 |
您最近一年使用:0次
名校
4 . 实验室制备 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: 配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目_______ 。

 与
与 用作消毒剂时均被还原为
用作消毒剂时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的_______ 倍(保留小数点后2位,消毒能力可以用氧化剂转移电子数来衡量)。
 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: 配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
 与
与 用作消毒剂时均被还原为
用作消毒剂时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的
您最近一年使用:0次
名校
5 . 工业氯气通过电解饱和食盐水制得
(1)图(1)中,铁棒作_______ 极,电极反应式是_______ 。
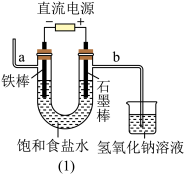
(2)检验导管b出来的气体可以用_______ ,反应的化学方程式是:_______ ;电解饱和食盐水的化学反应方程式为_______ 。
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:_______ 。
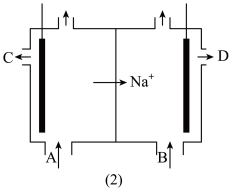
(4)下列关于图(2)的说法正确的是_______。
(5)工业上利用 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是_______ 。
A.氯气有毒 B.氯气可溶于水 C.氢气密度小
(1)图(1)中,铁棒作

(2)检验导管b出来的气体可以用
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:
(4)下列关于图(2)的说法正确的是_______。

| A.A与C、B与D溶质相同 | B.A、B通入的均为浓溶液 |
| C.理论上NaCl利用率可达100% | D.图(2)是负离子交换膜法示意图 |
(5)工业上利用
 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是A.氯气有毒 B.氯气可溶于水 C.氢气密度小
您最近一年使用:0次
名校
6 . 下列关于氯气与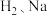 反应的叙述不正确的是
反应的叙述不正确的是
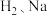 反应的叙述不正确的是
反应的叙述不正确的是| A.都有电子得失 | B.均放出热量 | C.都有白烟产生 | D.反应类型相同 |
您最近一年使用:0次
名校
解题方法
7 . 某学生设计下列实验装置利用 和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。回答下列问题:
和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。回答下列问题:
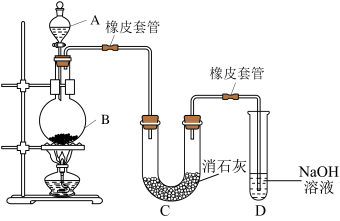
(1)写出装置B中制取氯气的化学方程式:___________ 。
(2)漂白粉在U形管中生成,实验结果所得漂白粉 产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成 ,写出该副反应的化学方程式
,写出该副反应的化学方程式___________ ,为避免发生该反应可采取的措施是___________ 。
②试判断另一个副反应是___________ (写出此反应方程式)。为避免此副反应的发生,可采取的措施是在B、C之间连接一个盛有___________ 的洗气瓶。
 和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。回答下列问题:
和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。回答下列问题:
(1)写出装置B中制取氯气的化学方程式:
(2)漂白粉在U形管中生成,实验结果所得漂白粉
 产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:①温度较高时氯气与消石灰反应生成
 ,写出该副反应的化学方程式
,写出该副反应的化学方程式②试判断另一个副反应是
您最近一年使用:0次
8 . 氯气与水的反应为 。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液,
。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液, 溶液反应。请完成下列问题:
溶液反应。请完成下列问题:
(1)向紫色石蕊溶液中滴加氯水的现象是___________ ,证明氯水中含有的微粒有___________ 。
(2)向 溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,___________ ,则证明氯水具有氧化性。
(3)氯水光照时黄绿色会逐渐变浅直至消失,并产生无色气体,请用平衡理论解释黄绿色变浅的原因:________ 。
 。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液,
。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液, 溶液反应。请完成下列问题:
溶液反应。请完成下列问题:(1)向紫色石蕊溶液中滴加氯水的现象是
(2)向
 溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,(3)氯水光照时黄绿色会逐渐变浅直至消失,并产生无色气体,请用平衡理论解释黄绿色变浅的原因:
您最近一年使用:0次
9 . 氯及其化合物在日常生活中有广泛应用。某实验小组设计多组实验,对氯气及氯的化合物的性质进行研究
I.氯气的制备与性质研究
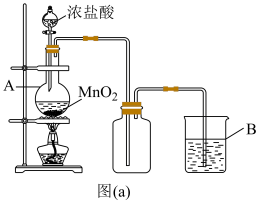
(1)实验室中常用如图(a)所示的装置制备氯气,反应的化学方程式为___________ 。
(2)图中仪器A的名称是___________ 。
(3)装置B内的溶液可以是___________ 。
(4)实验室中常用图(b)所示的装置制备氯气,并同时得到较浓的烧碱溶液。
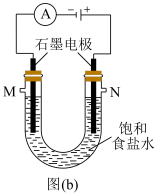
①图(b)反应的化学方程式为___________ 。
②检验制得的烧碱溶液中是否含有NaCl的实验方法是___________ 。
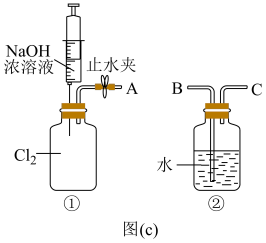
③用图(c)所示的组合装置验证氯气与烧碱溶液的反应。将A与B连接,打开止水夹,用注射器注入过量NaOH浓溶液,观察到的现象有___________ ;若其它操作不变,将A与C连接,②中观察到的现象有___________ 。
Ⅱ.次氯酸是重要的含氯化合物,应用于杀菌消毒、漂白等领域。学习小组以Cl2O为原料制备HClO。
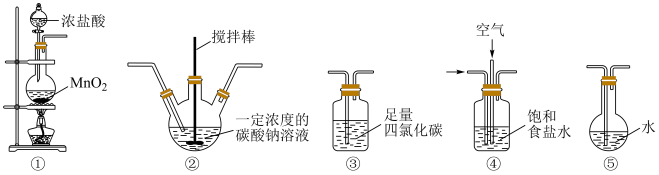
i.常温常压下Cl2O是一种黄绿色气体
ii.将氯气和空气(不参与反应)通入足量的Na2CO3溶液,发生反应生成Cl2O。
iii.Cl2O易溶于水并与水立即反应生成HClO
iv.已知:HClO+2I-+H+=I2+Cl-+H2O,I2+2 =2I-+
=2I-+
(5)装置③中的液体不可燃、不助燃也不导电,关于其用途正确的是___________。
(6)各装置的连接顺序为___________ 。
①→___________→___________→___________→___________
(7)装置②中发生的化学反应中氧化产物与还原产物的物质的量之比为___________ 。
(8)装置④的作用有___________ 。(至少写出2点)
I.氯气的制备与性质研究

(1)实验室中常用如图(a)所示的装置制备氯气,反应的化学方程式为
(2)图中仪器A的名称是
(3)装置B内的溶液可以是
(4)实验室中常用图(b)所示的装置制备氯气,并同时得到较浓的烧碱溶液。

①图(b)反应的化学方程式为
②检验制得的烧碱溶液中是否含有NaCl的实验方法是
③用图(c)所示的组合装置验证氯气与烧碱溶液的反应。将A与B连接,打开止水夹,用注射器注入过量NaOH浓溶液,观察到的现象有

Ⅱ.次氯酸是重要的含氯化合物,应用于杀菌消毒、漂白等领域。学习小组以Cl2O为原料制备HClO。

i.常温常压下Cl2O是一种黄绿色气体
ii.将氯气和空气(不参与反应)通入足量的Na2CO3溶液,发生反应生成Cl2O。
iii.Cl2O易溶于水并与水立即反应生成HClO
iv.已知:HClO+2I-+H+=I2+Cl-+H2O,I2+2
 =2I-+
=2I-+
(5)装置③中的液体不可燃、不助燃也不导电,关于其用途正确的是___________。
| A.可浮于水溶液上方——隔绝空气 | B.与水互不相溶——萃取剂 |
| C.可隔绝空气——灭火剂 | D.遇碘变色——指示剂 |
(6)各装置的连接顺序为
①→___________→___________→___________→___________
(7)装置②中发生的化学反应中氧化产物与还原产物的物质的量之比为
(8)装置④的作用有
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.完成下列问题
(1)下列氯化物中,既能由金属与氯气直接化合得到,也能由金属与盐酸反应制得_______
(2)用化学方法鉴别氯化氢和氯气,不能选用的是_______
(3)能一次性鉴别AgNO3、Na2CO3、NaCl三种溶液的试剂是_______
(4)下列关于含氯消毒剂的解释正确的是_______
(5)下列物质能使干燥的蓝色石蕊试纸变红又褪色的是_______
(1)氯气(2)液氯(3)新制氯水(4)盐酸(5)氯化氢气体(6)盐酸酸化的漂粉精溶液
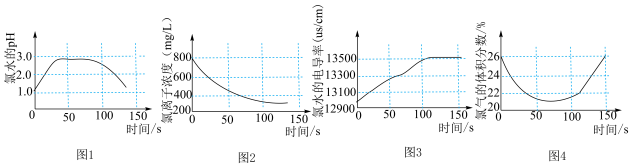
(6)某小组用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是_______
Ⅱ.某同学设计如下方案从粗食盐水中除去Ca2+、Mg2+、SO 等离子,以制得精盐水。并进行电解饱和食盐水的实验:
等离子,以制得精盐水。并进行电解饱和食盐水的实验:

(7)以下说法不正确的是_______
(8)电解饱和食盐水装置如图所示,其总反应的化学方程式为___________ 。
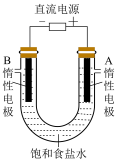
(9)向两极附近各加入酚酞溶液,___________ 极(填“A”或“B”)附近溶液变红色。A是___________ 极,检验该极产物的实验方法是___________ (必须有所用试剂或药品、现象和对应的结论)。
(1)下列氯化物中,既能由金属与氯气直接化合得到,也能由金属与盐酸反应制得_______
| A.FeCl3 | B.FeCl2 | C.CuCl2 | D.ZnCl2 |
(2)用化学方法鉴别氯化氢和氯气,不能选用的是_______
| A.湿润蓝色石蕊试纸 | B.湿润红色石蕊试纸 |
| C.湿润的淀粉KI试纸 | D.硝酸银溶液 |
(3)能一次性鉴别AgNO3、Na2CO3、NaCl三种溶液的试剂是_______
| A.盐酸 | B.NaOH溶液 | C.BaCl2溶液 | D.KNO3溶液 |
(4)下列关于含氯消毒剂的解释正确的是_______
| A.室温下,氯气通入NaOH溶液中制得漂白液:Cl2+OH-=Cl-+ClO-+H2O |
| B.氯水具有杀菌消毒作用:Cl2+H2O=HCl+HClO |
C.氯水应避光保存的原因是:2HClO H2O+Cl2↑ H2O+Cl2↑ |
| D.向Ca(ClO)2溶液中通入适量CO2可增强漂白效果:Ca(ClO)2+CO2+H2O=CaCO3+2HClO |
(5)下列物质能使干燥的蓝色石蕊试纸变红又褪色的是_______
(1)氯气(2)液氯(3)新制氯水(4)盐酸(5)氯化氢气体(6)盐酸酸化的漂粉精溶液
| A.(1)(2)(3) | B.(1)(2)(3)(6) |
| C.(3)(6) | D.(3)(4)(6) |
(6)某小组用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是_______

| A.图1表示氯水pH随时间的变化 |
| B.图2表示溶液中氯离子浓度随时间的变化 |
| C.图3表示氯水的电导率随时的变化 |
| D.图4表示液面上方氧气体积分数随时间的变化 |
Ⅱ.某同学设计如下方案从粗食盐水中除去Ca2+、Mg2+、SO
 等离子,以制得精盐水。并进行电解饱和食盐水的实验:
等离子,以制得精盐水。并进行电解饱和食盐水的实验:
(7)以下说法不正确的是_______
| A.E中主要有Mg(OH)2和BaSO4,也可能有一些Ca(OH)2 |
| B.②中加入过量Na2CO3溶液的主要目的是为了除去Ca2+ |
| C.N溶液呈碱性 |
D.③目的是除去CO 和OH- 和OH- |
(8)电解饱和食盐水装置如图所示,其总反应的化学方程式为

(9)向两极附近各加入酚酞溶液,
您最近一年使用:0次



