解题方法
1 . 根据操作及现象,下列结论中正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 将实验室制备的乙烯通入酸性KMnO4溶液中,溶液褪色 | 乙烯被酸性KMnO4溶液氧化 |
| B | 向某钠盐化合物粉末上滴加浓盐酸,将产生的气体通入品红溶液,品红溶液褪色 | 该钠盐为Na2SO3、NaHSO3或Na2S2O3中的一种 |
| C | 将氯气通入KI-淀粉溶液中,溶液先变蓝后褪色 | 氯气将生成的I2氧化 |
| D | 将浓盐酸与MnO2共热一段时间,二者均有剩余 | 该反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 某学习小组为探究 与
与 的酸性强弱开展下列实验,所用装置如图所示。回答下列问题:
的酸性强弱开展下列实验,所用装置如图所示。回答下列问题:
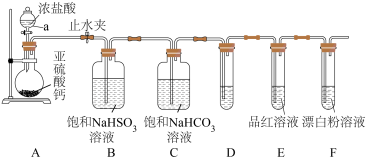
(1)仪器 的名称为
的名称为_____ 。
(2)装置 的作用是
的作用是_____ 。
(3)装置D中盛放的试剂是_____ (填“酸性 溶液”“
溶液”“ 溶液”或“
溶液”或“ 溶液”),该装置的作用是
溶液”),该装置的作用是_____ ,发生反应的离子方程式为_____ 。
(4)通过装置E、F中的现象:_____ 可证明 的酸性强于
的酸性强于 ,用
,用 试纸测定等浓度的
试纸测定等浓度的 溶液和
溶液和 溶液的
溶液的 ,
,_____ (填“能”或“不能”)判断 与
与 的酸性强弱。
的酸性强弱。
(5)由石灰乳与 反应制备漂白粉,发生反应的化学方程式为
反应制备漂白粉,发生反应的化学方程式为_____ ,若标准状况下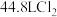 制得了
制得了 漂白粉,则漂白粉的产率为
漂白粉,则漂白粉的产率为_____  (保留两位有效数字)。
(保留两位有效数字)。
 与
与 的酸性强弱开展下列实验,所用装置如图所示。回答下列问题:
的酸性强弱开展下列实验,所用装置如图所示。回答下列问题:
(1)仪器
 的名称为
的名称为(2)装置
 的作用是
的作用是(3)装置D中盛放的试剂是
 溶液”“
溶液”“ 溶液”或“
溶液”或“ 溶液”),该装置的作用是
溶液”),该装置的作用是(4)通过装置E、F中的现象:
 的酸性强于
的酸性强于 ,用
,用 试纸测定等浓度的
试纸测定等浓度的 溶液和
溶液和 溶液的
溶液的 ,
, 与
与 的酸性强弱。
的酸性强弱。(5)由石灰乳与
 反应制备漂白粉,发生反应的化学方程式为
反应制备漂白粉,发生反应的化学方程式为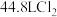 制得了
制得了 漂白粉,则漂白粉的产率为
漂白粉,则漂白粉的产率为 (保留两位有效数字)。
(保留两位有效数字)。
您最近一年使用:0次
2023-09-04更新
|
114次组卷
|
2卷引用:山西省部分学校2023-2024学年高三第一联考(月考)化学试题
解题方法
3 . 下列实验现象及所对应的离子方程式书写错误的是
A.收集酸雨并放置后 减小: 减小: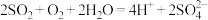 |
B.澄清石灰水放置过程中水面会出现结晶膜: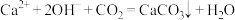 |
C.向 溶液中滴加几滴新制氯水得到黄色溶液: 溶液中滴加几滴新制氯水得到黄色溶液: |
D.盛放 的玻璃试剂瓶不能使用玻璃塞: 的玻璃试剂瓶不能使用玻璃塞: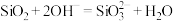 |
您最近一年使用:0次
21-22高一上·江西南昌·期末
4 . 水是一种重要的资源,图中和水相连的物质都能和水反应,下列说法正确的是
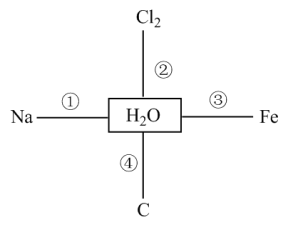

| A.①反应,1molNa与足量水反应,放出11.2L氢气 |
B.②反应, 与足量水反应,转移2mol电子 与足量水反应,转移2mol电子 |
C.③反应,生成 和 和 |
| D.④反应,水为还原剂 |
您最近一年使用:0次
21-22高一上·江苏无锡·期中
名校
5 . 下列物质的转化能一步实现的是
①Na→Na2O2→NaOH→Na2CO3→NaCl→Na
②Cu→CuO→Cu(OH)2→CuSO4→FeSO4→Fe
③Fe→FeCl2→FeCl3→Fe(OH)3→Fe2O3→Fe
④Cl2→NaClO→NaHCO3→BaCO3→BaCl2→HCl
⑤NaCl(饱和溶液)→NaHCO3→Na2CO3→NaOH→NaCl
①Na→Na2O2→NaOH→Na2CO3→NaCl→Na
②Cu→CuO→Cu(OH)2→CuSO4→FeSO4→Fe
③Fe→FeCl2→FeCl3→Fe(OH)3→Fe2O3→Fe
④Cl2→NaClO→NaHCO3→BaCO3→BaCl2→HCl
⑤NaCl(饱和溶液)→NaHCO3→Na2CO3→NaOH→NaCl
| A.①③④⑤ | B.①②③④ | C.②③④⑤ | D.①②④⑤ |
您最近一年使用:0次
2021-12-18更新
|
357次组卷
|
4卷引用:第二次月考测评卷-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
(已下线)第二次月考测评卷-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)湖北省襄阳市第四中学2022-2023学年高一上学期月考化学试题江苏省宜兴中学2021-2022学年高一上学期期中考试化学试题吉林省吉林市第二中学2022-2023学年高一上学期1月期末考试化学试题
解题方法
6 . 下列过程中的化学反应,相应的离子方程式正确的是
| A.“84消毒液”与洁厕灵(主要成分为浓盐酸)混用:ClO-+Cl-+2H+=Cl2↑+H2O |
B.工业上利用“侯氏制碱法”生产纯碱:CO2+2NH3+H2O+2Na+=Na2CO3↓+2NH |
C.向Ba(OH)2溶液中滴加少量NaHCO3溶液:Ba2++2OH-+2HCO =BaCO3↓+CO =BaCO3↓+CO +2H2O +2H2O |
D.KMnO4酸性溶液与H2C2O4溶液混合:2MnO +5C2O +5C2O +16H+=2Mn2++10CO2↑+8H2O +16H+=2Mn2++10CO2↑+8H2O |
您最近一年使用:0次
解题方法
7 . 高铁酸钾(K2FeO4)是一种高效、多功能的新型非氯绿色消毒剂,主要用于饮水处理,化工生产中作磺酸、亚硝酸盐、亚铁氰化物和其他无机物的氧化剂。某实验小组利用如图装置和药品制备高铁酸钾并探究其性质。
已知:K2FeO4为紫色固体,具有强氧化性,易溶于水、微溶于浓碱溶液、不溶于乙醇,在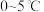 的强碱性溶液中较稳定。
的强碱性溶液中较稳定。
(1)制备 K2FeO4 (部分夹持装置略)
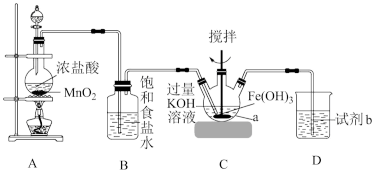
①仪器a的名称是___________ 。
②装置A为实验室制取氯气的装置,装置A中发生反应的离子方程式为___________ 。
③在搅拌下,将 通入含
通入含 的悬浊液(含
的悬浊液(含 )中即可制取K2FeO4,写出该反应的化学方程式:
)中即可制取K2FeO4,写出该反应的化学方程式:___________ 。
④在下列试剂中,试剂b的最佳选择是___________ (填标号)。
A.氢氧化钠溶液 B.澄清石灰水 C.浓硫酸 D.浓氨水
(2)制备的高铁酸钾粗产品中含有氢氧化钾、氯化钾、氢氧化铁等杂质,请完成提纯高铁酸钾的实验设计(实验药品:蒸馏水、乙醇、饱和 溶液、饱和
溶液、饱和 溶液、冷的
溶液、冷的 稀溶液)。
稀溶液)。
提纯高铁酸钾的实验步骤:①取一定量的高铁酸钾粗产品,溶于___________ 中;
②过滤除去___________ (填化学式),取滤液将其置于冰水浴中,向滤液中加入饱和 溶液;
溶液;
③搅拌、静置、过滤,用___________ 洗涤2~3次;④在真空干燥箱中干燥。
(3) K2FeO4性质探究
①取少量提纯后的晶体于烧杯中,加入足量 溶液,使固体完全溶解。往溶解后的溶液中加入稀盐酸,有黄绿色气体单质生成,该反应中被氧化的是
溶液,使固体完全溶解。往溶解后的溶液中加入稀盐酸,有黄绿色气体单质生成,该反应中被氧化的是___________ (填化学式)。
②根据 的制备实验得出氧化性:
的制备实验得出氧化性:
___________ (填“>”或“<”) ,而步骤①中实验表明,
,而步骤①中实验表明, 和
和 的氧化性强弱关系与之相反,原因是
的氧化性强弱关系与之相反,原因是___________ 。
③ 时,
时,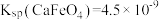 ,若要使
,若要使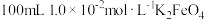 溶液中的
溶液中的 完全沉淀[
完全沉淀[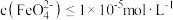 视为沉淀完全],理论上要加入
视为沉淀完全],理论上要加入 的
的
___________  (忽略溶液体积变化)。
(忽略溶液体积变化)。
已知:K2FeO4为紫色固体,具有强氧化性,易溶于水、微溶于浓碱溶液、不溶于乙醇,在
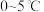 的强碱性溶液中较稳定。
的强碱性溶液中较稳定。(1)制备 K2FeO4 (部分夹持装置略)

①仪器a的名称是
②装置A为实验室制取氯气的装置,装置A中发生反应的离子方程式为
③在搅拌下,将
 通入含
通入含 的悬浊液(含
的悬浊液(含 )中即可制取K2FeO4,写出该反应的化学方程式:
)中即可制取K2FeO4,写出该反应的化学方程式:④在下列试剂中,试剂b的最佳选择是
A.氢氧化钠溶液 B.澄清石灰水 C.浓硫酸 D.浓氨水
(2)制备的高铁酸钾粗产品中含有氢氧化钾、氯化钾、氢氧化铁等杂质,请完成提纯高铁酸钾的实验设计(实验药品:蒸馏水、乙醇、饱和
 溶液、饱和
溶液、饱和 溶液、冷的
溶液、冷的 稀溶液)。
稀溶液)。提纯高铁酸钾的实验步骤:①取一定量的高铁酸钾粗产品,溶于
②过滤除去
 溶液;
溶液;③搅拌、静置、过滤,用
(3) K2FeO4性质探究
①取少量提纯后的晶体于烧杯中,加入足量
 溶液,使固体完全溶解。往溶解后的溶液中加入稀盐酸,有黄绿色气体单质生成,该反应中被氧化的是
溶液,使固体完全溶解。往溶解后的溶液中加入稀盐酸,有黄绿色气体单质生成,该反应中被氧化的是②根据
 的制备实验得出氧化性:
的制备实验得出氧化性:
 ,而步骤①中实验表明,
,而步骤①中实验表明, 和
和 的氧化性强弱关系与之相反,原因是
的氧化性强弱关系与之相反,原因是③
 时,
时,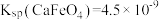 ,若要使
,若要使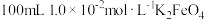 溶液中的
溶液中的 完全沉淀[
完全沉淀[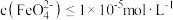 视为沉淀完全],理论上要加入
视为沉淀完全],理论上要加入 的
的
 (忽略溶液体积变化)。
(忽略溶液体积变化)。
您最近一年使用:0次
20-21高三上·全国·阶段练习
名校
8 . 根据Cl2通入不同溶液中的实验现象,所得结论正确的是
| 溶液 | 现象 | 结论 | |
| A | 含KSCN的FeBr2溶液 | 溶液立即变红色 | 还原性:Br−>Fe2+ |
| B | H2S溶液 | 产生淡黄色浑浊 | Cl2有氧化性 |
| C | 含淀粉的碘水 | 溶液的蓝色褪去 | Cl2有漂白性 |
| D | Na2SiO3溶液 | 产生胶状沉淀 | 非金属性:Cl>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列离子方程式书写正确的是
| A.氯气溶于水生成具有漂白性的物质:Cl2+H2O=H++Cl-+HClO |
| B.向沸水中滴入饱和FeCl3溶液,继续煮沸至液体显红褐色:Fe3++3H2O=Fe(OH)3↓+3H+ |
| C.用CH3COOH溶解CaCO3:CaCO3 + 2H+ =Ca2+ + CO2↑+ H2O |
D.NaHCO3溶液中加少量Ba(OH)2溶液:Ba2++ HCO +OH-=BaCO3↓+H2O +OH-=BaCO3↓+H2O |
您最近一年使用:0次
2021-01-08更新
|
408次组卷
|
4卷引用:港澳台部分学校2021-2022学年上学期高三12月月考化学试题
10 . 在给定条件下,下列所示物质间的转化均能一步实现的是
A.HCl(aq) Cl2(g) Cl2(g) FeCl2(s) FeCl2(s) |
B.Fe(s)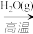 Fe2O3(s) Fe2O3(s)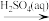 Fe2(SO4)3(aq) Fe2(SO4)3(aq) |
C.SiO2 Si Si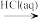 SiCl4 SiCl4 |
D.N2 NH3 NH3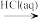 NH4Cl(aq) NH4Cl(aq) |
您最近一年使用:0次
2020-10-20更新
|
190次组卷
|
2卷引用:“皖豫名校联盟体”2021届高三上学期第一次考试化学试题



