名校
解题方法
1 . 如图所示是一个制取 并以
并以 为原料进行特定反应的装置,多余的
为原料进行特定反应的装置,多余的 可以贮存在
可以贮存在 瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。
瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。 烧瓶中的固体为
烧瓶中的固体为 ,液体为浓盐酸,则其发生反应的化学方程式为
,液体为浓盐酸,则其发生反应的化学方程式为___________
(2) 中的现象为
中的现象为___________ ,发生反应的离子方程式___________ 。
(3)装置 中硬质玻璃管内盛有炭粉,若
中硬质玻璃管内盛有炭粉,若 中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出
中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出 中反应的化学方程式:
中反应的化学方程式:___________ 。
(4)D中溶液的存在微粒有___________ (填化学式)。
(5)在F中紫色石蕊试液的颜色变化是___________ 。
(6)G中应盛放___________ 溶液。
 并以
并以 为原料进行特定反应的装置,多余的
为原料进行特定反应的装置,多余的 可以贮存在
可以贮存在 瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。
瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。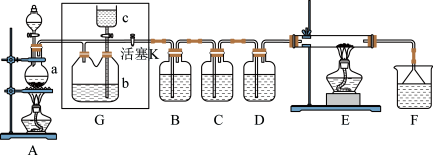
 烧瓶中的固体为
烧瓶中的固体为 ,液体为浓盐酸,则其发生反应的化学方程式为
,液体为浓盐酸,则其发生反应的化学方程式为(2)
 中的现象为
中的现象为(3)装置
 中硬质玻璃管内盛有炭粉,若
中硬质玻璃管内盛有炭粉,若 中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出
中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出 中反应的化学方程式:
中反应的化学方程式:(4)D中溶液的存在微粒有
(5)在F中紫色石蕊试液的颜色变化是
(6)G中应盛放
您最近一年使用:0次
名校
解题方法
2 . 下列装置或仪器用于相应实验合理的是
|
|
| A.钠的燃烧 | B.收集 气体 气体 |
|
|
| C.验证氯气的漂白性 | D.排盛 溶液滴定管尖嘴内气泡 溶液滴定管尖嘴内气泡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 为除去括号内的杂质,所选用的试剂或方法正确的是
| A.CO2(HCl):将混合气体通过足量的饱和碳酸钠溶液 |
| B.Na2CO3固体粉末(NaHCO3):加热到固体质量不再减轻为止 |
| C.NaHCO3溶液(Na2CO3):向溶液中加入过量Ca(OH)2溶液,过滤 |
| D.Cl2(HCl):将混合气体通过浓硫酸 |
您最近一年使用:0次
2024-04-07更新
|
69次组卷
|
2卷引用:江西省宜春市丰城市第九中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
4 . 某小组用下列装置制备 并探究其部分性质,下列说法错误的是
并探究其部分性质,下列说法错误的是
 并探究其部分性质,下列说法错误的是
并探究其部分性质,下列说法错误的是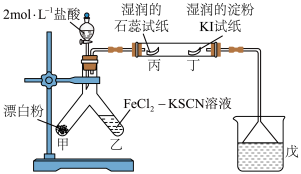
A.漂白粉的主要成分为 和 和 |
B.一段时间后,乙处溶液会变红,丁处湿润的淀粉 试纸会变蓝 试纸会变蓝 |
| C.实验过程中,能观察到丙处湿润的石蕊试纸先变蓝后褪色的现象 |
D.戊处的溶液为 浓溶液,用于吸收尾气中的 浓溶液,用于吸收尾气中的 |
您最近一年使用:0次
2024-03-28更新
|
100次组卷
|
2卷引用:江西省部分地区2023-2024学年高一下学期3月月考化学试题
名校
5 . 下列实验装置安全环保且能达到实验目的的是


| 选项 | A | B | C | D |
| 装置 | ① | ② | ③ | ④ |
| 试剂 | Cl2和H2的混合气体 | 还原铁粉、肥皂泡 | 蒸馏水 | 浓盐酸、KMnO4 |
| 目的 | 验证氢气和氯气的反应 | 进行还原铁粉与水蒸气的反应 | 配制一定物质的量浓度的溶液时,定容 | 实验室制备少量干燥的Cl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列实验现象描述错误的是
| A.硫酸钠溶液与氯化钡溶液反应,生成白色沉淀 |
| B.把一块绿豆大的金属钠放入盛水的烧杯中,观察到钠有浮、游、熔、响等现象 |
| C.纯净的氢气在氯气中燃烧,发出苍白色火焰集气瓶口处呈现雾状 |
| D.将水滴入盛有过氧化钠固体的试管中,立即把带火星的木条伸人该试管中,发出尖锐的爆鸣声 |
您最近一年使用:0次
名校
7 . 下列叙述正确的是
| A.燃烧一定是氧化还原反应 |
| B.高铁酸钠(Na2FeO4)具有强还原性 |
| C.使用自来水(氯气消毒)配制碳酸氢钠溶液 |
D.检验Cl-时,先使用盐酸酸化,防止 等离子的干扰 等离子的干扰 |
您最近一年使用:0次
名校
8 . 关于物质的相关用途,下列说法错误的是
| A.氧化铝可用于耐火材料 | B.通常状况下液氯可以用钢瓶储存运输 |
| C.金属钠着火时,可用泡沫灭火器灭火 | D.配制 溶液时加入少量的铁粉 溶液时加入少量的铁粉 |
您最近一年使用:0次
名校
9 . 某学习小组设计了如下实验,探究浓度和温度对反应的影响。
实验探究Ⅰ:
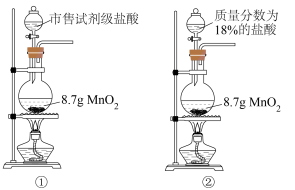
已知市售试剂级盐酸的密度为1.19g/mL,质量分数为37%;质量分数低于20%的盐酸为稀盐酸。
(1)装置①②同时加热,①中生成黄绿色气体,②中无明显变化,请从浓度和还原性的角度简要解释其原因:___________ ;①中发生反应的离子方程式为___________ ;8.7gMnO2与33.1mL市售试剂级盐酸在加热条件下反应,生成氯气的物质的量是否为0.1mol?______ (填“是"或“否),并简述其原因:___________ 。
实验探究Ⅱ:
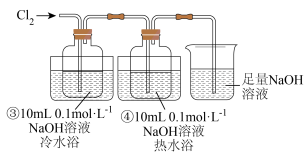
(2)通入氯气后,取出2mL装置③反应瓶中无色液体置于试管中,滴加2滴紫色石蕊溶液,溶液变蓝后褪色,请用简要的语言叙述其原因:___________ 。
(3)装置④中氧化产物和还原产物的物质的量之比为1:5,写出该反应的离子方程式并用双线桥表示电子转移的方向和数目:___________ 。
(4)装置③中所得溶液称之为“84”消毒液,其不能与洁厕灵(含盐酸)同时使用的原因为___________ (用离子方程式解释)。
实验探究Ⅰ:

已知市售试剂级盐酸的密度为1.19g/mL,质量分数为37%;质量分数低于20%的盐酸为稀盐酸。
(1)装置①②同时加热,①中生成黄绿色气体,②中无明显变化,请从浓度和还原性的角度简要解释其原因:
实验探究Ⅱ:

(2)通入氯气后,取出2mL装置③反应瓶中无色液体置于试管中,滴加2滴紫色石蕊溶液,溶液变蓝后褪色,请用简要的语言叙述其原因:
(3)装置④中氧化产物和还原产物的物质的量之比为1:5,写出该反应的离子方程式并用双线桥表示电子转移的方向和数目:
(4)装置③中所得溶液称之为“84”消毒液,其不能与洁厕灵(含盐酸)同时使用的原因为
您最近一年使用:0次
10 . 微型实验可节约药品,因而在中学化学教学中应用广泛。下图为实验室制备 并探究
并探究 是否具有漂白性的实验。下列说法正确的是
是否具有漂白性的实验。下列说法正确的是 (浓)
(浓)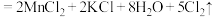 。
。
②白色干棉花球中有 粉末,主要作用是干燥气体。
粉末,主要作用是干燥气体。
 并探究
并探究 是否具有漂白性的实验。下列说法正确的是
是否具有漂白性的实验。下列说法正确的是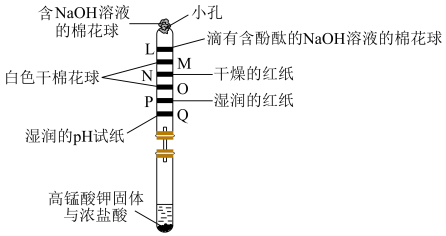
 (浓)
(浓)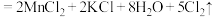 。
。②白色干棉花球中有
 粉末,主要作用是干燥气体。
粉末,主要作用是干燥气体。| A.Q处pH试纸变红且颜色一直保持不变 | B.P处红纸逐渐褪色,表明氯气具有漂白性 |
| C.N处红纸不变色 | D.向褪色后的L处棉花球滴入盐酸,红色重现 |
您最近一年使用:0次
2024-01-18更新
|
222次组卷
|
3卷引用:江西省宜春市宜丰中学2023-2024学年高一上学期1月月考化学试题