名校
1 . 下列物质的制备方法合理的是
A.将 通入澄清石灰水中制备漂白粉 通入澄清石灰水中制备漂白粉 |
B.将饱和 溶液滴入NaOH溶液中制备 溶液滴入NaOH溶液中制备 胶体 胶体 |
C.将浓盐酸滴入固体 中制备 中制备 |
D.将 和 和 混合点燃制备HCl 混合点燃制备HCl |
您最近半年使用:0次
2 . 下列物质的性质与用途具有对应关系的是
A. 能溶于水,可用于工业制盐酸 能溶于水,可用于工业制盐酸 | B.S有氧化性,可用于生产 |
C. 具有还原性,可用于废水脱氯( 具有还原性,可用于废水脱氯( ) ) | D. 受热易分解,可用于制抗酸药物 受热易分解,可用于制抗酸药物 |
您最近半年使用:0次
名校
解题方法
3 . 某同学用如图装置进行有关Cl2的实验。下列说法不正确的是

| A.I图中:鲜花褪色不能证明氯气有漂白作用 |
| B.Ⅱ图中:除去氯气中的少量HCl,试剂X可选用饱和食盐水 |
| C.Ⅲ图中:氢气在氯气中剧烈燃烧,产生白烟 |
| D.IV图中:铁丝在氯气中燃烧生成氯化铁 |
您最近半年使用:0次
名校
4 . 根据事物的某些相似性质进行类比推理是我们经常使用的一种思维方法。以下类推正确的是
| 选项 | 实际事实 | 类推 |
| A | 硫酸、硝酸都含有氧元素 | 酸中都含有氧元素 |
| B |  是碱性氧化物 是碱性氧化物 |  也是碱性氧化物 也是碱性氧化物 |
| C |  在 在 中燃烧生成水并放热 中燃烧生成水并放热 |  在 在 中也能燃烧生成HCl并放热 中也能燃烧生成HCl并放热 |
| D | 实验室可用 和浓盐酸加热反应制 和浓盐酸加热反应制 | 实验室也可用 和稀盐酸加热反应制 和稀盐酸加热反应制 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 以下两种物质在一定条件下能通过一步反应实现相互转化的是
①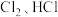 ②
②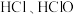 ③
③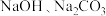 ④
④
①
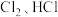 ②
②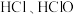 ③
③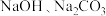 ④
④
| A.①② | B.③④ | C.②④ | D.①②③④ |
您最近半年使用:0次
名校
解题方法
6 . 下列说法正确的是
| A.Na着火用CO2灭火 |
| B.氢气在氯气中安静燃烧,发出苍白色火焰,生成白色烟雾 |
| C.新制氯水保存在盖有玻璃塞的棕色细口瓶中 |
| D.可用澄清石灰水鉴别碳酸钠和碳酸氢钠溶液 |
您最近半年使用:0次
2023-12-19更新
|
60次组卷
|
2卷引用:山东省实验中学2023-2024学年高一上学期11月期中考试化学试题
名校
解题方法
7 . NaCl是一种重要的化工原料,利用其制备烧碱和HCl的原理如图所示,下列说法错误的是
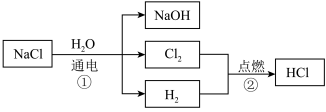

A.反应①的化学方程式为 |
| B.反应①中的氧化产物和还原产物的质量比为2:71 |
| C.反应①②均属于氧化还原反应 |
| D.纯净的H2能在Cl2中安静地燃烧,发出苍白色火焰 |
您最近半年使用:0次
2023-12-18更新
|
138次组卷
|
2卷引用:河南省部分名校2023-2024学年高一上学期11月期中考试化学试题
解题方法
8 . 下列物质不能一步实现如图转化的是
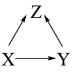
选项 | X | Y | Z |
A | C |
|
|
B |
|
|
|
C |
|
|
|
D |
|
|
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-12-16更新
|
55次组卷
|
2卷引用:广东省部分名校2023-2024学年高一上学期联合质量监测化学试卷
名校
9 . 下图是化学实验室浓盐酸试剂标签上的部分内容。
(1)写出工业上制 的化学方程式
的化学方程式___________ ,在实验室中进行该反应,现象是___________ 。
(2)该盐酸的物质的量浓度为___________ 。
(3)同学计划用该浓盐酸配制 的稀盐酸,现实验需要稀盐酸
的稀盐酸,现实验需要稀盐酸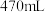 ,可供选用的仪器有:A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E.玻璃棒。
,可供选用的仪器有:A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E.玻璃棒。
①配制稀盐酸时,选择的仪器有:___________ (填序号),还缺少的仪器有___________ 。
②经计算,配制 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为___________  。
。
③测定所配制的稀盐酸,发现其浓度大于 ,引起误差的原因可能是
,引起误差的原因可能是___________ (填序号)。
A.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
B.转移溶液后,未洗涤烧杯和玻璃棒
C.定容时俯视容量瓶刻度线
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
| 盐酸 分子式:  相对分子质量:36.5 密度约   的质量分数:36.5% 的质量分数:36.5% |
 的化学方程式
的化学方程式(2)该盐酸的物质的量浓度为
(3)同学计划用该浓盐酸配制
 的稀盐酸,现实验需要稀盐酸
的稀盐酸,现实验需要稀盐酸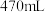 ,可供选用的仪器有:A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E.玻璃棒。
,可供选用的仪器有:A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E.玻璃棒。①配制稀盐酸时,选择的仪器有:
②经计算,配制
 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为 。
。③测定所配制的稀盐酸,发现其浓度大于
 ,引起误差的原因可能是
,引起误差的原因可能是A.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
B.转移溶液后,未洗涤烧杯和玻璃棒
C.定容时俯视容量瓶刻度线
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
您最近半年使用:0次
解题方法
10 . 以饱和食盐水为原料可以制得多种化工产品,其中部分物质的制取如图所示,水已略去,已知 为黄绿色气体,
为黄绿色气体, 气体在标准状况下的密度为
气体在标准状况下的密度为 ,
, 与
与 的反应可以用来生产漂白液,生成的
的反应可以用来生产漂白液,生成的 为漂白液的有效成分。
为漂白液的有效成分。

回答下列问题:
(1)气体 的化学式为
的化学式为___________ ;C在盛有 的集气瓶中燃烧时的现象为
的集气瓶中燃烧时的现象为___________ 。
(2)检验 中阴离子的方法为
中阴离子的方法为___________ 。
(3)标准状况下, 与足量
与足量 反应生成
反应生成 的质量为
的质量为______  。
。
(4)实验室一般用 的浓溶液配制其稀溶液,若配制
的浓溶液配制其稀溶液,若配制 的稀溶液,需用量筒量取
的稀溶液,需用量筒量取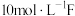 的浓溶液
的浓溶液______  。下列操作可能导致所配溶液浓度偏高的是
。下列操作可能导致所配溶液浓度偏高的是______ (填字母)。
A.量取 的浓溶液时仰视读数 B.转移前容量瓶中有水
的浓溶液时仰视读数 B.转移前容量瓶中有水
C.转移时液体溅出 D.定容时俯视读数
(5)A中金属元素的某种氧化物可以与 反应制取
反应制取 ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
 为黄绿色气体,
为黄绿色气体, 气体在标准状况下的密度为
气体在标准状况下的密度为 ,
, 与
与 的反应可以用来生产漂白液,生成的
的反应可以用来生产漂白液,生成的 为漂白液的有效成分。
为漂白液的有效成分。
回答下列问题:
(1)气体
 的化学式为
的化学式为 的集气瓶中燃烧时的现象为
的集气瓶中燃烧时的现象为(2)检验
 中阴离子的方法为
中阴离子的方法为(3)标准状况下,
 与足量
与足量 反应生成
反应生成 的质量为
的质量为 。
。(4)实验室一般用
 的浓溶液配制其稀溶液,若配制
的浓溶液配制其稀溶液,若配制 的稀溶液,需用量筒量取
的稀溶液,需用量筒量取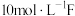 的浓溶液
的浓溶液 。下列操作可能导致所配溶液浓度偏高的是
。下列操作可能导致所配溶液浓度偏高的是A.量取
 的浓溶液时仰视读数 B.转移前容量瓶中有水
的浓溶液时仰视读数 B.转移前容量瓶中有水C.转移时液体溅出 D.定容时俯视读数
(5)A中金属元素的某种氧化物可以与
 反应制取
反应制取 ,写出该反应的化学方程式:
,写出该反应的化学方程式:
您最近半年使用:0次








