名校
解题方法
1 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)通过学习,我们掌握了胶体的知识,请完成下列问题:
①鉴别胶体和溶液的方法(只需写出方法名称,不用展开写)___________ ;
②请写出实验室制备氢氧化铁胶体的化学方程式为___________ 。
(2)写出下列物质在溶液中的电离方程式:Al2(SO4)3________ ,NaHCO3________ 。
(3)无色气体A在一种黄绿色气体B中可安静地燃烧,发出苍白色火焰,反应生成气体C,推断出各种物质后,回答下列问题:
①写出反应的化学方程式___________ 。
②1g物质A中含有的分子数约为___________ 。
(1)通过学习,我们掌握了胶体的知识,请完成下列问题:
①鉴别胶体和溶液的方法(只需写出方法名称,不用展开写)
②请写出实验室制备氢氧化铁胶体的化学方程式为
(2)写出下列物质在溶液中的电离方程式:Al2(SO4)3
(3)无色气体A在一种黄绿色气体B中可安静地燃烧,发出苍白色火焰,反应生成气体C,推断出各种物质后,回答下列问题:
①写出反应的化学方程式
②1g物质A中含有的分子数约为
您最近半年使用:0次
解题方法
2 . 下列实验操作 及现象 、结论 均正确的是
| 实验操作及现象 | 结论 | |
| A | 加热坩埚,迅速投入绿豆大小的金属钠,近距离俯视观察到钠先熔化后出现黄色火焰,生成淡黄色固体。 |  在空气燃烧生成 在空气燃烧生成 |
| B | 取某未知含铁固体于烧杯中,再滴入 溶液,观察溶液和固体表面均无明显变化。 溶液,观察溶液和固体表面均无明显变化。 | 固体中铁元素一定无+3价 |
| C | 将点燃的 伸入盛满 伸入盛满 的集气瓶中,可观察到苍白色火焰瓶口观察到白雾 的集气瓶中,可观察到苍白色火焰瓶口观察到白雾 |  在 在 点燃可生成 点燃可生成 气体 气体 |
| D | 将 气体通入滴有酚酞的 气体通入滴有酚酞的 溶液中,观察到原红色溶液褪成无色。 溶液中,观察到原红色溶液褪成无色。 |  气体具有漂白性 气体具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
3 . 下列说法错误的是
| A.配制100g10%的NaCl溶液时,可能要用到托盘天平 |
| B.将100g20%的KOH溶液分成2等份,则每份溶液的质量分数均为20% |
| C.燃烧一定要有氧气参与反应 |
| D.有氧气参与且有电子得失的反应一定是氧化还原反应 |
您最近半年使用:0次
2023-11-15更新
|
37次组卷
|
2卷引用:河北省2023-2024学年高一上学期选科调考第二次联考化学试题
名校
4 . 下列关于氯及其化合物的说法中正确的是
| A.Cl2的化学性质非常活泼,因此不能用钢瓶贮存液氯 |
| B.新制氯水在密闭无色玻璃瓶中放置数天后酸性减弱 |
| C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有HClO |
| D.H2在Cl2中燃烧,火焰呈苍白色,工业上利用该原理生产盐酸 |
您最近半年使用:0次
名校
5 . 下列叙述中不正确的是
| A.金属钠着火时,可用泡沫灭火器来灭火 |
| B.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰 |
| C.漂白液和漂白粉都可用于棉、麻、纸张的漂白剂,二者的原理是相同的 |
| D.Na、Na2O、Na2O2、NaOH长期放置在空气中,最终都将变为Na2CO3 |
您最近半年使用:0次
解题方法
6 . 下列有关氯及其化合物说法中不正确 的是
A. 有强氧化性,可用于自来水消毒 有强氧化性,可用于自来水消毒 |
| B.常温下,氯气和铁不反应,所以可将液氯用钢瓶贮存 |
| C.红热的铁丝在氯气中剧烈燃烧,生成棕红色的烟 |
| D.氢气在氯气中燃烧产生苍白色火焰,在瓶口出现白烟 |
您最近半年使用:0次
解题方法
7 . 高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知 A、F 为非金属单质气体,B为常见金属单质,E 为生活中最常见的调味品,F 在标准状况下密度为 0.090g·L-1。

请回答下列问题:
(1)写出 D 的名称___________ ,Na2FeO4中 Fe 元素的化合价为___________ 。
(2)反应③,F 在 A 中点燃的反应现象为___________ 。
(3)写出反应④的化学方程式,并用“双线桥”表示电子转移的方向和数目:___________ 。

请回答下列问题:
(1)写出 D 的名称
(2)反应③,F 在 A 中点燃的反应现象为
(3)写出反应④的化学方程式,并用“双线桥”表示电子转移的方向和数目:
您最近半年使用:0次
名校
解题方法
8 . 下列说法正确的是
A.纯净的 在 在 中安静地燃烧,发出苍白色火焰 中安静地燃烧,发出苍白色火焰 |
B.铁丝在少量的 中燃烧可生成 中燃烧可生成 |
| C.燃烧是发光发热的剧烈的化学反应,必须有氧气参与 |
D. 在 在 中燃烧产生蓝色的烟 中燃烧产生蓝色的烟 |
您最近半年使用:0次
2023-11-08更新
|
184次组卷
|
2卷引用:天津市河西区2023-2024学年高一上学期11月期中考试化学试题
名校
解题方法
9 . 下列物质中,不能 由单质直接化合生成的是
| A.Na2O2 | B.FeCl2 | C.HCl | D.FeCl3 |
您最近半年使用:0次
10 . 以 为原料制备
为原料制备 和
和 ,并利用
,并利用 冶炼金属钛(Ti)的工艺流程如下:
冶炼金属钛(Ti)的工艺流程如下:
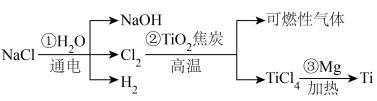
已知:高温条件下Ti的性质很活泼。
回答下列问题:
(1)在实际生产中,应避免步骤①的产物 与
与 接触发生副反应,降低
接触发生副反应,降低 纯度,解释其原因,用离子方程式表示为
纯度,解释其原因,用离子方程式表示为___________ 。
(2) 在
在 中燃烧的现象是
中燃烧的现象是___________ ,恰好完全反应后,将产物溶于水制得密度为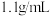 ,质量分数为
,质量分数为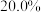 的盐酸溶液,其物质的量浓度为
的盐酸溶液,其物质的量浓度为___________ 。
(3)步骤②发生反应的化学方程式为___________ ,该反应中氧化产物与还原产物的物质的量之比为___________ 。
(4)步骤③须在稀有气体(如氩)的氛围下进行,稀有气体的作用是___________ 。
 为原料制备
为原料制备 和
和 ,并利用
,并利用 冶炼金属钛(Ti)的工艺流程如下:
冶炼金属钛(Ti)的工艺流程如下:
已知:高温条件下Ti的性质很活泼。
回答下列问题:
(1)在实际生产中,应避免步骤①的产物
 与
与 接触发生副反应,降低
接触发生副反应,降低 纯度,解释其原因,用离子方程式表示为
纯度,解释其原因,用离子方程式表示为(2)
 在
在 中燃烧的现象是
中燃烧的现象是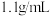 ,质量分数为
,质量分数为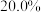 的盐酸溶液,其物质的量浓度为
的盐酸溶液,其物质的量浓度为(3)步骤②发生反应的化学方程式为
(4)步骤③须在稀有气体(如氩)的氛围下进行,稀有气体的作用是
您最近半年使用:0次



