1 . 如图是实验室用二氧化锰和浓盐酸制备氯气并进行一系列相关实验的装置(夹持装置已略)。

(1)装置A中盛装浓盐酸的仪器名称为________ ,发生反应的离子方程式为________ 。
(2)装置B中盛装的试剂为________ ,在实验过程中可以起到安全瓶的作用,一旦后续装置堵塞,B中会出现________ 现象。
(3)装置C的作用是证明干燥的 无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是________ (填字母,试剂不重复使用)。
a.干燥的石蕊试纸 b.湿润的石蕊试纸
c.碱石灰 d.无水氯化钙
(4)装置E中溶液变蓝色,证明了氯气化学性质中的________ 性;装置F中的试剂为________ 溶液(填化学式)。
(5) 也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用
也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用 和
和 制备等量的氯气,转移电子数之比为
制备等量的氯气,转移电子数之比为________ 。

(1)装置A中盛装浓盐酸的仪器名称为
(2)装置B中盛装的试剂为
(3)装置C的作用是证明干燥的
 无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是a.干燥的石蕊试纸 b.湿润的石蕊试纸
c.碱石灰 d.无水氯化钙
(4)装置E中溶液变蓝色,证明了氯气化学性质中的
(5)
 也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用
也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用 和
和 制备等量的氯气,转移电子数之比为
制备等量的氯气,转移电子数之比为
您最近一年使用:0次
名校
2 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。下列说法不正确的是


| A.A→C需要加入氧化剂 |
B.将 通入C的钠盐溶液中,其离子方程式为: 通入C的钠盐溶液中,其离子方程式为: |
| C.由A制备消毒液需要控制温度 |
D. 的消毒效率是 的消毒效率是 的2倍还原产物都是 的2倍还原产物都是 ,消毒效率以单位物质的量的物质得到的电子数表示) ,消毒效率以单位物质的量的物质得到的电子数表示) |
您最近一年使用:0次
解题方法
3 . 下列反应的离子方程式书写正确的是
A.向铜片上滴加 溶液: 溶液: |
B.将 通入石灰乳中制漂白粉: 通入石灰乳中制漂白粉: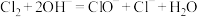 |
C.苯甲醛与新制的 共热: 共热: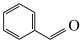 +2Cu(OH)2+OH- +2Cu(OH)2+OH- 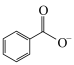 +Cu2O↓+2H2O +Cu2O↓+2H2O |
D.苯酚钠溶液中通入少量的 气体: 气体: +CO2+H2O→ +CO2+H2O→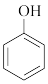 +HCO +HCO |
您最近一年使用:0次
4 . 宏观辨识与微观探析是化学核心素养之一,下列有关方程式与所述事实相符合的是
A.电解熔融 制取Mg: 制取Mg: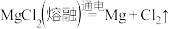 |
B.实验室制氨气: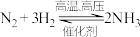 |
C.工业制漂白粉: |
D.过量的铁粉在 中燃烧: 中燃烧: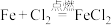 |
您最近一年使用:0次
名校
解题方法
5 .  是原子序数依次增大的短周期主族元素,X与Z同主族,Z的最高正价与最低负价之和为4,Y在同周期中半径最大,下列说法正确的是
是原子序数依次增大的短周期主族元素,X与Z同主族,Z的最高正价与最低负价之和为4,Y在同周期中半径最大,下列说法正确的是
 是原子序数依次增大的短周期主族元素,X与Z同主族,Z的最高正价与最低负价之和为4,Y在同周期中半径最大,下列说法正确的是
是原子序数依次增大的短周期主族元素,X与Z同主族,Z的最高正价与最低负价之和为4,Y在同周期中半径最大,下列说法正确的是A.简单氢化物沸点: | B.最高价氧化物对应的水化物的酸性: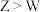 |
| C.X与Y形成的化合物中只有离子键 | D.W的单质可用于制备漂白液 |
您最近一年使用:0次
名校
解题方法
6 . 下列反应的离子方程式正确的是
A.常温下用 稀溶液吸收 稀溶液吸收 : :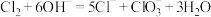 |
B.向浓氨水中滴加少量硝酸银溶液: |
C.三氧化硫与氢氧化钡溶液反应: |
D.用酸性高锰酸钾标准溶液滴定草酸: |
您最近一年使用:0次
7 . 实验室利用以下反应可以快速制取少量氯气: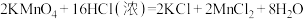
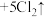 ,关于该反应的说法正确的是
,关于该反应的说法正确的是
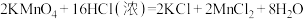
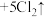 ,关于该反应的说法正确的是
,关于该反应的说法正确的是| A.由该反应判断氧化性:KMnO4>Cl2 |
| B.氧化剂与还原剂的物质的量之比为1:8 |
| C.可以用饱和NaHCO3溶液除去Cl2中混有的HCl |
| D.1 mol Cl2与足量的NaOH溶液充分反应制备“84”消毒液,转移电子的物质的量为2 mol |
您最近一年使用:0次
解题方法
8 . 下列离子方程式书写正确 的是
| A.Zn和稀硝酸反应:Zn+2H+=Zn2++H2↑ |
B.Si与NaOH溶液反应:Si+2OH-+H2O=SiO +2H2↑ +2H2↑ |
| C.Cl2通入热的NaOH溶液中:Cl2+2OH-=ClO-+Cl- |
| D.Na投入到CuSO4溶液中:2Na+Cu2+=2Na++Cu |
您最近一年使用:0次
2024-02-24更新
|
298次组卷
|
2卷引用:贵州省黔西南州金成实验学校2022-2023学年高一下学期期末质量检测化学试卷
名校
9 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。

已知: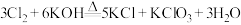
回答下列问题:
(1)盛装浓盐酸的仪器名称为________ 。 的作用
的作用________ 。
(2)b中试管内发生反应的还原剂和氧化剂的物质的量之比为________ 。 中反应的离子方程式是
中反应的离子方程式是________ 。
(3)用双线桥表示该实验制备氯气的化学方程式,并标注电子转移的方向和数目________ 。
(4)将氯气持续通入紫色石蕊试液中,溶液颜色呈如图变化:
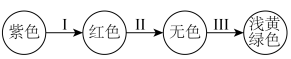
根据溶液变色情况,写出相应微粒的化学式,Ⅰ为________ 、Ⅱ为________ 、Ⅲ为________ 。
(5)某游泳池常用 来抑制藻类生长,工作人员一次错用
来抑制藻类生长,工作人员一次错用 消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了
消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了 和
和 ,写出相应的离子方程式
,写出相应的离子方程式________ 。
 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
已知:
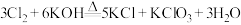
回答下列问题:
(1)盛装浓盐酸的仪器名称为
 的作用
的作用(2)b中试管内发生反应的还原剂和氧化剂的物质的量之比为
 中反应的离子方程式是
中反应的离子方程式是(3)用双线桥表示该实验制备氯气的化学方程式,并标注电子转移的方向和数目
(4)将氯气持续通入紫色石蕊试液中,溶液颜色呈如图变化:

根据溶液变色情况,写出相应微粒的化学式,Ⅰ为
(5)某游泳池常用
 来抑制藻类生长,工作人员一次错用
来抑制藻类生长,工作人员一次错用 消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了
消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了 和
和 ,写出相应的离子方程式
,写出相应的离子方程式
您最近一年使用:0次
2024-02-22更新
|
72次组卷
|
2卷引用:广西壮族自治区百色市2023-2024学年高一上学期1月期末化学试题
名校
解题方法
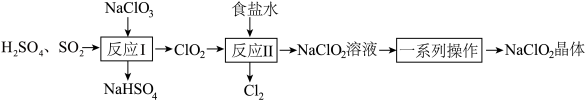
10 . NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等。已知:饱和NaClO2溶液在温度低于38℃时析出NaCO2•3H2O晶体,温度高于38℃时析出NaClO2晶体,温度高于60℃时,NaClO2分解生成NaClO3和NaCl。其生产工艺如图所示。
(1)NaClO2中氯元素的化合价为___________ 。
(2)“反应I”中氧化剂与还原剂的物质的量之比为___________ 。
(3)“反应Ⅱ”的离子方程式为___________ 。
(4)“反应”所用“食盐水”由粗盐水精制而成。精制时,为除去粗盐水中的Ca2+、Mg2+和 ,需要用到试剂:①NaOH溶液②Na2CO3溶液③BaCl2溶液④稀盐酸,所用试剂的加入顺序正确的是___________。(填标号)
,需要用到试剂:①NaOH溶液②Na2CO3溶液③BaCl2溶液④稀盐酸,所用试剂的加入顺序正确的是___________。(填标号)
(5)“一系列操作”为蒸发浓缩、趁热过滤、___________ 、干燥,其中“趁热过滤”应控制的温度范围是___________ 。
(6)“反应Ⅱ”产生的Cl2可用于制备含氯消毒剂。将Cl2通入足量NaOH溶液中,加热后得到NaCl、NaClO、NaClO3的混合液。经测定ClO-与 的物质的量浓度之比为3∶1,则Cl2与NaOH溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为
的物质的量浓度之比为3∶1,则Cl2与NaOH溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为___________ 。
(1)NaClO2中氯元素的化合价为
(2)“反应I”中氧化剂与还原剂的物质的量之比为
(3)“反应Ⅱ”的离子方程式为
(4)“反应”所用“食盐水”由粗盐水精制而成。精制时,为除去粗盐水中的Ca2+、Mg2+和
 ,需要用到试剂:①NaOH溶液②Na2CO3溶液③BaCl2溶液④稀盐酸,所用试剂的加入顺序正确的是___________。(填标号)
,需要用到试剂:①NaOH溶液②Na2CO3溶液③BaCl2溶液④稀盐酸,所用试剂的加入顺序正确的是___________。(填标号)| A.①②③④ | B.②①③④ | C.③①②④ | D.③②①④ |
(5)“一系列操作”为蒸发浓缩、趁热过滤、
(6)“反应Ⅱ”产生的Cl2可用于制备含氯消毒剂。将Cl2通入足量NaOH溶液中,加热后得到NaCl、NaClO、NaClO3的混合液。经测定ClO-与
 的物质的量浓度之比为3∶1,则Cl2与NaOH溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为
的物质的量浓度之比为3∶1,则Cl2与NaOH溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为
您最近一年使用:0次
2024-02-11更新
|
626次组卷
|
6卷引用:2024届河南省南阳市方城县第一高级中学高一上学期1月期末模拟预测化学试题



