解题方法
1 . 海水是一个巨大的化学资源宝库。回答下列问题:
(1)海水提溴工艺中,发生反应: ,该反应中氧化剂是
,该反应中氧化剂是__________ ,它在反应中__________ (填“得到”或“失去”)电子;现有 标准状况下的
标准状况下的 参加该反应,则理论上可转化
参加该反应,则理论上可转化 的物质的量是
的物质的量是_________  。
。
(2)利用化学沉淀法可以去除粗盐中的杂质离子( 等)。向某粗盐水滴加过量
等)。向某粗盐水滴加过量 溶液,有关反应的离子方程式为
溶液,有关反应的离子方程式为__________ ,滴加 溶液略微过量的目的是
溶液略微过量的目的是__________ 。
(3)在常温下,将氯气通入 溶液中,可以得到一种漂白液,上述反应的化学方程式为
溶液中,可以得到一种漂白液,上述反应的化学方程式为__________ ,该漂白液的有效成分是__________ (填名称)。
(1)海水提溴工艺中,发生反应:
 ,该反应中氧化剂是
,该反应中氧化剂是 标准状况下的
标准状况下的 参加该反应,则理论上可转化
参加该反应,则理论上可转化 的物质的量是
的物质的量是 。
。(2)利用化学沉淀法可以去除粗盐中的杂质离子(
 等)。向某粗盐水滴加过量
等)。向某粗盐水滴加过量 溶液,有关反应的离子方程式为
溶液,有关反应的离子方程式为 溶液略微过量的目的是
溶液略微过量的目的是(3)在常温下,将氯气通入
 溶液中,可以得到一种漂白液,上述反应的化学方程式为
溶液中,可以得到一种漂白液,上述反应的化学方程式为
您最近一年使用:0次
解题方法
2 . 某化学兴趣小组进行了如下实验。请回答:
(1)用一氧化碳还原氧化铁,反应的化学方程式为_______ 。反应完毕后,他们将得到的铁屑装入下图所示装置进行实验,A中的玻璃丝可以阻止固体离开A管,B中碱石灰的作用是_______ 。一段时间后,他们将A中的固体溶于水,并向所得溶液中滴入几滴KSCN溶液。
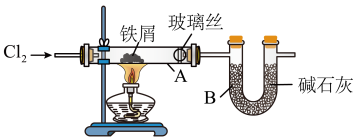
①若观察到溶液出现红色,证明溶液中含有_______ (填离子符号)。
②若未观察到溶液出现红色,可能的原因是_______ 。
(2)用足量的稀盐酸溶解一定量的Fe2O3,得到棕黄色溶液。甲同学向溶液中加入铜粉欲获得铁,他_______ (填“能”或“不能”)成功,原因是_______
(3)已知铝粉与氧化铁能发生反应2Al+Fe2O3 2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为
2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为_______ 。某同学认为用足量稀盐酸浸泡也能达到相同的结果,他的观点_______ (填“正确”或“不正确”)。
(1)用一氧化碳还原氧化铁,反应的化学方程式为

①若观察到溶液出现红色,证明溶液中含有
②若未观察到溶液出现红色,可能的原因是
(2)用足量的稀盐酸溶解一定量的Fe2O3,得到棕黄色溶液。甲同学向溶液中加入铜粉欲获得铁,他
(3)已知铝粉与氧化铁能发生反应2Al+Fe2O3
 2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为
2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为
您最近一年使用:0次
名校
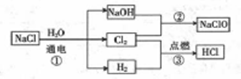
3 . 次氯酸钠(NaClO)是漂白液的主要成分,次氯酸钠溶液可用于消毒、杀菌及水处理。一种生产次氯酸钠的工艺如图所示。
-
(1)Cl 元素位于元素周期表第______ 周期___ 族。
(2)写出NaOH的电子式:__________ 。
(3)写出反应②的化学方程式:_______________ 。该反应中每生成1mol NaClO时,转移______ mol 电子。
(4)“84”消毒液( 主要成分为NaClO)和洁厕灵( 主要成分为浓盐酸)不能混在一起使用,原因是_____________________ (用离子方程式表示)。
-

(1)Cl 元素位于元素周期表第
(2)写出NaOH的电子式:
(3)写出反应②的化学方程式:
(4)“84”消毒液( 主要成分为NaClO)和洁厕灵( 主要成分为浓盐酸)不能混在一起使用,原因是
您最近一年使用:0次



