名校
1 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。如图为氯元素的“价-类”二维图。
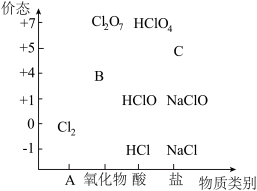
请回答下列问题:
(1)二维图中B可以代替 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是___________ (填化学式,下同);C是一种钠盐,则C是___________ 。
(2)某同学利用①FeO、② 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与________ (填序号)发生反应;从化合价角度看,盐酸中 具有
具有_________ 性,可能与(填序号)___________ 发生反应。
(3)若将84消毒液与双氧水混用给游泳池消毒,反应产生的 会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:
会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:___________ 。
(4)一定温度下, 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为___________ 。

请回答下列问题:
(1)二维图中B可以代替
 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是(2)某同学利用①FeO、②
 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与 具有
具有(3)若将84消毒液与双氧水混用给游泳池消毒,反应产生的
 会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:
会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:(4)一定温度下,
 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 写出下列反应的离子 方程式。
(1)氯气通入氢氧化钠溶液中:___________ ;
(2)冰醋酸中滴加氢氧化钾溶液:___________ ;
(3)实验室制备 :
:___________ ;
(4)氧化镁溶液中滴加氨水:___________ ;
(5)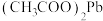 (弱电解质)溶液中滴加盐酸:
(弱电解质)溶液中滴加盐酸:___________ ;
(6)酸性高锰酸钾溶液中滴加淀粉碘化钾溶液,溶液变为蓝色:___________ 。
(1)氯气通入氢氧化钠溶液中:
(2)冰醋酸中滴加氢氧化钾溶液:
(3)实验室制备
 :
:(4)氧化镁溶液中滴加氨水:
(5)
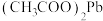 (弱电解质)溶液中滴加盐酸:
(弱电解质)溶液中滴加盐酸:(6)酸性高锰酸钾溶液中滴加淀粉碘化钾溶液,溶液变为蓝色:
您最近一年使用:0次
名校
3 . 某家用防疫用品“84消毒液”的包装说明如下,请回答下列问题:
(1)“84”消毒液可由Cl2与NaOH溶液反应制得,Cl2与NaOH溶液反应的化学方程式为___________
(2)欲将“84消毒液”原液稀释配制成450mL c(NaClO)=0.100mol·L-1的溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、___________ 、___________ 。
②配制时,需要取用___________ mL“84消毒液”原液。
③下列操作会使溶液中NaClO浓度偏低的是___________ 。
A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
(3)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到pH试纸的现象是___________
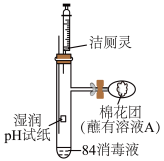
| 【产品名称】84消毒液 【有效成分】NaClO 【规格】1000mL 【物质的量浓度】4.0  注:①按一定比例稀释后使用 ②不得与酸性产品(如洁厕灵)同时使用。 |
(2)欲将“84消毒液”原液稀释配制成450mL c(NaClO)=0.100mol·L-1的溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、
②配制时,需要取用
③下列操作会使溶液中NaClO浓度偏低的是
A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
(3)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到pH试纸的现象是

您最近一年使用:0次
2023-11-11更新
|
221次组卷
|
4卷引用:福建省福州市八县一中2023-2024学年高一上学期11月期中化学试题
名校
4 . 含氧化合物具有广泛的应用,请回答下列问题。
(1) 中含有的电子数目为
中含有的电子数目为___________ 。
(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是___________ (填微粒符号,下同),Ⅱ是___________ ,Ⅲ是___________ 。
(3)氯气和氢氧化钠溶液反应可制备“84消毒液”,其化学方程式为___________ 。
(4)漂白粉漂白时,通入 可增加漂白效果,其化学方程式为
可增加漂白效果,其化学方程式为___________ 。
(5)用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,反应的现象为___________ 。
(6) 是酸性氧化物,
是酸性氧化物, 和碱反应生成
和碱反应生成 的化学方程式为
的化学方程式为___________ 。
(1)
 中含有的电子数目为
中含有的电子数目为(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是
(3)氯气和氢氧化钠溶液反应可制备“84消毒液”,其化学方程式为
(4)漂白粉漂白时,通入
 可增加漂白效果,其化学方程式为
可增加漂白效果,其化学方程式为(5)用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,反应的现象为
(6)
 是酸性氧化物,
是酸性氧化物, 和碱反应生成
和碱反应生成 的化学方程式为
的化学方程式为
您最近一年使用:0次
名校
解题方法
5 . 含氯化合物在生产生活中具有广泛的用途。氯及其化合物的“价一类”二维图如图所示,回答下列问题:
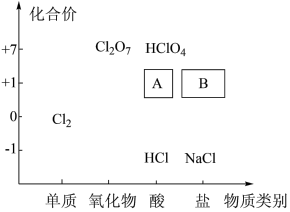
(1)自来水厂常将一定量氯气通入自来水进行消毒杀菌,用化学方程式解释为_____ ;其中具有杀菌作用的物质名称 为_____ ,实验室保存该物质的方法是将其置于_____ 试剂瓶中,_____ 保存。
(2)氯气与烧碱的反应可用于制备84消毒液,反应的化学方程式为_____ 。84消毒液的功能有_____ (填序号),其有效成分 应在“价类二维图“中的位置是_____ (选填A或B)
a.环境消毒b.器物杀菌c.织物漂白d.发酵食物
(3)某同学利用以下试剂研究HClO的性质,并进行了如下预测:
a.NaOHb.NaHCO3c.紫色石蕊试剂
从物质类别角度看,HClO具有酸性,可能与_____ 发生反应;(填标号,下同)
从化合价角度看,HClO具有氧化性,可能与_____ 发生反应;
从稳定性角度看,HClO具有不稳定性,反应的化学方程式为_____ 。
(4)漂白粉也具有和84消毒液类似的作用,漂白粉的有效成分是_____ (填化学式),漂白粉生效的化学方程式为_____ 。

(1)自来水厂常将一定量氯气通入自来水进行消毒杀菌,用化学方程式解释为
(2)氯气与烧碱的反应可用于制备84消毒液,反应的化学方程式为
a.环境消毒b.器物杀菌c.织物漂白d.发酵食物
(3)某同学利用以下试剂研究HClO的性质,并进行了如下预测:
a.NaOHb.NaHCO3c.紫色石蕊试剂
从物质类别角度看,HClO具有酸性,可能与
从化合价角度看,HClO具有氧化性,可能与
从稳定性角度看,HClO具有不稳定性,反应的化学方程式为
(4)漂白粉也具有和84消毒液类似的作用,漂白粉的有效成分是
您最近一年使用:0次
6 . 一种生产高铁酸钾的流程如图所示,写出下列反应的离子方程式
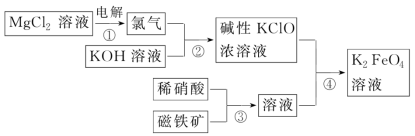
(1)反应①:_______
(2)反应②:_______
(3)反应③:_______
(4)反应④:_______

(1)反应①:
(2)反应②:
(3)反应③:
(4)反应④:
您最近一年使用:0次
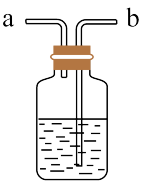
7 . 氯是一种生产生活中常见的元素,下图是几种含氯产品。

(1) 是有毒气体,为了防止多余
是有毒气体,为了防止多余 污染空气、需要如图装置进行尾气处理,用离子方程式表示该原理
污染空气、需要如图装置进行尾气处理,用离子方程式表示该原理_______ 气体应该由_______ (填a或b)管通入。若要吸收标准状况下 ,至少需要
,至少需要 上述溶液
上述溶液_______ mL。
(2)工业上制取漂白粉的化学方程式是_______ 。
(3)同学们探究“84”消毒液在不同pH不使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用 溶液将3个烧杯内溶液的pH分别调至10、7和4.(溶液体积变化忽略不计)
溶液将3个烧杯内溶液的pH分别调至10、7和4.(溶液体积变化忽略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
已知溶液中 、
、 和
和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
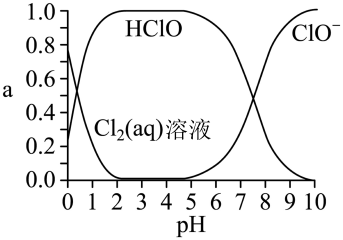
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色_______ (填“越快”或“越慢”)。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是_______ 。
③预测pH=1、10min后,红纸的颜色(与a、b、c颜色相比)_______ 。

(1)
 是有毒气体,为了防止多余
是有毒气体,为了防止多余 污染空气、需要如图装置进行尾气处理,用离子方程式表示该原理
污染空气、需要如图装置进行尾气处理,用离子方程式表示该原理 ,至少需要
,至少需要 上述溶液
上述溶液
(2)工业上制取漂白粉的化学方程式是
(3)同学们探究“84”消毒液在不同pH不使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用
 溶液将3个烧杯内溶液的pH分别调至10、7和4.(溶液体积变化忽略不计)
溶液将3个烧杯内溶液的pH分别调至10、7和4.(溶液体积变化忽略不计)步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
| 烧杯 | 溶液的pH | 现象 |
| a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
| b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
| c | 4 | 10min后,红纸颜色变得更浅;4h后红纸褪色 |
 、
、 和
和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是
③预测pH=1、10min后,红纸的颜色(与a、b、c颜色相比)
您最近一年使用:0次
2022-11-05更新
|
188次组卷
|
2卷引用:福建省厦门双十中学2022-2023学年高一上学期期中考试化学试题
名校
解题方法
8 . 按要求书写化学方程式或离子方程式。
(1)工业上用将氯气通入石灰乳中制漂白粉,相应的化学方程式为___________ 。
(2)硫酸厂附近的新收集雨水pH不断降低,相应的化学方程式为___________ 。
(3)木炭和浓硫酸混合加热产生大量的CO2和SO2,相应的化学方程式为___________ 。
(4)工业上用FeCl3溶液腐蚀铜线路板,相应的离子 方程式为___________ 。
(5)SO2能使氯水褪色,相应的离子 方程式为___________ 。
(1)工业上用将氯气通入石灰乳中制漂白粉,相应的化学方程式为
(2)硫酸厂附近的新收集雨水pH不断降低,相应的化学方程式为
(3)木炭和浓硫酸混合加热产生大量的CO2和SO2,相应的化学方程式为
(4)工业上用FeCl3溶液腐蚀铜线路板,相应的
(5)SO2能使氯水褪色,相应的
您最近一年使用:0次
名校
解题方法
9 . 将 通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
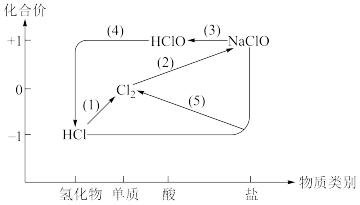
(1)实验室用二氧化锰和浓盐酸反成制备氯气,在制取Cl2的反应中,浓盐酸发生了___________ 反应
(2)制备84消毒液的化学方程式为___________ 。
(3)84消毒液中加入少量醋酸(CH3COOH)可增强效果,该反应的化学方程式为___________ 。
(4)次氯酸不稳定,光照条件下易分解。该反应的化学方程式为___________ 。
(5)84消毒液不能与洁厕剂(含盐酸)一起混合使用的原因为___________ (用离子反应方程式表示)。
 通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
(1)实验室用二氧化锰和浓盐酸反成制备氯气,在制取Cl2的反应中,浓盐酸发生了
(2)制备84消毒液的化学方程式为
(3)84消毒液中加入少量醋酸(CH3COOH)可增强效果,该反应的化学方程式为
(4)次氯酸不稳定,光照条件下易分解。该反应的化学方程式为
(5)84消毒液不能与洁厕剂(含盐酸)一起混合使用的原因为
您最近一年使用:0次
10 . 游泳池水中的氯气含量应该控制在0.5~1.0 mg·L-1之间。
(1)写出氯气溶于水的化学方程式:___________ 。溶于水后的哪种物质可杀菌消毒:___________ (写化学式)。
(2)如图显示一星期中每天19时游泳池水中的氯气含量,哪几天19时使用游泳池不安全?___________ 。
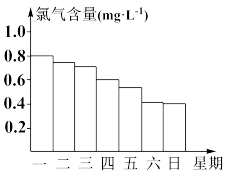
(3)你认为哪几天的天气炎热、阳光强烈?___________ ,说出一种理由___________ 。
(4)若把一片紫色的花瓣放入氯水中,可观察到的现象是___________ (花瓣所含色素性质与石蕊相似)。
(5)小型游泳池通常使用次氯酸钠溶液而非氯气给池水消毒,用化学方程式说明工业上如何生产次氯酸钠:___________ 。
(1)写出氯气溶于水的化学方程式:
(2)如图显示一星期中每天19时游泳池水中的氯气含量,哪几天19时使用游泳池不安全?

(3)你认为哪几天的天气炎热、阳光强烈?
(4)若把一片紫色的花瓣放入氯水中,可观察到的现象是
(5)小型游泳池通常使用次氯酸钠溶液而非氯气给池水消毒,用化学方程式说明工业上如何生产次氯酸钠:
您最近一年使用:0次
2021-10-26更新
|
67次组卷
|
2卷引用:福建省永安市第三中学高中校2021-2022学年高一上学期10月月考化学试题



