1 . 利用分类法可以更系统、全面的认识物质的性质以及化学反应。
Ⅰ、有下列物质:①盐酸② ③
③ ④KOH溶液⑤
④KOH溶液⑤
(1)属于碱性氧化物的是___________ (填序号)。
(2)③属于___________ (填“共价”或“离子”)化合物。
(3)属于电解质的是___________ (填序号)。
(4)①和④反应的离子方程式是___________ 。
Ⅱ、有以下四个反应:①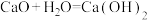 ②
②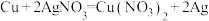
③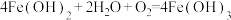 ④
④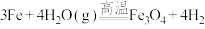
(5)不属于氧化还原反应的是___________ (填序号)。
(6)既是化合反应又是氧化还原反应的是___________ (填序号)。
Ⅲ、单质到盐的转化关系可表示为:A(单质)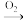 B(氧化物)
B(氧化物)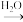 C
C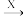 D(盐)。
D(盐)。
(7)若A是碳单质,则C的水溶液呈___________ (填“酸”、“碱”或“中”)性。
(8)若C→D的转化可用于工业制漂白粉,则物质X是___________ 。
(9)若B是一种淡黄色固体,X是 ,则B的用途是
,则B的用途是___________ (举一例),D的化学式可能是___________ 。
Ⅰ、有下列物质:①盐酸②
 ③
③ ④KOH溶液⑤
④KOH溶液⑤
(1)属于碱性氧化物的是
(2)③属于
(3)属于电解质的是
(4)①和④反应的离子方程式是
Ⅱ、有以下四个反应:①
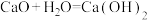 ②
②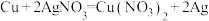
③
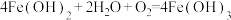 ④
④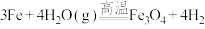
(5)不属于氧化还原反应的是
(6)既是化合反应又是氧化还原反应的是
Ⅲ、单质到盐的转化关系可表示为:A(单质)
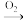 B(氧化物)
B(氧化物)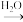 C
C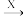 D(盐)。
D(盐)。(7)若A是碳单质,则C的水溶液呈
(8)若C→D的转化可用于工业制漂白粉,则物质X是
(9)若B是一种淡黄色固体,X是
 ,则B的用途是
,则B的用途是
您最近一年使用:0次
解题方法
2 . 新冠疫情的发生,消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,而氯气是制取消毒液的重要原料之一。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式___________________________________ ,若收集到标准状况下3.36LCl2,则被氧化的HCl的物质的量为_____________ mol。
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式_______________________________________ ,若要制取1.5L 2 mol/L的84消毒液,则需要标准状况下___________ L 氯气。
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因__________________________________ (用化学方程式表示), 该反应中氧化剂是______________ 。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因
您最近一年使用:0次
3 . 消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1) 、
、 、
、 (还原产物为
(还原产物为 )、
)、 都可以做消毒剂,都具有
都可以做消毒剂,都具有___________ 性。
(2)将紫色石蕊试液滴入氯水中现象是___________ 。
(3)漂白剂亚氯酸钠( )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为
)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为 (未配平)。在该反应中,被氧化的元素是
(未配平)。在该反应中,被氧化的元素是___________ ,13.7g 完全反应转移电子数是
完全反应转移电子数是___________ 。
(4)“84”消毒液(主要成分是NaClO),用氯气制取NaClO的离子方程式是___________ ,使用“84”消毒液时加入少量的稀硫酸效果更好,原理是___________ (用离子方程式表示)。
(1)
 、
、 、
、 (还原产物为
(还原产物为 )、
)、 都可以做消毒剂,都具有
都可以做消毒剂,都具有(2)将紫色石蕊试液滴入氯水中现象是
(3)漂白剂亚氯酸钠(
 )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为
)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为 (未配平)。在该反应中,被氧化的元素是
(未配平)。在该反应中,被氧化的元素是 完全反应转移电子数是
完全反应转移电子数是(4)“84”消毒液(主要成分是NaClO),用氯气制取NaClO的离子方程式是
您最近一年使用:0次
解题方法
4 . COVID-19在全球的蔓延,对人类的健康和全球的经济带来了很大的影响,为了控制疫情,全球进行了大面积的消杀工作,消毒液发挥了重要的作用,请回答下列有关消毒液的问题。
(1)生产消毒液是将氯气通入 溶液中,发生反应的化学方程式为
溶液中,发生反应的化学方程式为_______ 。
(2)取少量消毒液滴加酸性 溶液,现象是出现白色沉淀,说明消毒液中有
溶液,现象是出现白色沉淀,说明消毒液中有_______ (填离子符号)。
(3)消毒液稀释后喷洒在空气中,可以生成有漂白性的物质和碳酸氢钠,请写出此过程的化学方程式:_______ ;该物质有漂白性是因为它有强氧化性,但是它也很不稳定,请写出它分解的化学方程式:_______ 。
(1)生产消毒液是将氯气通入
 溶液中,发生反应的化学方程式为
溶液中,发生反应的化学方程式为(2)取少量消毒液滴加酸性
 溶液,现象是出现白色沉淀,说明消毒液中有
溶液,现象是出现白色沉淀,说明消毒液中有(3)消毒液稀释后喷洒在空气中,可以生成有漂白性的物质和碳酸氢钠,请写出此过程的化学方程式:
您最近一年使用:0次
5 . 下表是海水晒盐时,在浓缩过程中析出的盐的种类和质量(每升海水析出的各种盐的质量,单位为克)。
试回答下列问题:
(1)海水中含量较高的是氯元素、钠元素和镁元素,但从表中数据可以看出,海水晒盐时先析出的是CaSO4,其原因可能是_______ 。
(2)综合成本等因素,通常海水晒盐时,在海水密度为1.21 g·mL-1~1.22 g·mL-1之间效益最佳,此时得到的粗盐中含有杂质,含有杂质的粗盐不能直接用作化工原料,需要进行精制。精制时,加入的试剂和进行的操作为①NaOH溶液、②BaCl2溶液、③Na2CO3液、④稀盐酸、⑤过滤,⑥蒸发结晶。则加入试剂和进行的操作的顺序为_______ (填标号)。
(3)经过精制的食盐在化工上有着广泛的用途。电解饱和食盐水可制得氯气和氢氧化钠,其反应的化学方程式为2NaCl+2H2O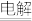 Cl2↑+H2↑+2NaOH,该反应中氧化产物与还原产物的物质的量之比为
Cl2↑+H2↑+2NaOH,该反应中氧化产物与还原产物的物质的量之比为_____ ,若将收集到的氯气通入石灰乳中,可制得漂白粉(主要成分为次氯酸钙),则工业上制漂白粉的化学方程式为_______ 。
(4)从海水中还可以提取镁、溴等。利用电解饱和食盐水得到的氯气作海水提取溴(在海水中主要以Br-形式存在)的氧化剂,则氯气作氧化剂得到溴单质反应的离子方程式为_____ 。
盐的种类 盐的质量(g) 海水的密度(g·mL-1) | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
1.13 | 0.56 | _______ | _______ | _______ | _______ |
1.20 | 0.91 | _______ | _______ | _______ | _______ |
1.21 | 0.05 | 3.26 | 0.004 | 0.008 | _______ |
1.22 | 0.015 | 9.65 | 0.01 | 0.04 | _______ |
1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
1.31 | _______ | 1.40 | 0.54 | 0.03 | 0.05 |
(1)海水中含量较高的是氯元素、钠元素和镁元素,但从表中数据可以看出,海水晒盐时先析出的是CaSO4,其原因可能是
(2)综合成本等因素,通常海水晒盐时,在海水密度为1.21 g·mL-1~1.22 g·mL-1之间效益最佳,此时得到的粗盐中含有杂质,含有杂质的粗盐不能直接用作化工原料,需要进行精制。精制时,加入的试剂和进行的操作为①NaOH溶液、②BaCl2溶液、③Na2CO3液、④稀盐酸、⑤过滤,⑥蒸发结晶。则加入试剂和进行的操作的顺序为
(3)经过精制的食盐在化工上有着广泛的用途。电解饱和食盐水可制得氯气和氢氧化钠,其反应的化学方程式为2NaCl+2H2O
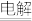 Cl2↑+H2↑+2NaOH,该反应中氧化产物与还原产物的物质的量之比为
Cl2↑+H2↑+2NaOH,该反应中氧化产物与还原产物的物质的量之比为(4)从海水中还可以提取镁、溴等。利用电解饱和食盐水得到的氯气作海水提取溴(在海水中主要以Br-形式存在)的氧化剂,则氯气作氧化剂得到溴单质反应的离子方程式为
您最近一年使用:0次
名校
6 . 氯气极其相关产品在生产生活中应用广泛。
(1)氯气属于有毒气体,贮氯罐意外泄漏时,消防员会喷洒稀氢氧化钠溶液,其作用是__________ 。(用化学方程式表示)。
实验室常用NaOH溶液吸收多余的氯气,下列也可用于吸收氯气的是_________ (填字母)。
a.NaCl溶液 b.FeSO4溶液 c.KMnO4溶液
(2)家庭中常用消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)等清洁卫生。某品牌消毒液包装上的说明如下图。
①分析“对金属制品有腐蚀作用”的原因:_______________ 。
②需“密闭保存”的原因:______________ 。
③“与洁厕灵同时使用”会产生有毒的氯气,请写出反应的离子方程式_____________ 。
(3)已知空气中氯气含量超过0.1mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗0.001ml/L Kl溶液100mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是_______ 。
(1)氯气属于有毒气体,贮氯罐意外泄漏时,消防员会喷洒稀氢氧化钠溶液,其作用是
实验室常用NaOH溶液吸收多余的氯气,下列也可用于吸收氯气的是
a.NaCl溶液 b.FeSO4溶液 c.KMnO4溶液
(2)家庭中常用消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)等清洁卫生。某品牌消毒液包装上的说明如下图。

①分析“对金属制品有腐蚀作用”的原因:
②需“密闭保存”的原因:
③“与洁厕灵同时使用”会产生有毒的氯气,请写出反应的离子方程式
(3)已知空气中氯气含量超过0.1mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗0.001ml/L Kl溶液100mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是
您最近一年使用:0次
7 . 根据下列实验过程,请回答:
(1)在常温下,将氯气通入氢氧化钠溶液中,所发生反应的离子方程式为:__ ;所得溶液具有漂白性,其有效成分的名称为__ 。
(2)将上述呈碱性的溶液与FeCl3溶液混合,可制得一种新型绿色消毒剂——高铁酸钠(Na2FeO4),反应如下:3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O则该反应中的氧化产物是__ (填离子符号),当反应中转移电子的数目是0.3NA时,所消耗的氧化剂的物质的量为__ 。
(3)证实最终所得溶液中含有Na+的操作是:进行焰色实验时,火焰呈现__ 色。
(1)在常温下,将氯气通入氢氧化钠溶液中,所发生反应的离子方程式为:
(2)将上述呈碱性的溶液与FeCl3溶液混合,可制得一种新型绿色消毒剂——高铁酸钠(Na2FeO4),反应如下:3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O则该反应中的氧化产物是
(3)证实最终所得溶液中含有Na+的操作是:进行焰色实验时,火焰呈现
您最近一年使用:0次
2020-04-28更新
|
167次组卷
|
3卷引用:广西百色市田阳区田阳高中2021-2022学年高一上学期12月月考化学试题



