名校
解题方法
1 . 已知: 是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为:
是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为: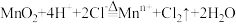 ,回答下列问题:
,回答下列问题:
(1)从方程式两边电荷守恒角度判断,方程式中
___________ 。
(2)该反应的还原剂是___________ ,实验室检验该离子的试剂是硝酸酸化的硝酸银溶液。
(3)该反应的还原产物是___________ 。
(4)若该反应消耗 ,产生标准状况下的
,产生标准状况下的
___________ L。
(5)实验室制取 时要用
时要用 溶液吸收多余的氯气。反应的化学方程式为:
溶液吸收多余的氯气。反应的化学方程式为: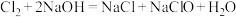 (已知:电离方程式
(已知:电离方程式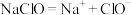 ),该反应的离子方程式为
),该反应的离子方程式为___________ 。
 是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为:
是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为: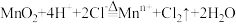 ,回答下列问题:
,回答下列问题:(1)从方程式两边电荷守恒角度判断,方程式中

(2)该反应的还原剂是
(3)该反应的还原产物是
(4)若该反应消耗
 ,产生标准状况下的
,产生标准状况下的
(5)实验室制取
 时要用
时要用 溶液吸收多余的氯气。反应的化学方程式为:
溶液吸收多余的氯气。反应的化学方程式为: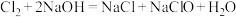 (已知:电离方程式
(已知:电离方程式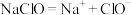 ),该反应的离子方程式为
),该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 如图为钠和氯的价类二维图,请据图完成下列问题:
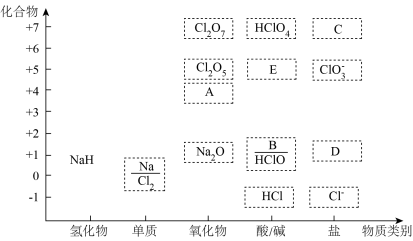
(1)NaH中的氢为___________ 价。可与水反应生成氢气,该反应中氧化产物和还原产物的质量比为___________ 。
(2)A是氯的氧化物,其化学式为___________ 。A可用于自来水消毒。其消毒效率是 的
的___________ 倍(还原产物都是 ,消毒效率以单位物质的量的物质得到的电子数表示)。
,消毒效率以单位物质的量的物质得到的电子数表示)。
(3)B属于碱,其水溶液与 反应生成D的离子方程式为
反应生成D的离子方程式为___________ 。
(4)C是高氯酸钠,受热分解可产生 和非含氧酸盐,则高氯酸钠热分解的化学方程式为
和非含氧酸盐,则高氯酸钠热分解的化学方程式为___________ 。
(5) 可与水反应生成
可与水反应生成 ,
, 生成E也是发生类似的反应,请写出
生成E也是发生类似的反应,请写出 与B在水中生成
与B在水中生成 的离子反应方程式
的离子反应方程式___________ 。

(1)NaH中的氢为
(2)A是氯的氧化物,其化学式为
 的
的 ,消毒效率以单位物质的量的物质得到的电子数表示)。
,消毒效率以单位物质的量的物质得到的电子数表示)。(3)B属于碱,其水溶液与
 反应生成D的离子方程式为
反应生成D的离子方程式为(4)C是高氯酸钠,受热分解可产生
 和非含氧酸盐,则高氯酸钠热分解的化学方程式为
和非含氧酸盐,则高氯酸钠热分解的化学方程式为(5)
 可与水反应生成
可与水反应生成 ,
, 生成E也是发生类似的反应,请写出
生成E也是发生类似的反应,请写出 与B在水中生成
与B在水中生成 的离子反应方程式
的离子反应方程式
您最近一年使用:0次
24-25高一上·全国·假期作业
解题方法
3 . 某校高一化学研究性学习小组对氯气在日常生活中的用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等。
(1)氯气可以用于漂白、消毒的原因是氯气能与水反应,生成具有漂白、消毒作用的___________ (填名称),相关反应的离子方程式为___________ 。
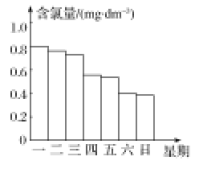
(2)在调查某室外大型游泳池夏季池水消毒情况时,该小组成员了解到,游泳池每周一上午8:00换水,然后通入氯气消毒,通常游泳池水中的含氯量(有效氯)控制在 时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?
时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?___________ 。
(3)根据下图判断,你认为哪几天的天气炎热、阳光强烈?___________ ,请写出可能的原因:___________ (用化学方程式表示)。
(4)小型游泳池通常使用漂白液(含 的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:
的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:___________ (写出一个即可);用化学方程式说明工业上生产漂白液的原理:___________ 。
(1)氯气可以用于漂白、消毒的原因是氯气能与水反应,生成具有漂白、消毒作用的
(2)在调查某室外大型游泳池夏季池水消毒情况时,该小组成员了解到,游泳池每周一上午8:00换水,然后通入氯气消毒,通常游泳池水中的含氯量(有效氯)控制在
 时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?
时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?(3)根据下图判断,你认为哪几天的天气炎热、阳光强烈?

(4)小型游泳池通常使用漂白液(含
 的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:
的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:
您最近一年使用:0次
名校
4 . 某家用防疫用品“84消毒液”的包装说明如下,请回答下列问题:
(1)“84”消毒液可由Cl2与NaOH溶液反应制得,Cl2与NaOH溶液反应的化学方程式为___________
(2)欲将“84消毒液”原液稀释配制成450mL c(NaClO)=0.100mol·L-1的溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、___________ 、___________ 。
②配制时,需要取用___________ mL“84消毒液”原液。
③下列操作会使溶液中NaClO浓度偏低的是___________ 。
A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
(3)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到pH试纸的现象是___________
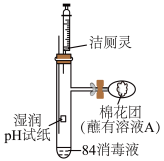
| 【产品名称】84消毒液 【有效成分】NaClO 【规格】1000mL 【物质的量浓度】4.0  注:①按一定比例稀释后使用 ②不得与酸性产品(如洁厕灵)同时使用。 |
(2)欲将“84消毒液”原液稀释配制成450mL c(NaClO)=0.100mol·L-1的溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、
②配制时,需要取用
③下列操作会使溶液中NaClO浓度偏低的是
A.取用的“84消毒液”原液是久置的
B.定容操作时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
(3)利用如图装置探究84消毒液与洁厕灵(主要成分为盐酸)的反应,当注射器中的洁厕灵注入试管中时,装置内产生黄绿色气体,可观察到pH试纸的现象是

您最近一年使用:0次
2023-11-11更新
|
221次组卷
|
4卷引用:福建省福州市八县一中2023-2024学年高一上学期11月期中化学试题
23-24高一上·山东烟台·阶段练习
名校
5 . 氯气是一种重要的化工原料。
(1)氯气和石灰乳反应可以制得漂白粉,写出反应的化学方程式___________ ,漂白粉暴露在空气中容易失效,漂白粉失效过程的化学反应方程式为___________ 。
(2)氯气与烧碱溶液反应能够制取消毒液
①写出反应的化学方程式___________ 。
②“84消毒液”能有效杀灭甲型H1N1等病毒,某同学购买了一瓶“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:
“84消毒液”:含质量分数为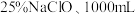 、密度
、密度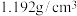 ,稀释100倍(体积比)后使用。
,稀释100倍(体积比)后使用。
请根据以上信息和相关知识回答下列问题:
该“84消毒液”的物质的量浓度为___________  。若一瓶“84消毒液”完全变质,最多能吸收
。若一瓶“84消毒液”完全变质,最多能吸收___________  空气中的
空气中的 (标准状况)。
(标准状况)。
(3)同学参阅该品牌“84消毒液”的配方,欲用 固体配制
固体配制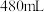 含质量分数为
含质量分数为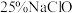 的消毒液,下列说法正确的是___________(填字母)。
的消毒液,下列说法正确的是___________(填字母)。
(4)工业上用氢气在氯气中燃烧的方法制取浓盐酸,现配制一定物质的量浓度的盐酸,下列操作导致所配制的稀盐酸的物质的量浓度偏低的是___________ (填字母)。
A.未恢复到室温就将溶液注入容量瓶并进行定容
B.用量筒量取浓盐酸时俯视凹液面最低处读数
C.容量瓶用蒸馏水洗后未干燥
D.未洗涤烧杯和玻璃棒
E.定容时俯视刻度线
(1)氯气和石灰乳反应可以制得漂白粉,写出反应的化学方程式
(2)氯气与烧碱溶液反应能够制取消毒液
①写出反应的化学方程式
②“84消毒液”能有效杀灭甲型H1N1等病毒,某同学购买了一瓶“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:
“84消毒液”:含质量分数为
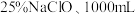 、密度
、密度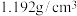 ,稀释100倍(体积比)后使用。
,稀释100倍(体积比)后使用。请根据以上信息和相关知识回答下列问题:
该“84消毒液”的物质的量浓度为
 。若一瓶“84消毒液”完全变质,最多能吸收
。若一瓶“84消毒液”完全变质,最多能吸收 空气中的
空气中的 (标准状况)。
(标准状况)。(3)同学参阅该品牌“84消毒液”的配方,欲用
 固体配制
固体配制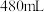 含质量分数为
含质量分数为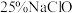 的消毒液,下列说法正确的是___________(填字母)。
的消毒液,下列说法正确的是___________(填字母)。| A.容量瓶在使用前必须要先检漏,检漏时需要倒置一次 |
| B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制 |
C.利用购买的商品 来配制可能导致结果偏低 来配制可能导致结果偏低 |
D.需要称量的 固体质量为 固体质量为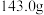 |
A.未恢复到室温就将溶液注入容量瓶并进行定容
B.用量筒量取浓盐酸时俯视凹液面最低处读数
C.容量瓶用蒸馏水洗后未干燥
D.未洗涤烧杯和玻璃棒
E.定容时俯视刻度线
您最近一年使用:0次
6 . 某校化学小组同学将氯气通入NaOH溶液中,制得一种消毒液,运用下列实验,检测该消毒液的性质:
①将少量消毒液滴入含有淀粉的KI溶液中,溶液中出现蓝色;
②用pH试纸检测消毒液,试纸边缘为蓝紫色(pH=13),中间部分为白色;
③向消毒液中加入少量稀硫酸,溶液变为黄绿色,产生使湿润的淀粉KI试纸变蓝的气体。请回答以下问题:
(1)用离子方程式表示制备该消毒液的原理___________ 。
(2)该消毒液中大量存在的阴离子有OH-、___________ 、___________ 。
(3)实验①表现出该消毒液具有___________ 性。
(4)实验②用pH试纸检测消毒液的操作是___________ 。
(5)实验③中涉及反应的离子方程式为___________ 。
①将少量消毒液滴入含有淀粉的KI溶液中,溶液中出现蓝色;
②用pH试纸检测消毒液,试纸边缘为蓝紫色(pH=13),中间部分为白色;
③向消毒液中加入少量稀硫酸,溶液变为黄绿色,产生使湿润的淀粉KI试纸变蓝的气体。请回答以下问题:
(1)用离子方程式表示制备该消毒液的原理
(2)该消毒液中大量存在的阴离子有OH-、
(3)实验①表现出该消毒液具有
(4)实验②用pH试纸检测消毒液的操作是
(5)实验③中涉及反应的离子方程式为
您最近一年使用:0次
解题方法
7 . 海水是一个巨大的化学资源宝库。回答下列问题:
(1)海水提溴工艺中,发生反应: ,该反应中氧化剂是
,该反应中氧化剂是__________ ,它在反应中__________ (填“得到”或“失去”)电子;现有 标准状况下的
标准状况下的 参加该反应,则理论上可转化
参加该反应,则理论上可转化 的物质的量是
的物质的量是_________  。
。
(2)利用化学沉淀法可以去除粗盐中的杂质离子( 等)。向某粗盐水滴加过量
等)。向某粗盐水滴加过量 溶液,有关反应的离子方程式为
溶液,有关反应的离子方程式为__________ ,滴加 溶液略微过量的目的是
溶液略微过量的目的是__________ 。
(3)在常温下,将氯气通入 溶液中,可以得到一种漂白液,上述反应的化学方程式为
溶液中,可以得到一种漂白液,上述反应的化学方程式为__________ ,该漂白液的有效成分是__________ (填名称)。
(1)海水提溴工艺中,发生反应:
 ,该反应中氧化剂是
,该反应中氧化剂是 标准状况下的
标准状况下的 参加该反应,则理论上可转化
参加该反应,则理论上可转化 的物质的量是
的物质的量是 。
。(2)利用化学沉淀法可以去除粗盐中的杂质离子(
 等)。向某粗盐水滴加过量
等)。向某粗盐水滴加过量 溶液,有关反应的离子方程式为
溶液,有关反应的离子方程式为 溶液略微过量的目的是
溶液略微过量的目的是(3)在常温下,将氯气通入
 溶液中,可以得到一种漂白液,上述反应的化学方程式为
溶液中,可以得到一种漂白液,上述反应的化学方程式为
您最近一年使用:0次
23-24高一·全国·假期作业
8 . 配平下列方程式为___________
Cl2 + KOH — KCl + KClO + H2O
Cl2 + KOH — KCl + KClO + H2O
您最近一年使用:0次
22-23高一下·全国·期中
解题方法
9 . 尾气处理装置(见下图a、b、c)
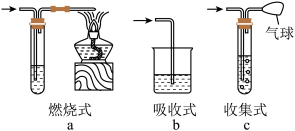
(1)制取Cl2时,尾气的处理可采用________ 装置。
(2)制取CO时,尾气处理可采用________ 装置。
(3)制取H2时,尾气处理可采用________ 装置。

(1)制取Cl2时,尾气的处理可采用
(2)制取CO时,尾气处理可采用
(3)制取H2时,尾气处理可采用
您最近一年使用:0次
10 . 下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与FeCl3溶液 ⑤Cl2与NaOH溶液 ⑥Fe与HNO3溶液 ⑦Fe与H2SO4溶液 ⑧Na与O2
(1)由于浓度不同而发生不同氧化还原反应的是_______ (填序号,下同)。
(2)由于温度不同而发生不同氧化还原反应的是_______ 。
(3)氧化还原反应不受浓度、温度影响的是_______ 。
(1)由于浓度不同而发生不同氧化还原反应的是
(2)由于温度不同而发生不同氧化还原反应的是
(3)氧化还原反应不受浓度、温度影响的是
您最近一年使用:0次



