名校
1 . 按要求回答下列问题。
(1)写出重晶石主要成分的化学式_______ 。
(2)写出用氢氧化钠溶液吸收尾气氯气的化学方程式_______ 。
(3)向氯化铁溶液中滴加硫氰化钾溶液,现象是_______ 。
(1)写出重晶石主要成分的化学式
(2)写出用氢氧化钠溶液吸收尾气氯气的化学方程式
(3)向氯化铁溶液中滴加硫氰化钾溶液,现象是
您最近一年使用:0次
解题方法
2 . 完成下列小题
(1)写出实验室制备氯气的化学方程式_____ 。
(2)常温下, 通入NaOH溶液中,可以制备漂白液,写出此反应离子方程式:
通入NaOH溶液中,可以制备漂白液,写出此反应离子方程式:_____ 。
(3)请用单线桥法标出此反应电子转移方向和数目:_____ 。
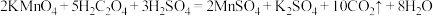
(4)现有下列七种物质:
① 固体②
固体② ③氯化铁溶液④
③氯化铁溶液④ 固体⑤稀硫酸⑥熔融
固体⑤稀硫酸⑥熔融 ⑦Na
⑦Na
在上述物质中,能导电的是_____ ;属于电解质的是_____ 。
(1)写出实验室制备氯气的化学方程式
(2)常温下,
 通入NaOH溶液中,可以制备漂白液,写出此反应离子方程式:
通入NaOH溶液中,可以制备漂白液,写出此反应离子方程式:(3)请用单线桥法标出此反应电子转移方向和数目:
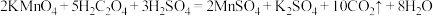
(4)现有下列七种物质:
①
 固体②
固体② ③氯化铁溶液④
③氯化铁溶液④ 固体⑤稀硫酸⑥熔融
固体⑤稀硫酸⑥熔融 ⑦Na
⑦Na在上述物质中,能导电的是
您最近一年使用:0次
名校
解题方法
3 . 回答下列问题:
(1)写出下列物质的化学式:①钡餐:_____ ;②漂白液的有效成分:_____ 。
(2)写出木炭与浓硫酸共热时发生反应的化学方程式:_____ 。
(3)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的基本操作是_____ 。
(1)写出下列物质的化学式:①钡餐:
(2)写出木炭与浓硫酸共热时发生反应的化学方程式:
(3)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的基本操作是
您最近一年使用:0次
解题方法
4 . 完成下列小题
(1)写出“纯碱”的化学式___________ 。
(2)写出AlCl3在水中的电离方程式___________ 。
(3)写出NH3的电子式___________ 。
(4)将氯气通入冷的石灰乳中的化学反应方程式___________ 。
(1)写出“纯碱”的化学式
(2)写出AlCl3在水中的电离方程式
(3)写出NH3的电子式
(4)将氯气通入冷的石灰乳中的化学反应方程式
您最近一年使用:0次
解题方法
5 . 填空
(1)金属钠与水反应的化学方程式:_______
(2)写出次氯酸见光分解的化学方程式:_______
(3)写出氯气和氢氧化钠溶液反应的离子方程式 :_______
(1)金属钠与水反应的化学方程式:
(2)写出次氯酸见光分解的化学方程式:
(3)写出氯气和氢氧化钠溶液反应的
您最近一年使用:0次
解题方法
6 . 化学与人类生活密切相关。请按要求,回答下列问题:
(1)氯气是重要的化工原科,实验室常用 反应制备氯气,该反应的氧化剂是
反应制备氯气,该反应的氧化剂是_______ ;当生成的气体在标准状况下的体积为5.6L时转移的电子数为_______ 个,此时被氧化的物质的物质的量为_______ mol。
(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为_______ 。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为_______ 。
(1)氯气是重要的化工原科,实验室常用
 反应制备氯气,该反应的氧化剂是
反应制备氯气,该反应的氧化剂是(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为
您最近一年使用:0次
7 . 氯是重要的非金属元素,研究它的性质及用途对生产, 生活、科研具有重要意义。
(1)一氯胺(NH2Cl)是一种长效缓释水消毒剂,在中性或酸性环境中会发生反应,生成一种具有强烈杀菌作用的物质,该物质为_______ 。工业上可利用NH3和Cl2反应制备一氯胺; 生成1molNH2Cl时,转移的电子数目为_______ 。
(2)Cl2 与NaOH溶液反应可制取“84消毒液。
用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3), 此时ClO-的浓度为c0mol/L;加热时NaClO能转化为NaClO3,测得t时刻溶液中ClO-的浓度为c1 mol/L (不考虑加热前后溶液体积的变化)。
①用24gNaOH配成250mL溶液时,c(NaOH)=_______ mol/L。
②写出溶液中NaClO分解生成NaClO3的化学方程式:_______ 。
③t时刻溶液中c(Cl-)=_______ mol/L(用含c0、c1的代数式表示)。
(1)一氯胺(NH2Cl)是一种长效缓释水消毒剂,在中性或酸性环境中会发生反应,生成一种具有强烈杀菌作用的物质,该物质为
(2)Cl2 与NaOH溶液反应可制取“84消毒液。
用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3), 此时ClO-的浓度为c0mol/L;加热时NaClO能转化为NaClO3,测得t时刻溶液中ClO-的浓度为c1 mol/L (不考虑加热前后溶液体积的变化)。
①用24gNaOH配成250mL溶液时,c(NaOH)=
②写出溶液中NaClO分解生成NaClO3的化学方程式:
③t时刻溶液中c(Cl-)=
您最近一年使用:0次
8 . 碱式次氯酸镁[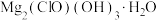 ]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
(1)工业上利用 、NaOH、
、NaOH、 为原料合成碱式次氯酸镁,写出发生反应的化学方程式
为原料合成碱式次氯酸镁,写出发生反应的化学方程式_______ 。
(2)碱式次氯酸镁也可通过电解法制备,在无隔膜状况下以铁为阴极、 为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是
为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是_______ ,阴极电极反应方程式为_______ 。
(3)碱式次氯酸镁经醋酸酸化后杀菌功能增强,原因是_______ (用离子方程式表示)。
(4)碱式次氯酸镁( )的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用
)的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用 标准溶液测定生成的
标准溶液测定生成的 ,将碘单质折算为
,将碘单质折算为 ,有效氯含量
,有效氯含量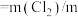 (样品)。则产品的理论有效氯含量为
(样品)。则产品的理论有效氯含量为_______ 。
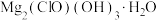 ]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
]微溶于水,是一种有开发价值的无机抗菌剂。请回答:(1)工业上利用
 、NaOH、
、NaOH、 为原料合成碱式次氯酸镁,写出发生反应的化学方程式
为原料合成碱式次氯酸镁,写出发生反应的化学方程式(2)碱式次氯酸镁也可通过电解法制备,在无隔膜状况下以铁为阴极、
 为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是
为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是(3)碱式次氯酸镁经醋酸酸化后杀菌功能增强,原因是
(4)碱式次氯酸镁(
 )的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用
)的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用 标准溶液测定生成的
标准溶液测定生成的 ,将碘单质折算为
,将碘单质折算为 ,有效氯含量
,有效氯含量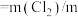 (样品)。则产品的理论有效氯含量为
(样品)。则产品的理论有效氯含量为
您最近一年使用:0次
名校
解题方法
9 . 回答下列问题:
(1)写出漂白液有效成分的化学式_______ 。
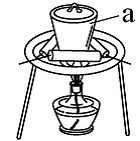
(2)写出仪器a的名称:_______ 。
(3)现有下列物质,能导电的是_______ ,属于电解质的是_______ 。
①NaCl固体 ②盐酸 ③熔融的KNO3④氯水 ⑤CaO ⑥H2SO4 ⑦CO2⑧汽油 ⑨氧化钠 ⑩Na
(4)写出过氧化钠与二氧化碳反应的化学方程式_______ 。
(5)写出氯气和氢氧化钠反应的离子方程式_______ 。
(6)配平并用双线桥 标注电子的转移_______ 。
_______KIO3+_______KI+_______H2SO4——_______I2+_______K2SO4+_______H2O
(1)写出漂白液有效成分的化学式
(2)写出仪器a的名称:

(3)现有下列物质,能导电的是
①NaCl固体 ②盐酸 ③熔融的KNO3④氯水 ⑤CaO ⑥H2SO4 ⑦CO2⑧汽油 ⑨氧化钠 ⑩Na
(4)写出过氧化钠与二氧化碳反应的化学方程式
(5)写出氯气和氢氧化钠反应的离子方程式
(6)配平并用
_______KIO3+_______KI+_______H2SO4——_______I2+_______K2SO4+_______H2O
您最近一年使用:0次
解题方法
10 . 将一定量 通入1kg质量分数为
通入1kg质量分数为 的
的 溶液中,制成含有
溶液中,制成含有 、
、 和
和 的混合溶液。用此溶液吸收标准状况下
的混合溶液。用此溶液吸收标准状况下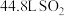 ,恰好形成中性溶液(假设气体均完全反应),请计算:
,恰好形成中性溶液(假设气体均完全反应),请计算:
(1)原 溶液中
溶液中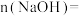
_______  。
。
(2)所通 在标准状况下的体积为
在标准状况下的体积为_______ L。
 通入1kg质量分数为
通入1kg质量分数为 的
的 溶液中,制成含有
溶液中,制成含有 、
、 和
和 的混合溶液。用此溶液吸收标准状况下
的混合溶液。用此溶液吸收标准状况下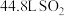 ,恰好形成中性溶液(假设气体均完全反应),请计算:
,恰好形成中性溶液(假设气体均完全反应),请计算:(1)原
 溶液中
溶液中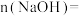
 。
。(2)所通
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次



