名校
1 . 离子反应是中学化学中重要的反应类型。回答下列问题:
(1)离子方程式是重要的化学用语。下列是有关离子方程式的一个错误观点:酸碱中和反应均可表示为 ,请用一个相应的“离子方程式”否定这个观点。
,请用一个相应的“离子方程式”否定这个观点。___________
(2)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“ ”来表示,请写出2个有关反应的化学方程式:
”来表示,请写出2个有关反应的化学方程式:
①___________ ;
②___________ 。
(3)实验室用铁、氧化铜、稀硫酸为原料制取铜,某同学设计了两个实验方案:
方案一: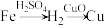
方案二:
写出上述两个方案每步转化的有关方程式。
方案一,化学方程式:___________ ;___________
方案二,离子方程式:___________ ;___________
(4)在常温下,将 通入
通入 溶液中,可以得到一种漂白液。上述反应的离子方程式为
溶液中,可以得到一种漂白液。上述反应的离子方程式为___________ ,该漂白液的有效成分是___________ (填名称)。
(5)检验某溶液中是否含有 的方法是:
的方法是:___________ ,有关离子方程式是___________ 。
(1)离子方程式是重要的化学用语。下列是有关离子方程式的一个错误观点:酸碱中和反应均可表示为
 ,请用一个相应的“离子方程式”否定这个观点。
,请用一个相应的“离子方程式”否定这个观点。(2)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“
 ”来表示,请写出2个有关反应的化学方程式:
”来表示,请写出2个有关反应的化学方程式:①
②
(3)实验室用铁、氧化铜、稀硫酸为原料制取铜,某同学设计了两个实验方案:
方案一:
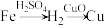
方案二:

写出上述两个方案每步转化的有关方程式。
方案一,化学方程式:
方案二,离子方程式:
(4)在常温下,将
 通入
通入 溶液中,可以得到一种漂白液。上述反应的离子方程式为
溶液中,可以得到一种漂白液。上述反应的离子方程式为(5)检验某溶液中是否含有
 的方法是:
的方法是:
您最近一年使用:0次
2 . 消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1) 、
、 、
、 (还原产物为
(还原产物为 )、
)、 都可以做消毒剂,都具有
都可以做消毒剂,都具有___________ 性。
(2)将紫色石蕊试液滴入氯水中现象是___________ 。
(3)漂白剂亚氯酸钠( )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为
)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为 (未配平)。在该反应中,被氧化的元素是
(未配平)。在该反应中,被氧化的元素是___________ ,13.7g 完全反应转移电子数是
完全反应转移电子数是___________ 。
(4)“84”消毒液(主要成分是NaClO),用氯气制取NaClO的离子方程式是___________ ,使用“84”消毒液时加入少量的稀硫酸效果更好,原理是___________ (用离子方程式表示)。
(1)
 、
、 、
、 (还原产物为
(还原产物为 )、
)、 都可以做消毒剂,都具有
都可以做消毒剂,都具有(2)将紫色石蕊试液滴入氯水中现象是
(3)漂白剂亚氯酸钠(
 )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为
)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为 (未配平)。在该反应中,被氧化的元素是
(未配平)。在该反应中,被氧化的元素是 完全反应转移电子数是
完全反应转移电子数是(4)“84”消毒液(主要成分是NaClO),用氯气制取NaClO的离子方程式是
您最近一年使用:0次
名校
解题方法
3 . 将 通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
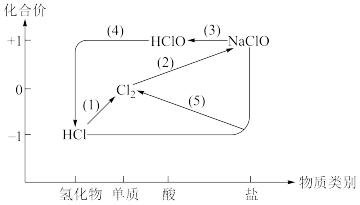
(1)实验室用二氧化锰和浓盐酸反成制备氯气,在制取Cl2的反应中,浓盐酸发生了___________ 反应
(2)制备84消毒液的化学方程式为___________ 。
(3)84消毒液中加入少量醋酸(CH3COOH)可增强效果,该反应的化学方程式为___________ 。
(4)次氯酸不稳定,光照条件下易分解。该反应的化学方程式为___________ 。
(5)84消毒液不能与洁厕剂(含盐酸)一起混合使用的原因为___________ (用离子反应方程式表示)。
 通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
(1)实验室用二氧化锰和浓盐酸反成制备氯气,在制取Cl2的反应中,浓盐酸发生了
(2)制备84消毒液的化学方程式为
(3)84消毒液中加入少量醋酸(CH3COOH)可增强效果,该反应的化学方程式为
(4)次氯酸不稳定,光照条件下易分解。该反应的化学方程式为
(5)84消毒液不能与洁厕剂(含盐酸)一起混合使用的原因为
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
(1)根据分类的方法可以预测物质的性质及可能发生的变化。SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:___________ 。
(2)根据所学,写出一个H2O既做氧化剂,又做还原剂的化学反应方程式___________ 。
(3)将Cl2通入NaOH溶液,充分反应后测得溶液中ClO-与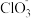 个数比为3:1,则被氧化与被还原的氯元素质量比为
个数比为3:1,则被氧化与被还原的氯元素质量比为___________ ;离子方程式为___________ 。
(4)H2与Cl2混合点燃,充分反应后,将气体通入含有40 g NaOH的溶液中恰好完全反应,则混合气体中Cl2质量为___________ 。
(5)向FeBr2溶液中通入一定量的Cl2,充分反应后,测得游离态的溴元素和化合态的溴元素质量比为1:1,写出反应的离子方程式___________ 。
(6)将醋酸(CH3COOH)溶液滴入到Na2CO3溶液中,开始时发生的离子方程式是___________ 。将Na2CO3溶液滴入到醋酸(CH3COOH)溶液中,开始时发生的离子方程式是___________ 。
(7)在碱性条件下,Cl2可将废水中的CN-氧化为无毒的N2和 ,该过程反应的离子方程式为
,该过程反应的离子方程式为___________ 。
(8)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得相同质量的氧气时,四个反应中转移的电子数之比为___________ 。
(1)根据分类的方法可以预测物质的性质及可能发生的变化。SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:
(2)根据所学,写出一个H2O既做氧化剂,又做还原剂的化学反应方程式
(3)将Cl2通入NaOH溶液,充分反应后测得溶液中ClO-与
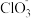 个数比为3:1,则被氧化与被还原的氯元素质量比为
个数比为3:1,则被氧化与被还原的氯元素质量比为(4)H2与Cl2混合点燃,充分反应后,将气体通入含有40 g NaOH的溶液中恰好完全反应,则混合气体中Cl2质量为
(5)向FeBr2溶液中通入一定量的Cl2,充分反应后,测得游离态的溴元素和化合态的溴元素质量比为1:1,写出反应的离子方程式
(6)将醋酸(CH3COOH)溶液滴入到Na2CO3溶液中,开始时发生的离子方程式是
(7)在碱性条件下,Cl2可将废水中的CN-氧化为无毒的N2和
 ,该过程反应的离子方程式为
,该过程反应的离子方程式为(8)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得相同质量的氧气时,四个反应中转移的电子数之比为
您最近一年使用:0次
名校
5 . 由氢气和氯气组成的混合气体,经光照充分反应后,通入100mL1molLNaOH溶液中,溶液中某种离子的物质的量(图甲)和溶液的导电性(图乙)随着反应后的混合气体通入体积的变化而变化。
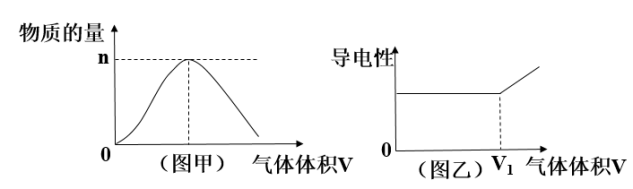
(1)图甲曲线表示溶液中___________ 离子的变化。
(2)对溶液进行导电性实验时,发现当通入的光照反应后的混合气体体积大于V1时,随着混合气体的通入,溶液导电性明显增强,引起导电性增强的主要正、负离子是___________ 。
(3)当图甲中n=0.01mol时,则光照前的混合气体中H2和Cl2的物质的量之比为___________ 。(书写必要步骤)

(1)图甲曲线表示溶液中
(2)对溶液进行导电性实验时,发现当通入的光照反应后的混合气体体积大于V1时,随着混合气体的通入,溶液导电性明显增强,引起导电性增强的主要正、负离子是
(3)当图甲中n=0.01mol时,则光照前的混合气体中H2和Cl2的物质的量之比为
您最近一年使用:0次
6 . 氯是一种生产生活中常见的元素,下图是几种含氯产品。

(1)Cl2是有毒气体,为了防止多余Cl2污染空气,需要上图装置进行尾气处理,用化学方程式表示该原理___________ 。气体应该由___________ (填a或b)管通入。若要吸收标准状况下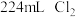 ,至少需要1mol/L的上述溶液
,至少需要1mol/L的上述溶液___________ mL。
(2)工业上制取漂白粉的化学方程式是___________ 。
(3)抗击新冠肺炎的战役中使用了大量的84消毒液。同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验。将5mL市售84消毒液稀释100倍,测得稀释后溶液的 ,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
已知溶液中 、HClO和
、HClO和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
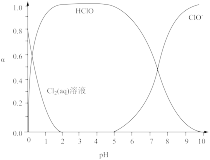
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色___________ (填“越快”或“越慢”)。
②结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是___________ 。

(1)Cl2是有毒气体,为了防止多余Cl2污染空气,需要上图装置进行尾气处理,用化学方程式表示该原理
 ,至少需要1mol/L的上述溶液
,至少需要1mol/L的上述溶液(2)工业上制取漂白粉的化学方程式是
(3)抗击新冠肺炎的战役中使用了大量的84消毒液。同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验。将5mL市售84消毒液稀释100倍,测得稀释后溶液的
 ,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:| 烧杯 | 溶液pH | 现象 |
| a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
| b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
| c | 4 | 10min后,红纸颜色比b烧杯中10min后的浅;4h后红纸褪色 |
 、HClO和
、HClO和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色
②结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
7 . 回答下列问题:
(1)向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有NaHCO3生成,该反应的化学方程式是___ 。
(2)Na2CO3浓溶液中通入氯气时,可产生气体CO2和化合物NaClO3。反应的化学方程式为___ 。
(1)向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有NaHCO3生成,该反应的化学方程式是
(2)Na2CO3浓溶液中通入氯气时,可产生气体CO2和化合物NaClO3。反应的化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 按要求书写方程式
(1)NaHSO4在熔融状态的电离方程式___________
(2)碳酸钙溶解在醋酸中的离子反应方程式___________
(3)将“ ”改写为对应的化学方程式
”改写为对应的化学方程式___________
(4)除去Na2CO3粉末中混有少量NaHCO3的化学方程式___________
(5)氯气与烧碱溶液反应的化学方程式为___________
(6)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是___________
(7)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的 ,配平该反应的离子方程式:
,配平该反应的离子方程式:___________
_______MnO +_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
+_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
(1)NaHSO4在熔融状态的电离方程式
(2)碳酸钙溶解在醋酸中的离子反应方程式
(3)将“
 ”改写为对应的化学方程式
”改写为对应的化学方程式(4)除去Na2CO3粉末中混有少量NaHCO3的化学方程式
(5)氯气与烧碱溶液反应的化学方程式为
(6)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是
(7)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的
 ,配平该反应的离子方程式:
,配平该反应的离子方程式:_______MnO
 +_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
+_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
您最近一年使用:0次
2021高三·全国·专题练习
9 . 实验室制备氯酸钾、次氯酸钠和氯水的装置如图所示。
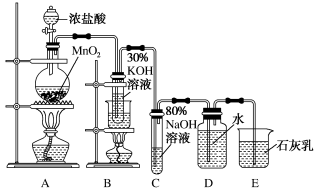
制备KClO3需在70~80℃进行,写出制备KClO3的离子方程式:___ 。

制备KClO3需在70~80℃进行,写出制备KClO3的离子方程式:
您最近一年使用:0次
10 . 游泳池水中的氯气含量应该控制在0.5~1.0 mg·L-1之间。
(1)写出氯气溶于水的化学方程式:___________ 。溶于水后的哪种物质可杀菌消毒:___________ (写化学式)。
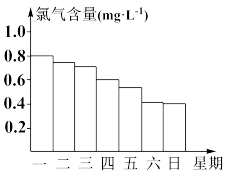
(2)如图显示一星期中每天19时游泳池水中的氯气含量,哪几天19时使用游泳池不安全?___________ 。
(3)你认为哪几天的天气炎热、阳光强烈?___________ ,说出一种理由___________ 。
(4)若把一片紫色的花瓣放入氯水中,可观察到的现象是___________ (花瓣所含色素性质与石蕊相似)。
(5)小型游泳池通常使用次氯酸钠溶液而非氯气给池水消毒,用化学方程式说明工业上如何生产次氯酸钠:___________ 。
(1)写出氯气溶于水的化学方程式:
(2)如图显示一星期中每天19时游泳池水中的氯气含量,哪几天19时使用游泳池不安全?

(3)你认为哪几天的天气炎热、阳光强烈?
(4)若把一片紫色的花瓣放入氯水中,可观察到的现象是
(5)小型游泳池通常使用次氯酸钠溶液而非氯气给池水消毒,用化学方程式说明工业上如何生产次氯酸钠:
您最近一年使用:0次
2021-10-26更新
|
67次组卷
|
2卷引用:福建省永安市第三中学高中校2021-2022学年高一上学期10月月考化学试题



