名校
解题方法
1 . 2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、以及由其制备得到的漂白液、漂白粉都是生活中常见的含氯消毒剂。
(1)常温下用烧碱溶液吸收Cl2制备“84”消毒液,但是将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO、NaClO3的混合溶液。当混合溶液中的Cl-和ClO 的个数比为15:2时,混合液中的ClO-和ClO
的个数比为15:2时,混合液中的ClO-和ClO 的个数比为
的个数比为__ ,从氧化还原角度分析Cl2表现了_______ 性。
(2)“洁厕灵”和“84”消毒液不可以混合使用,请用离子方程式解释原因:_______
(1)常温下用烧碱溶液吸收Cl2制备“84”消毒液,但是将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO、NaClO3的混合溶液。当混合溶液中的Cl-和ClO
 的个数比为15:2时,混合液中的ClO-和ClO
的个数比为15:2时,混合液中的ClO-和ClO 的个数比为
的个数比为(2)“洁厕灵”和“84”消毒液不可以混合使用,请用离子方程式解释原因:
您最近一年使用:0次
解题方法
2 . (1)在某防空防灾演习现场,模拟一起大客车与一辆装有氯气的槽罐车发生追尾事故,造成槽罐翻落、氯气泄漏。人防办立即指挥专业救援队在事发地点,测定风向,进行事故处置。引导大客车上的乘客_____________ (填序号)
a.顺风向高处转移 b.顺风向低处转移
c.逆风向高处转移 d.逆风向低处转移
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是________ 。
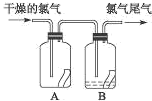
(3)为防止氯气尾气污染空气,根据氯气的性质,可用NaOH溶液吸收多余的氯气,原理是(用离子方程式表示)____________ 。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是________ (填化学式),长期露置于空气中的漂白粉会失效的原因,用化学反应方程式可表示为________ 。
a.顺风向高处转移 b.顺风向低处转移
c.逆风向高处转移 d.逆风向低处转移
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是

(3)为防止氯气尾气污染空气,根据氯气的性质,可用NaOH溶液吸收多余的氯气,原理是(用离子方程式表示)
您最近一年使用:0次
2021-01-29更新
|
255次组卷
|
2卷引用:首都师范大学附属中学2020-2021学年高一上学期期末考试化学试题
名校
3 . “84消毒液”是日常生活中常用的消毒液,有效成分是NaClO。在抗击新冠肺炎中广泛应用。
(1)用“84”消毒液漂白衣物时,在空气中放置一段时间漂白效果更好,结合离子方程式解释原因_ ;(已知酸性:H2CO3>HClO> )
)
(2)“84消毒液”与适量醋酸混合使用可增强消毒能力,某消毒组成员欲用盐酸代替醋酸,是否可行__ (填“是”或“否”),原因是________ ;
(3)Cl2是最早用于饮用水消毒的物质,ClO2是一种广谱消毒剂,Cl2和ClO2消毒效率(消毒效率是指单位质量的氧化剂转移电子数,转移电子数越多,消毒效率越高)高的是___ (填化学式),工业上ClO2常用NaClO3和Na2SO3溶液混合酸化反应制得,请写出此过程的离子方程式_____ ;
(4)实验室常用烧碱溶液吸收Cl2,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时,混合液中NaClO和NaClO3的物质的量之比为_ ;
(5)已知:3Cl2+8NH3=6NH4Cl+N2,化工厂可用浓氨水来检验Cl2是否泄漏,该反应中被氧化和未被氧化的NH3的物质的量之比为______ 。
(1)用“84”消毒液漂白衣物时,在空气中放置一段时间漂白效果更好,结合离子方程式解释原因
 )
)(2)“84消毒液”与适量醋酸混合使用可增强消毒能力,某消毒组成员欲用盐酸代替醋酸,是否可行
(3)Cl2是最早用于饮用水消毒的物质,ClO2是一种广谱消毒剂,Cl2和ClO2消毒效率(消毒效率是指单位质量的氧化剂转移电子数,转移电子数越多,消毒效率越高)高的是
(4)实验室常用烧碱溶液吸收Cl2,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时,混合液中NaClO和NaClO3的物质的量之比为
(5)已知:3Cl2+8NH3=6NH4Cl+N2,化工厂可用浓氨水来检验Cl2是否泄漏,该反应中被氧化和未被氧化的NH3的物质的量之比为
您最近一年使用:0次
4 . 工业尾气中的氯气有多种处理方法。
(1)处理尾气中少量氯气的方法如图所示。
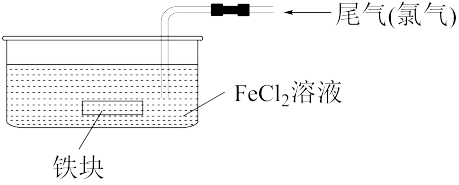
①处理过程中,发生反应的离子方程式为_______ 。
②为维持处理过程的持续进行,需要定期加入的物质是_______ 。
(2)大量氯气可用NaOH溶液处理,标准状况下,处理11.2L Cl2转移电子的物质的量为_______ mol。
(1)处理尾气中少量氯气的方法如图所示。

①处理过程中,发生反应的离子方程式为
②为维持处理过程的持续进行,需要定期加入的物质是
(2)大量氯气可用NaOH溶液处理,标准状况下,处理11.2L Cl2转移电子的物质的量为
您最近一年使用:0次
解题方法
5 . 工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水。下图为离子交换膜法电解原理示意图:
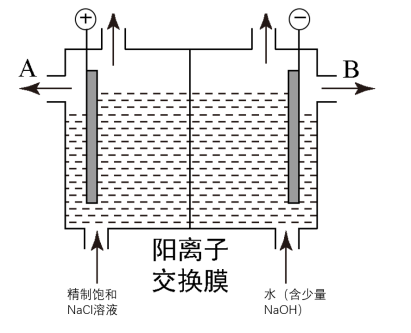
请回答下列问题:
(1)A极为电解槽的_______ 极(正、负、阴、阳),电极反应式为_______ 。
(2)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,它只允许_______ (填离子符号,下同)通过,而不允许_______ 和气体通过。
(3)电解法制碱的主要原料饱和食盐水是由粗盐制得,其中含有泥沙及 、
、 、
、 、
、 等杂质,因此必须精制。精制时所用试剂为①
等杂质,因此必须精制。精制时所用试剂为① ②
② ③
③ ④盐酸,这四种试剂的添加顺序为
④盐酸,这四种试剂的添加顺序为_______ (填序号)。
(4)若将标准状况下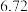 L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是
L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是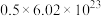 ,产物中得到了两种含氯化合物,写出该反应的离子方程式:
,产物中得到了两种含氯化合物,写出该反应的离子方程式:_______ 。

请回答下列问题:
(1)A极为电解槽的
(2)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,它只允许
(3)电解法制碱的主要原料饱和食盐水是由粗盐制得,其中含有泥沙及
 、
、 、
、 、
、 等杂质,因此必须精制。精制时所用试剂为①
等杂质,因此必须精制。精制时所用试剂为① ②
② ③
③ ④盐酸,这四种试剂的添加顺序为
④盐酸,这四种试剂的添加顺序为(4)若将标准状况下
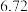 L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是
L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是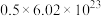 ,产物中得到了两种含氯化合物,写出该反应的离子方程式:
,产物中得到了两种含氯化合物,写出该反应的离子方程式:
您最近一年使用:0次
6 . 下面是有关金属钠和非金属氯及其化合物的实验探究。
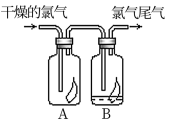
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是:_________________________ 。
(2)实验室制备氯气时要在通风橱内完成,并且为了防止氯气污染空气,要有尾气处理装置,一般用_______ 溶液吸收多余的氯气,原理是_________________ (用化学方程式表示)。
(3)钠是___________ 色金属,在空气中燃烧的产物的化学式是_______________ ,燃烧时火焰颜色是____________ ,产物颜色是______________ 。将切开的小块钠投入水中,发生反应的化学方程式为________________ 。
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是:

(2)实验室制备氯气时要在通风橱内完成,并且为了防止氯气污染空气,要有尾气处理装置,一般用
(3)钠是
您最近一年使用:0次
解题方法
7 . 疫情防控期间的消毒工作含氯消毒剂功不可没,研究消毒剂的性质意义重大。回答下列问题:
(1)2016年巴西奥运会游泳池变绿是因为84消毒液与过氧化氢消毒剂混用,写出该反应的化学方程式_______ ,转移电子数为3NA时,理论上生成标况下气体体积是________ 。
(2) 、HClO和
、HClO和 三种微粒的物质的量分数随pH变化的关系如图所示。
三种微粒的物质的量分数随pH变化的关系如图所示。
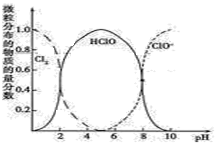
回答问题:
①使用84消毒液时为增强消毒效果常调节 ,原因是
,原因是___________ 。
②通常购买的84消毒液pH在12左右,此时主要成分是___________ (化学式),为增强消毒效果可向其中滴加___________ (填字母序号)。
A.可口可乐 B.稀 C.食醋 D.浓盐酸
C.食醋 D.浓盐酸
(3)实验室将 通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为NA,计算此时所得溶液中NaClO的质量分数为
通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为NA,计算此时所得溶液中NaClO的质量分数为___________ %。
(1)2016年巴西奥运会游泳池变绿是因为84消毒液与过氧化氢消毒剂混用,写出该反应的化学方程式
(2)
 、HClO和
、HClO和 三种微粒的物质的量分数随pH变化的关系如图所示。
三种微粒的物质的量分数随pH变化的关系如图所示。
回答问题:
①使用84消毒液时为增强消毒效果常调节
 ,原因是
,原因是②通常购买的84消毒液pH在12左右,此时主要成分是
A.可口可乐 B.稀
 C.食醋 D.浓盐酸
C.食醋 D.浓盐酸(3)实验室将
 通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为NA,计算此时所得溶液中NaClO的质量分数为
通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为NA,计算此时所得溶液中NaClO的质量分数为
您最近一年使用:0次
解题方法
8 . 短周期主族元素A、B、C、D、E,F在元素周期表中的位置如图所示。试回答下列问题:
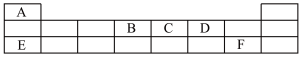
(l)E的某种氧化物可以做制氧剂,请书写所涉及的化学反应方程式:__ 、___ 。
(2)F在周期表中的位置为__ ,其下一周期元素的原子结构示意图为__ ,写出其单质与EDA溶液反应的离子方程式__ 。
(3)写出化合物EABD3在水溶液中的电离方程式__ ,其溶液可与足量的澄清石灰水反应,则反应的离子方程式为__ 。

(l)E的某种氧化物可以做制氧剂,请书写所涉及的化学反应方程式:
(2)F在周期表中的位置为
(3)写出化合物EABD3在水溶液中的电离方程式
您最近一年使用:0次
解题方法
9 . 新型冠状病毒蔓延期间,为做好自我保护,我们要减少外出,避免与表现出有呼吸道疾病症状的人密切接触,外出最重要的防护措施是佩戴符合要求的口罩。在生活中常见的口罩一般有棉布口罩、医用外科口罩、活性炭口罩和N95口罩。也可以在实验室进行制备84消毒液(有效成分是NaClO)。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的_______ (“溶液”、“胶体”、“悬浊液”)。
(2)佩戴口罩预防疾病的原理相当于化学实验中的_______ 操作。(“蒸发”、“过滤”“萃取”)
(3)生成N95口罩的主要原料是聚丙烯,它属于_________ (填“金属材料”或“合成材料”)
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:________ 。

(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为____ 。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的
(2)佩戴口罩预防疾病的原理相当于化学实验中的
(3)生成N95口罩的主要原料是聚丙烯,它属于
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:

(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为
您最近一年使用:0次
解题方法
10 . 新型冠状病毒蔓延期间,为做好自我保护,我们要减少外出,避免与表现出有呼吸道疾病症状的人密切接触,外出最重要的防护措施是佩戴符合要求的口罩。在生活中常见的口罩一般有棉布口罩、医用外科口罩、活性炭口罩和N95口罩。也可以在实验室进行制备84消毒液(有效成分是NaClO)。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的___________ (“溶液”、“胶体”、“悬浊液”)。
(2)佩戴口罩预防疾病的原理相当于化学实验中的_________ 操作。(“蒸发”、“过滤”“萃取”)
(3)生成N95口罩的主要原料是聚丙烯,它属于___________ (填“金属材料”或“合成材料”)
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:__________________________ ,氧化剂是_________ ,氧化产物是_________ 。
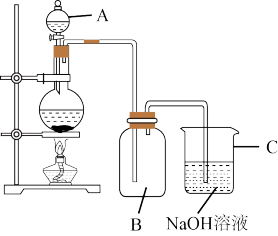
(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为_________ 。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的
(2)佩戴口罩预防疾病的原理相当于化学实验中的
(3)生成N95口罩的主要原料是聚丙烯,它属于
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:

(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为
您最近一年使用:0次



