名校
解题方法
1 . 实验室用石墨电极电解加有酚酞的饱和NaCl溶液,装置如图1所示。氯碱工业用图2所示装置制备NaOH等工业原料。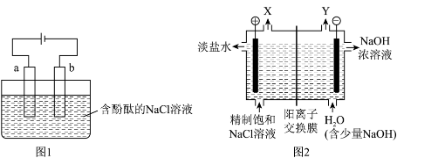
(1)a为电解池的
(2)该电解池中发生的总反应的化学方程式为
(3)下列与电解饱和食盐水有关的说法,正确的是
A.通电使NaCl发生电离
B.在溶液中,阴离子向电极a移动
C.a电极附近溶液变红
Ⅱ.利用实验室装置制备NaOH,不仅有安全隐患,而且存在Cl2与NaOH的副反应,氯碱工业采用改进后的装置,如上图2所示。
(4)气体X和气体Y被阳离子交换膜分隔开,避免混合爆炸。气体X是
(5)阳离子交换膜避免了Cl2与NaOH发生反应,写出Cl2 与NaOH常温下反应的离子方程式
(6)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3混合溶液,经测定ClO-、
 的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原与被氧化的氯元素的物质的量之比为_____。
的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原与被氧化的氯元素的物质的量之比为_____。| A.21:5 | B.4:1 | C.3:1 | D.11:3 |
您最近一年使用:0次
2 . 某工厂在山坡坑道的仓库里贮有氯气钢瓶。某天,有一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取以下措施,请选择。
(1)①处理该钢瓶的方法正确的是_______ 。
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是_______ 。
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______ ;氯水可作为漂白剂,起主要作用的是氯水中含有的_______ (用化学式表示)。
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是_______ (化学方程式);根据这一原理,工业上常用廉价的石灰乳吸收制得漂白粉,漂白粉的有效成分是_______ (填化学式)。
(1)①处理该钢瓶的方法正确的是
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是
您最近一年使用:0次
名校
3 . 按要求回答下列问题。
(1)写出重晶石主要成分的化学式_______ 。
(2)写出用氢氧化钠溶液吸收尾气氯气的化学方程式_______ 。
(3)向氯化铁溶液中滴加硫氰化钾溶液,现象是_______ 。
(1)写出重晶石主要成分的化学式
(2)写出用氢氧化钠溶液吸收尾气氯气的化学方程式
(3)向氯化铁溶液中滴加硫氰化钾溶液,现象是
您最近一年使用:0次
4 . 氯气及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)NaClO中Cl的化合价为______ ,有较强的______ (填氧化、还原)性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式______ 。
(2)黄绿色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为______ ;
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为______ ;
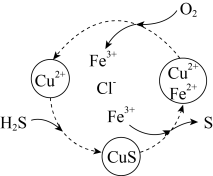
(3)将H2S和空气的混合气体通入FcCl3、FeCl2,CuCl2的混合溶液中反应可以回收S,其物质转化如下图所示。在图示的转化过程中,化合价保持不变的元素有______ (写元素符号),Fe2+和Cu2+反应过程中起______ 作用,该图示的总反应的化学方程式为______ 。
(1)NaClO中Cl的化合价为
(2)黄绿色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为
(3)将H2S和空气的混合气体通入FcCl3、FeCl2,CuCl2的混合溶液中反应可以回收S,其物质转化如下图所示。在图示的转化过程中,化合价保持不变的元素有

您最近一年使用:0次
名校
5 . 根据要求,写出化学方程式或者离子方程式;
(1)氯气和石灰乳反应制取漂白粉的化学方程式___________ ;
(2)过氧化钠和水反应的化学方程式___________ ;
(3)写出 和足量
和足量 反应的离子方程式
反应的离子方程式___________ ;
(4)碘盐中的 和
和 在稀硫酸溶液中发生反应的离子方程式
在稀硫酸溶液中发生反应的离子方程式___________ ;
(5)工业上用黄铁矿制硫酸第一步,在沸腾炉中发生反应的化学方程式___________ ;
(6)铜和浓硫酸加热反应的化学方程式___________ 。
(1)氯气和石灰乳反应制取漂白粉的化学方程式
(2)过氧化钠和水反应的化学方程式
(3)写出
 和足量
和足量 反应的离子方程式
反应的离子方程式(4)碘盐中的
 和
和 在稀硫酸溶液中发生反应的离子方程式
在稀硫酸溶液中发生反应的离子方程式(5)工业上用黄铁矿制硫酸第一步,在沸腾炉中发生反应的化学方程式
(6)铜和浓硫酸加热反应的化学方程式
您最近一年使用:0次
6 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图中分别为钠和氯及其化合物的“价-类”二维图,请回答下列问题:

(1)填写二维图中缺失的化学式:①________ 、②________ 。
(2)含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种________ 颜色气体。实验室沿用舍勒的方法制取Cl2的化学方程式为_________ 。
(3)常温下将Cl2通入NaOH溶液中,可以得到一中漂白液。上述反应的离子方程式为:________________ ,该漂白液的有效成分为________ (填名称)。
(4)小苏打是某种治疗胃酸过多的胃药的主要成分,请写出该反应的离子方程式:________________ 。

(1)填写二维图中缺失的化学式:①
(2)含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种
(3)常温下将Cl2通入NaOH溶液中,可以得到一中漂白液。上述反应的离子方程式为:
(4)小苏打是某种治疗胃酸过多的胃药的主要成分,请写出该反应的离子方程式:
您最近一年使用:0次
名校
解题方法
7 . 按要求回答下列问题:
(1)对含有K2CO3的样品进行焰色试验,需要准备的仪器和试剂有:铂丝、酒精灯、___________ 和___________ 。
(2)高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: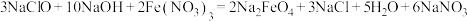 。回答下列问题:
。回答下列问题:
①用氯气制备 的反应原理为
的反应原理为___________ (化学方程式)
②制备高铁酸钠的反应中 体现了
体现了___________ (填“还原性”、“氧化性”或“氧化性和还原性”)
(3)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少了3.1g,所得固体与足量盐酸充分反应(假设CO2完全逸出)。计算:
①混合物中Na2CO3和NaHCO3的物质的量之比为___________ 。
②加入足量盐酸充分反应后产生的CO2在标准状况下的体积为___________ L。
(1)对含有K2CO3的样品进行焰色试验,需要准备的仪器和试剂有:铂丝、酒精灯、
(2)高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: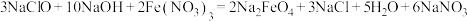 。回答下列问题:
。回答下列问题:①用氯气制备
 的反应原理为
的反应原理为②制备高铁酸钠的反应中
 体现了
体现了(3)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少了3.1g,所得固体与足量盐酸充分反应(假设CO2完全逸出)。计算:
①混合物中Na2CO3和NaHCO3的物质的量之比为
②加入足量盐酸充分反应后产生的CO2在标准状况下的体积为
您最近一年使用:0次
名校
解题方法
8 . NaClO广泛用作水处理剂及漂白剂。
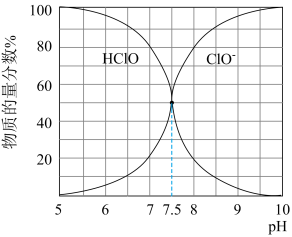
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。
(1)工业上将Cl2通入 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。
①NaClO属于______ (填“酸”、“盐”、“氧化物”),制备NaClO的离子方程式为_______ 。
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了 外,还有
外,还有______ 。
③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目_______ ,该反应中氧化剂与还原剂的物质的量之比是_____ 。
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式______ 。
已知:25℃时NaClO溶液中HClO、ClO-的物质的量分数随pH的分布如下图所示。

(1)工业上将Cl2通入
 的NaOH溶液中制备NaClO。
的NaOH溶液中制备NaClO。①NaClO属于
②取少量pH=9时的溶液加入稀硫酸,发生离子方程式除了
 外,还有
外,还有③若反应温度过高会生成副产物NaClO3,写出该反应的离子方程式并用双线桥标明电子转移的方向和数目
(2)含NaClO消毒液与洁厕剂(含有盐酸)会产生有毒气体,写出该反应的离子方程式
您最近一年使用:0次
名校
解题方法
9 . 已知: 是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为:
是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为: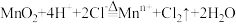 ,回答下列问题:
,回答下列问题:
(1)从方程式两边电荷守恒角度判断,方程式中
___________ 。
(2)该反应的还原剂是___________ ,实验室检验该离子的试剂是硝酸酸化的硝酸银溶液。
(3)该反应的还原产物是___________ 。
(4)若该反应消耗 ,产生标准状况下的
,产生标准状况下的
___________ L。
(5)实验室制取 时要用
时要用 溶液吸收多余的氯气。反应的化学方程式为:
溶液吸收多余的氯气。反应的化学方程式为: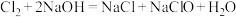 (已知:电离方程式
(已知:电离方程式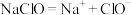 ),该反应的离子方程式为
),该反应的离子方程式为___________ 。
 是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为:
是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为: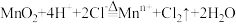 ,回答下列问题:
,回答下列问题:(1)从方程式两边电荷守恒角度判断,方程式中

(2)该反应的还原剂是
(3)该反应的还原产物是
(4)若该反应消耗
 ,产生标准状况下的
,产生标准状况下的
(5)实验室制取
 时要用
时要用 溶液吸收多余的氯气。反应的化学方程式为:
溶液吸收多余的氯气。反应的化学方程式为: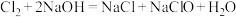 (已知:电离方程式
(已知:电离方程式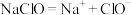 ),该反应的离子方程式为
),该反应的离子方程式为
您最近一年使用:0次
名校
10 . I.海洋约占地球表面积的71%,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、
、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、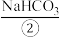 、
、 、
、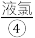 、
、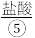 等,苦卤经过氯气氧化,热空气吹出
等,苦卤经过氯气氧化,热空气吹出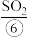 吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼
吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼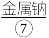 ;海底埋藏大量可燃冰
;海底埋藏大量可燃冰 是一种清洁能源。
是一种清洁能源。
(1)上述标有序号的物质中属于电解质的是___________ (填序号,下同),既不属于电解质也不属于非电解质的是___________ 。
(2)写出③溶于水的电离方程式:___________ 。
(3)在下图所示的装置里,若灯泡亮,广口瓶内的物质A可以是___________ 。(填序号)
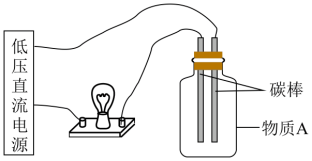
(4) 能被水吸收制备次氯酸(HClO),从物质分类的角度看,
能被水吸收制备次氯酸(HClO),从物质分类的角度看, 属于
属于___________ (填“酸性氧化物”、“碱性氧化物”或“不成盐氧化物”)
Ⅱ.海水中的有丰富的卤素资源。地球是一颗蓝色星球,浩瀚的海洋覆盖了70%以上的地球表面,是蕴藏着极为丰富化学资源的“聚宝盆”,其中氯化物含量很高,氯和同族的氟、溴、碘、砹总称为卤素。
(5)将氯气分别通入含下列离子的溶液中,离子浓度减小的是___________。
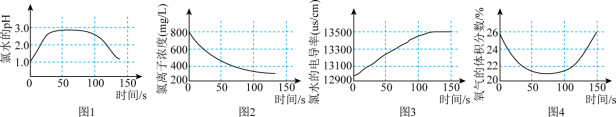
(6)氯气的水溶液即氯水,某学习小组拟用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是___________。
(7)将氯气通入热的NaOH溶液中,反应得到NaCl, 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数之比为4∶1,写出该反应总的离子方程式:
的个数之比为4∶1,写出该反应总的离子方程式:___________ 。
 、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、
、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、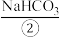 、
、 、
、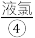 、
、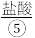 等,苦卤经过氯气氧化,热空气吹出
等,苦卤经过氯气氧化,热空气吹出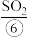 吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼
吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼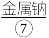 ;海底埋藏大量可燃冰
;海底埋藏大量可燃冰 是一种清洁能源。
是一种清洁能源。(1)上述标有序号的物质中属于电解质的是
(2)写出③溶于水的电离方程式:
(3)在下图所示的装置里,若灯泡亮,广口瓶内的物质A可以是

(4)
 能被水吸收制备次氯酸(HClO),从物质分类的角度看,
能被水吸收制备次氯酸(HClO),从物质分类的角度看, 属于
属于Ⅱ.海水中的有丰富的卤素资源。地球是一颗蓝色星球,浩瀚的海洋覆盖了70%以上的地球表面,是蕴藏着极为丰富化学资源的“聚宝盆”,其中氯化物含量很高,氯和同族的氟、溴、碘、砹总称为卤素。
(5)将氯气分别通入含下列离子的溶液中,离子浓度减小的是___________。
A. | B. | C.Mg2+ | D. |
(6)氯气的水溶液即氯水,某学习小组拟用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是___________。

| A.图1表示氯水pH随时间的变化 |
| B.图2表示溶液中氯离子浓度随时间的变化 |
| C.图3表示氯水的电导率随时间的变化 |
| D.图4表示液面上方氧气体积分数随时间的变化 |
(7)将氯气通入热的NaOH溶液中,反应得到NaCl,
 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数之比为4∶1,写出该反应总的离子方程式:
的个数之比为4∶1,写出该反应总的离子方程式:
您最近一年使用:0次



