1 . 下列实验不能达到对应目的的是
| 选项 | A | B |
| 实验 |
|
|
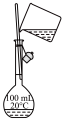
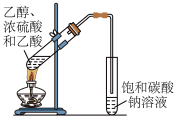
| 目的 | 配制一定物质的量浓度的氯化钠溶液 | 实验室制乙酸乙酯 |
| 选项 | C | D |
| 实验 |
|
|
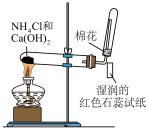
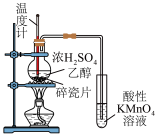
| 目的 | 实验室制氨气并检验氨气的性质 | 检验乙醇消去反应产物中的乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质。______ ;C中圆底烧瓶收集氨气时,请你选择氨气的进气口______ (填“a”或“b”)。
(2)若观察到装置C中的烧瓶内产生了红色喷泉,用化学方程式表示烧瓶内液体变红的原因______ 。
(3)干燥管B中装的试剂是______ (填物质名称)。
(4)以下装置(盛放的液体均为水)可用于吸收多余氨气的是______。(从A-D项中选择)
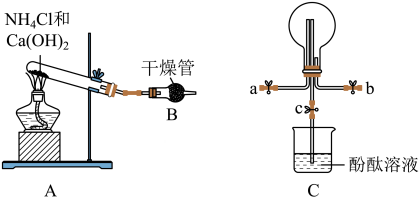
(2)若观察到装置C中的烧瓶内产生了红色喷泉,用化学方程式表示烧瓶内液体变红的原因
(3)干燥管B中装的试剂是
(4)以下装置(盛放的液体均为水)可用于吸收多余氨气的是______。(从A-D项中选择)
①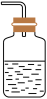 ②
②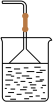 ③
③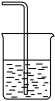 ④
④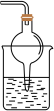
| A.①②③④ | B.①②④ | C.②④ | D.①② |
您最近一年使用:0次
名校
3 . 选择完成下列实验的装置。 和
和 固体混合物制取
固体混合物制取 ,化学方程式为
,化学方程式为___________ 。
(2)加热 和
和 固体混合物制取
固体混合物制取 应选用的发生装置是
应选用的发生装置是___________ 。(填序号,下同)
(3)从NaCl溶液中获取NaCl固体,选用___________ 。

 和
和 固体混合物制取
固体混合物制取 ,化学方程式为
,化学方程式为(2)加热
 和
和 固体混合物制取
固体混合物制取 应选用的发生装置是
应选用的发生装置是(3)从NaCl溶液中获取NaCl固体,选用
您最近一年使用:0次
名校
解题方法
4 . 某化学实验小组同学利用如图所示装置制备氨气,并探究氨气的性质(部分仪器已略去)。___________ 。
(2)干燥氨气可选用的试剂是___________ (填序号)。
①浓H2SO4 ②碱石灰 ③P2O5
(3)收集氨气时,氨气的进气口为___________ (填“a”或“b”)。
(4)证明烧瓶中氨气集满的方法是___________ 。
(5)为防止环境污染,下列装置中(盛放的液体均为水)可用于吸收多余氨气的是___________ (填序号)。___________ (填选项代号)。
a.装置Ⅰ中红色Fe2O3粉末变为黑色粉末,经检验是一种铁的氧化物
b.装置Ⅱ中无水CuSO4粉末变为蓝色
c.装置Ⅲ无水CaCl2的质量增加
d.生成一种无色无味气体,该气体无污染
(7)小组同学继续对(6)装置I反应后黑色粉末的组成进行探究。
(8)结合(6)(7)实验,写出(6)中NH3还原Fe2O3的化学方程式___________ 。
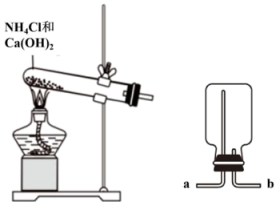
(2)干燥氨气可选用的试剂是
①浓H2SO4 ②碱石灰 ③P2O5
(3)收集氨气时,氨气的进气口为
(4)证明烧瓶中氨气集满的方法是
(5)为防止环境污染,下列装置中(盛放的液体均为水)可用于吸收多余氨气的是
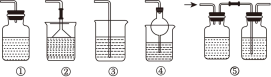
a.装置Ⅰ中红色Fe2O3粉末变为黑色粉末,经检验是一种铁的氧化物
b.装置Ⅱ中无水CuSO4粉末变为蓝色
c.装置Ⅲ无水CaCl2的质量增加
d.生成一种无色无味气体,该气体无污染
(7)小组同学继续对(6)装置I反应后黑色粉末的组成进行探究。
| 操作 | 现象 | 结论或离子方程式 |
| 步骤1:取少量黑色粉末于小烧杯中,加入过量盐酸 | 黑色粉末全部溶解,无气泡产生,溶液呈浅绿色 | 溶液中可能含有Fe2+ |
| 步骤2:取步骤1少量溶液于试管中,滴入2-3滴KSCN溶液,振荡 | 溶液颜色 | 溶液中不含有Fe3+ |
| 步骤3:向步骤2试管中滴入少量氯水 | 溶液变红色 | 涉及离子方程式有 Fe(SCN)3 Fe(SCN)3 |
您最近一年使用:0次
2024-05-27更新
|
208次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷
5 . 下列实验装置及试剂能达成实验目的的是
| A | B | C | D |
|
|
|
|
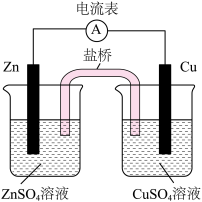
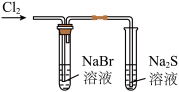
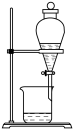
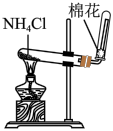
| 验证金属性:Zn>Cu | 验证非金属性:Cl>Br>S | 用乙醇萃取碘水中的碘 | 实验室制氨气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 氨是重要的化工原料,也被认为是一种具有潜在应用前景的能源载体。
(1) 是1754年研究人员加热氯化铵和石灰的混合物时发现的,反应的化学方程式是
是1754年研究人员加热氯化铵和石灰的混合物时发现的,反应的化学方程式是___________ 。
(2)现在依然利用上述原理制取少量 ,实验室可用下图所示装置(夹持仪器略)制备并收集
,实验室可用下图所示装置(夹持仪器略)制备并收集 。
。___________ 。
②采用倒置的漏斗是为了___________ ,一段时间后向蒸馏水中滴加酚酞,溶液变红,用化学用语表示原因___________ 。
(3)由 和
和 直接合成氨是获得大量氨的主要途径。科研人员采用表面科学技术手段,从原子层面上较为清晰的揭示了该反应的微观历程,示意如下:
直接合成氨是获得大量氨的主要途径。科研人员采用表面科学技术手段,从原子层面上较为清晰的揭示了该反应的微观历程,示意如下:___________ (填“吸收能量”或“放出能量”)。
②上述过程中,形成化学键的是___________ (填过程序号)。
(4)以 和
和 为原料直接合成
为原料直接合成 能耗高。最近,我国科研人员报道了一种氯化镁循环法,可进一步降低能耗。该方法的总反应为
能耗高。最近,我国科研人员报道了一种氯化镁循环法,可进一步降低能耗。该方法的总反应为 。转化关系如下:
。转化关系如下:___________ 。
②将X与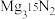 混合反应,证实了氮化镁中氮元素能转化为氨。不考虑其他副反应,产物中
混合反应,证实了氮化镁中氮元素能转化为氨。不考虑其他副反应,产物中
___________ 。
(1)
 是1754年研究人员加热氯化铵和石灰的混合物时发现的,反应的化学方程式是
是1754年研究人员加热氯化铵和石灰的混合物时发现的,反应的化学方程式是(2)现在依然利用上述原理制取少量
 ,实验室可用下图所示装置(夹持仪器略)制备并收集
,实验室可用下图所示装置(夹持仪器略)制备并收集 。
。
②采用倒置的漏斗是为了
(3)由
 和
和 直接合成氨是获得大量氨的主要途径。科研人员采用表面科学技术手段,从原子层面上较为清晰的揭示了该反应的微观历程,示意如下:
直接合成氨是获得大量氨的主要途径。科研人员采用表面科学技术手段,从原子层面上较为清晰的揭示了该反应的微观历程,示意如下:
②上述过程中,形成化学键的是
(4)以
 和
和 为原料直接合成
为原料直接合成 能耗高。最近,我国科研人员报道了一种氯化镁循环法,可进一步降低能耗。该方法的总反应为
能耗高。最近,我国科研人员报道了一种氯化镁循环法,可进一步降低能耗。该方法的总反应为 。转化关系如下:
。转化关系如下:
②将X与
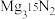 混合反应,证实了氮化镁中氮元素能转化为氨。不考虑其他副反应,产物中
混合反应,证实了氮化镁中氮元素能转化为氨。不考虑其他副反应,产物中
您最近一年使用:0次
名校
7 . 氨气是重要的含氮元素物质。
I. 工业上氨气是重要的化工产品及制备硝酸的原料。
(1)工业合成氨的化学方程式___________ 。
(2)氨的催化氧化是工业制硝酸的基础,写出化学方程式___________ 。
II.实验室常利用如图所示装置及药品制取干燥的氨气。___________ 。
(4)C处是收集氨气的装置,请将集气瓶中导管补充完整_______ 。
(5)证明氨气已收集满的操作和现象是___________ 。
I. 工业上氨气是重要的化工产品及制备硝酸的原料。
(1)工业合成氨的化学方程式
(2)氨的催化氧化是工业制硝酸的基础,写出化学方程式
II.实验室常利用如图所示装置及药品制取干燥的氨气。
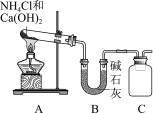
(4)C处是收集氨气的装置,请将集气瓶中导管补充完整
(5)证明氨气已收集满的操作和现象是
您最近一年使用:0次
名校
解题方法
8 . 利用下图所示装置及药品制取干燥的氨气。_______ 。
(2)C处是收集氨气的装置,请将集气瓶中导管补充完整_______ 。
(3)若A中只有 固体,不能制取
固体,不能制取 ,原因是
,原因是_______ (用化学方程式表示)。
(4)检验 固体中
固体中 的方法
的方法_______ 。
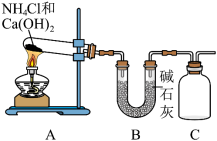
(2)C处是收集氨气的装置,请将集气瓶中导管补充完整
(3)若A中只有
 固体,不能制取
固体,不能制取 ,原因是
,原因是(4)检验
 固体中
固体中 的方法
的方法
您最近一年使用:0次
9 . 实验室用下图装置(夹持装置已略去)制备 ,并研究其性质。其中,
,并研究其性质。其中, 、
、 为湿润的红色石蕊试纸,下列说法不正确的是
为湿润的红色石蕊试纸,下列说法不正确的是
 ,并研究其性质。其中,
,并研究其性质。其中, 、
、 为湿润的红色石蕊试纸,下列说法不正确的是
为湿润的红色石蕊试纸,下列说法不正确的是
A.用装置甲制 ,试管中应加入的试剂为 ,试管中应加入的试剂为 固体 固体 |
B.装置乙中, 比 比 先变蓝 先变蓝 |
| C.装置丙中,产生大量白烟 |
| D.装置丁具有防止倒吸的作用,试剂可以用水 |
您最近一年使用:0次
名校
解题方法
10 . 利用下列实验装置图可以达到实验目的是
| A | B | C | D | |
| 实验目的 | 此装置可以形成Cu-Zn原电池 | 制取并干燥氨气 | 检验氨气极易溶于水 | 制取并收集二氧化氮 |
| 反应装置 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次