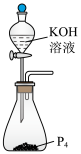
1 . 实验室在如图所示装置中制取 ,将
,将 通入
通入 溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得
溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得 晶体。已知:
晶体。已知: 呈蓝色。下列说法
呈蓝色。下列说法不正确 的是
 ,将
,将 通入
通入 溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得
溶液,当生成的蓝色沉淀溶解为深蓝色溶液,再滴加乙醇可获得 晶体。已知:
晶体。已知: 呈蓝色。下列说法
呈蓝色。下列说法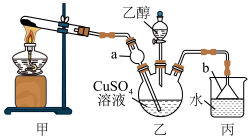
A.在装置甲试管中加入 和 和 固体加热制取 固体加热制取 |
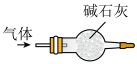
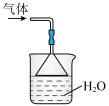
B.装置乙中的 和装置丙中的 和装置丙中的 均可防止倒吸 均可防止倒吸 |
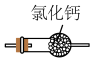
C. 晶体在乙醇中的溶解度小于在水中的溶解度 晶体在乙醇中的溶解度小于在水中的溶解度 |
D.与 相比, 相比, 更易与 更易与 形成配位键 形成配位键 |
您最近一年使用:0次
名校
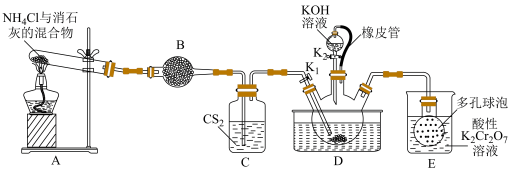
2 . 硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示:
(1)制备NH4SCN溶液
①实验前,经检验装置的气密性良好。其中装置B中的试剂是_______ 。
②实验开始时,打开K1,加热装置A、D,使A中产生的气体缓缓通入D中,发生反应
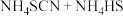 该反应比较缓慢),当看到
该反应比较缓慢),当看到_______ 现象时说明该反应接近完全。
(2)制备KSCN溶液:
①熄灭A处的酒精灯,关闭K2,移开水浴,将装置D继续加热至105℃,当NH4HS完全分解后(NH4HS=H2S↑+NH3↑),打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,发生反应的化学方程式为_______ 。
②装置E中多孔球泡的作用是_______ 。
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,蒸发浓缩、降温结晶,过滤、洗涤、干燥,得到硫氰化钾晶体。
补充完整实验步骤:测定晶体中KSCN的含量:称取10.0g样品,配成500mL溶液。量取20.00mL溶液于锥形瓶中,_______ 消耗标准溶液20.00mL(须使用的试剂:稀硝酸、Fe(NO3)3,0.1000mol/LAgNO3溶液)。
①滴定时发生的反应:SCN-+Ag+=AgSCN↓(白色)。则判断到达滴定终点的方法是_______ 。
②晶体中KSCN的质量分数为_______ (结果精确至0.1%)。
(1)制备NH4SCN溶液
①实验前,经检验装置的气密性良好。其中装置B中的试剂是
②实验开始时,打开K1,加热装置A、D,使A中产生的气体缓缓通入D中,发生反应

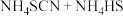 该反应比较缓慢),当看到
该反应比较缓慢),当看到(2)制备KSCN溶液:
①熄灭A处的酒精灯,关闭K2,移开水浴,将装置D继续加热至105℃,当NH4HS完全分解后(NH4HS=H2S↑+NH3↑),打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,发生反应的化学方程式为
②装置E中多孔球泡的作用是
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,蒸发浓缩、降温结晶,过滤、洗涤、干燥,得到硫氰化钾晶体。
补充完整实验步骤:测定晶体中KSCN的含量:称取10.0g样品,配成500mL溶液。量取20.00mL溶液于锥形瓶中,
①滴定时发生的反应:SCN-+Ag+=AgSCN↓(白色)。则判断到达滴定终点的方法是
②晶体中KSCN的质量分数为
您最近一年使用:0次
名校
解题方法
3 .  气体微溶于水,有强还原性,可由反应
气体微溶于水,有强还原性,可由反应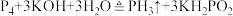 制得。实验室制取少量
制得。实验室制取少量 的原理及装置均正确的是
的原理及装置均正确的是
 气体微溶于水,有强还原性,可由反应
气体微溶于水,有强还原性,可由反应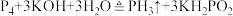 制得。实验室制取少量
制得。实验室制取少量 的原理及装置均正确的是
的原理及装置均正确的是
|
|
A.制取 | B.干燥 |
|
|
C.收集 | D.吸收尾气中的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 实验室制备NH3的实验原理及装置均正确的是
|
|
| A.制取氨气 | B.干燥氨气 |
|
|
| C.收集氨气 | D.吸收氨气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-27更新
|
575次组卷
|
2卷引用:江苏省南通市海安高级中学2024届高三下学期第二次模拟考试化学试题
名校
解题方法
5 . 下列有关氮、硫、氯的单质及其化合物的转化正确的是
A.工业制备漂白粉:饱和食盐水 Cl2 Cl2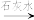 漂白粉 漂白粉 |
B.实验室制备NH3:Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O CaCl2+2NH3↑+2H2O |
C.工业制备硫酸:FeS2 SO3 SO3 H2SO4 H2SO4 |
| D.实验室制备SO2:Na2SO3+2HNO3=2NaNO3+SO2↑+H2O |
您最近一年使用:0次
2024-05-24更新
|
313次组卷
|
3卷引用:江苏省连云港高级中学2023-2024学年高三下学期4月期中考试化学试题
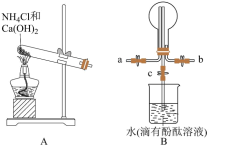
6 . 某化学实验小组同学利用如图所示装置制备氨气,并探究氨气的性质(部分仪器已略去)。___________ ;干燥氨气常用的干燥剂是___________ 。
(2)收集氨气时,请你选择氨气的进气口___________ (填“a”或“b”),理由是___________ 。
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是___________ 。
(2)收集氨气时,请你选择氨气的进气口
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
您最近一年使用:0次
名校
解题方法
7 . 实验室制取少量NH3并探究其性质。下列装置不能 达到实验目的的是
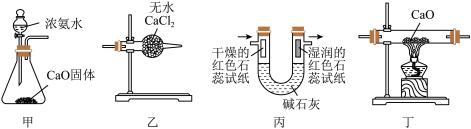
| A.用装置甲制取NH3 | B.用装置乙干燥NH3 |
| C.用装置丙检验NH3水溶液呈碱性 | D.用装置丁探究的NH3还原性 |
您最近一年使用:0次
2024-05-17更新
|
397次组卷
|
2卷引用:江苏省无锡市第一中学2023-2024学年高一下学期4月期中考试化学试题
解题方法
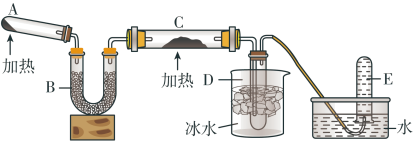
8 . 已知氨气具有还原性,可以与灼热的氧化铜反应生成两种单质和水,用下图中的装置可以实现该反应。
(1)A中加入的物质是两种固体,A中反应的化学方程式为______ 。
(2)仪器B中加入的物质是_______ (单选,填标号)。
a.碱石灰 b.无水氯化钙 c.无水硫酸铜 d.五氧化二磷
(3)实验时在C中观察到得现象是_______ ,发生反应的化学方程式为________ 。
(4)D中收集到的物质是_______ (选填“液氨”或“氨水”);将酚酞溶液滴到该物质中,出现的现象是_______ ,用电离方程式解释出现该现象的原因________ 。
(5)金属镁在E中收集到的气体中燃烧的化学方程式为_______ 。
(1)A中加入的物质是两种固体,A中反应的化学方程式为
(2)仪器B中加入的物质是
a.碱石灰 b.无水氯化钙 c.无水硫酸铜 d.五氧化二磷
(3)实验时在C中观察到得现象是
(4)D中收集到的物质是
(5)金属镁在E中收集到的气体中燃烧的化学方程式为
您最近一年使用:0次
9 . 某化学小组经查阅资料得知常温下过量的氨气和氯气反应能生成氯化铵,该实验小组对该反应进行探究,部分实验装置如下 夹持装置略去
夹持装置略去 。
。
(1)装置 是一种
是一种 的制备装置,其中盛放浓氨水的仪器名称为
的制备装置,其中盛放浓氨水的仪器名称为____ 。请再写出一种在实验室中制备 的反应原理
的反应原理_____  用化学方程式表示
用化学方程式表示 。
。
(2)装置F中发生反应的离子方程式为_____ 。
(3)装置 中盛装的试剂
中盛装的试剂 的为饱和食盐水,该装置的作用为
的为饱和食盐水,该装置的作用为______ 。
(4)装置C的设计有明显的不足之处,应该将左右的短长导管互换理由是:_____ 。
(5)利用改进后的实验装置完成实验,某同学设计如下实验证明装置C中所得固体为氯化铵:
①取少量装置C中固体产物溶于水配成溶液,取少量溶液置于两支小试管中;
②_____ ;
③向另一支试管中加入过量稀硝酸,再加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
结论:常温下过量的氨气和氯气反应可生成氯化铵。
 夹持装置略去
夹持装置略去 。
。 
(1)装置
 是一种
是一种 的制备装置,其中盛放浓氨水的仪器名称为
的制备装置,其中盛放浓氨水的仪器名称为 的反应原理
的反应原理 用化学方程式表示
用化学方程式表示 。
。(2)装置F中发生反应的离子方程式为
(3)装置
 中盛装的试剂
中盛装的试剂 的为饱和食盐水,该装置的作用为
的为饱和食盐水,该装置的作用为(4)装置C的设计有明显的不足之处,应该将左右的短长导管互换理由是:
(5)利用改进后的实验装置完成实验,某同学设计如下实验证明装置C中所得固体为氯化铵:
①取少量装置C中固体产物溶于水配成溶液,取少量溶液置于两支小试管中;
②
③向另一支试管中加入过量稀硝酸,再加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。 结论:常温下过量的氨气和氯气反应可生成氯化铵。
您最近一年使用:0次
名校
10 . 某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。
(1)实验室利用图中a装置作为制备氨气的发生装置时反应的化学方程式为_______ 。
(2)B装置中的干燥剂不能使用浓硫酸的原因是______ (用化学方程式表示)。
(3)气体通过C、D装置时,观察到的现象是________ 。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是_______ 。
(5)F装置中倒置漏斗的作用________ 。
(6)用5.35g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积是____ (写出计算过程)。
(7)氨气的用途很广。如可用氨气处理二氧化氮可获得两种对空气无污染的物质,其中之一是气态单质,反应的化学方程式为________ 。


(1)实验室利用图中a装置作为制备氨气的发生装置时反应的化学方程式为
(2)B装置中的干燥剂不能使用浓硫酸的原因是
(3)气体通过C、D装置时,观察到的现象是
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)F装置中倒置漏斗的作用
(6)用5.35g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积是
(7)氨气的用途很广。如可用氨气处理二氧化氮可获得两种对空气无污染的物质,其中之一是气态单质,反应的化学方程式为
您最近一年使用:0次