1 . 氨在人类的生产和生活中有着广泛的应用。某化学兴趣小组为了制取并探究氨气的性质,用下列装置(部分夹持装置已略去)进行实验。 装置,则该反应的化学方程式为
装置,则该反应的化学方程式为___________ 。
(2)B装置中的干燥剂可选用___________ (填名称)。
(3)气体通过C、D装置时,试纸颜色会发生变化的是___________ (填“C”或“D”)装置。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___________ ,发生该反应的化学方程式为___________ 。
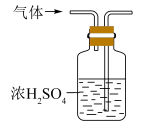
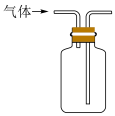
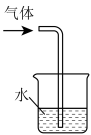
(5)F装置中倒置漏斗的作用是___________ ,与F有相同作用的装置为___________ (填序号)。
(6)氨的用途很广,如:①用氨处理二氧化氮: ,该反应中氨体现
,该反应中氨体现___________ (填“氧化性”或“还原性”);②工业上用氨气制硝酸,首先将氨气催化氧化,写出氨气催化氧化的化学方程式___________ 。
(7)氨气极易溶于水,会形成喷泉实验,实验装置如图所示。下列可以产生类似现象的组合为___________ 。

 装置,则该反应的化学方程式为
装置,则该反应的化学方程式为(2)B装置中的干燥剂可选用
(3)气体通过C、D装置时,试纸颜色会发生变化的是
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)F装置中倒置漏斗的作用是
|
|
|
| Ⅰ | Ⅱ | Ⅲ |
(6)氨的用途很广,如:①用氨处理二氧化氮:
 ,该反应中氨体现
,该反应中氨体现(7)氨气极易溶于水,会形成喷泉实验,实验装置如图所示。下列可以产生类似现象的组合为

| 圆底烧瓶(干燥气体) | 烧杯及胶头滴管(液体) | |
| A | NO | 水 |
| B |  | 4mol/L NaOH溶液 |
| C |  | 饱和NaCl溶液 |
| D |  | 1mol/L盐酸 |
您最近一年使用:0次
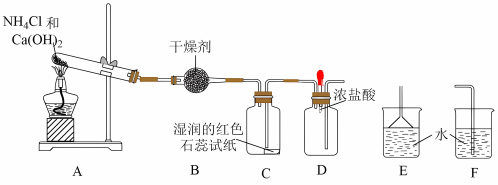
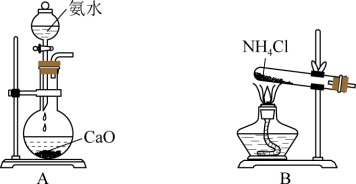
2 . 某实验小组利用以下装置制取氨气并探究氨气的性质:___________ 。
(2)装置B中的干燥剂是___________ (填名称)。
(3)装置C中的现象是___________ 。
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___________ ,发生反应的化学方程式为___________ 。
(5)验满方法
①把湿润的红色石蕊试纸置于试管口,试纸变___________ 。
②将蘸有浓盐酸的玻璃棒置于试管口,有___________ 产生。
(6)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置___________ (填
“E”或“F”)。
(7)实验室制取氨气,还可采用图中的___________ (填“A”或“B”)。
(2)装置B中的干燥剂是
(3)装置C中的现象是
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)验满方法
①把湿润的红色石蕊试纸置于试管口,试纸变
②将蘸有浓盐酸的玻璃棒置于试管口,有
(6)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置
“E”或“F”)。
(7)实验室制取氨气,还可采用图中的
您最近一年使用:0次
3 . 实验室模拟侯氏制碱,所用到的部分装置如图所示。下列叙述不正确的是

A.侯氏制碱法的关键反应为: |
B.实验时先从装置③的 口通入足量 口通入足量 ,再从 ,再从 口通入足量 口通入足量 |
| C.装置③中的尾气可用碱石灰吸收 |
D.装置④是连接在装置①、③之间的气体净化装置,进气口是 |
您最近一年使用:0次
名校
解题方法
4 . 实验室制取 的实验原理及装置均正确的是
的实验原理及装置均正确的是
 的实验原理及装置均正确的是
的实验原理及装置均正确的是
|
|
|
|
| A.制取NH3 | B.干燥NH3 | C.收集NH3 | D.吸收尾气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-13更新
|
685次组卷
|
5卷引用:新疆维霍尔果斯市苏港中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
5 . 下列实验中所选用的仪器或实验基本操作合理的是
①用10mL量筒准确量取稀硫酸溶液8.0mL;
②用浓硫酸干燥二氧化硫,用无水氯化钙干燥氨气;
③用干燥的pH试纸测定氯水的pH:
④用过滤的方法除去淀粉胶体中的氯化钠溶液:
⑤用饱和NaHCO3溶液除去CO2中的少量SO2;
⑥粗盐提纯的三个步骤中每一步都用的仪器是玻璃棒
①用10mL量筒准确量取稀硫酸溶液8.0mL;
②用浓硫酸干燥二氧化硫,用无水氯化钙干燥氨气;
③用干燥的pH试纸测定氯水的pH:
④用过滤的方法除去淀粉胶体中的氯化钠溶液:
⑤用饱和NaHCO3溶液除去CO2中的少量SO2;
⑥粗盐提纯的三个步骤中每一步都用的仪器是玻璃棒
| A.①③⑥ | B.②③④ | C.①③⑤ | D.①⑤⑥ |
您最近一年使用:0次
名校
解题方法
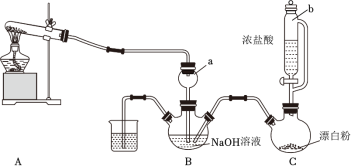
6 . 实验室模拟拉希法用氨气和次氯酸钠反应制备肼(N2H4),并探究肼的性质。制备装置如图所示。
已知:硫酸肼为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。
回答下列问题:
(1)装置C中仪器b的名称是_____ 。
(2)装置A试管中发生反应的化学方程式为_____ 。
(3)装置B中制备肼反应的离子方程式为_____ 。
(4)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是_____ 。
(5)①探究性质。取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,容器底部有无色晶体析出。过滤后用_____ 洗涤,洗涤是否完成,可通过检测洗出液中是否存在 来判断。检测的方法是
来判断。检测的方法是_____ 。
②测定产品中肼的质量分数。称取mg装置B中溶液,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成100mL溶液,移取25.00mL置于锥形瓶中,用cmol/L的碘溶液滴定,滴定过程中有无色无味无毒气体产生。终点消耗标准溶液VmL,产品中肼的质量分数表达式为_____ 。
已知:硫酸肼为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。

回答下列问题:
(1)装置C中仪器b的名称是
(2)装置A试管中发生反应的化学方程式为
(3)装置B中制备肼反应的离子方程式为
(4)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是
(5)①探究性质。取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,容器底部有无色晶体析出。过滤后用
 来判断。检测的方法是
来判断。检测的方法是②测定产品中肼的质量分数。称取mg装置B中溶液,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成100mL溶液,移取25.00mL置于锥形瓶中,用cmol/L的碘溶液滴定,滴定过程中有无色无味无毒气体产生。终点消耗标准溶液VmL,产品中肼的质量分数表达式为
您最近一年使用:0次
7 . 如图是氮元素的几种价态与物质类别的对应关系:
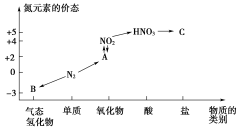
回答下列问题:
(1)写出B(氨气)的最重要的用途:________________________ 。
(2)从氮元素化合价分析,N2具有氧化性和还原性。N2表现氧化性时化合价:_________ (升高、降低、不变)
(3)HNO3与图中的物质C(硝酸盐)合用常用于检验Cl-的存在,则C的化学式为__________ 。
(4)实验室铵盐和熟石灰加热制取物质B的化学方程式为________________ 。
(5)NO2与水反应生成物质A和硝酸的化学方程式为_______________________ 。
(6)浓硝酸与木炭在加热条件下反应生成一种无色气体、一种红棕色气体、水,化学方程式为_________________ 。

回答下列问题:
(1)写出B(氨气)的最重要的用途:
(2)从氮元素化合价分析,N2具有氧化性和还原性。N2表现氧化性时化合价:
(3)HNO3与图中的物质C(硝酸盐)合用常用于检验Cl-的存在,则C的化学式为
(4)实验室铵盐和熟石灰加热制取物质B的化学方程式为
(5)NO2与水反应生成物质A和硝酸的化学方程式为
(6)浓硝酸与木炭在加热条件下反应生成一种无色气体、一种红棕色气体、水,化学方程式为
您最近一年使用:0次
名校
解题方法
8 . I.某化学自主实验小组利用如图所示装置探究 能否被
能否被 还原
还原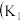 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。________ 。 装置发生的化学反应方程式为
装置发生的化学反应方程式为_________ 。
(2)甲、乙分别是___________  填标号
填标号 。
。
a.硫酸、浓硫酸 b.碱石灰、无水氯化钙 c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若 能够被
能够被 还原,写出发生反应的化学方程式:
还原,写出发生反应的化学方程式:___________ 。
(4)此实验装置存在一个明显的缺陷是___________ 。
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下: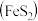 为原料来制备SO2,将黄铁矿粉碎的原因是:
为原料来制备SO2,将黄铁矿粉碎的原因是:___________ 。
(6)写出催化反应室中SO2被氧化为SO3的化学方程式___________ 。
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,可用___________ 吸收。
 能否被
能否被 还原
还原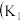 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。
 装置发生的化学反应方程式为
装置发生的化学反应方程式为(2)甲、乙分别是
 填标号
填标号 。
。a.硫酸、浓硫酸 b.碱石灰、无水氯化钙 c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若
 能够被
能够被 还原,写出发生反应的化学方程式:
还原,写出发生反应的化学方程式:(4)此实验装置存在一个明显的缺陷是
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下:
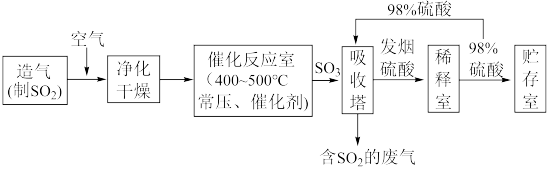
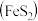 为原料来制备SO2,将黄铁矿粉碎的原因是:
为原料来制备SO2,将黄铁矿粉碎的原因是:(6)写出催化反应室中SO2被氧化为SO3的化学方程式
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,可用
您最近一年使用:0次
2024-02-24更新
|
738次组卷
|
5卷引用:新疆克孜勒苏柯尔克孜自治州第二中学2022-2023学年高一下学期期末考试化学试题
新疆克孜勒苏柯尔克孜自治州第二中学2022-2023学年高一下学期期末考试化学试题安徽省合肥市第一中学2023-2024学年高一下学期月考化学试题(一)广东省广州市黄广中学2023-2024学年高一下学期3月月考化学试题河南省三门峡市渑池县第二高级中学2023-2024学年高一下学期4月期中考试化学试题(已下线)期末押题卷01-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)
名校
9 . W、X、Y、Z是原子序数依次增大的同一周期主族元素,W是金属元素,X是地壳中含量最多的金属元素,且W、X的最高价氧化物的水化物相互反应生成盐和水;Y、Z是非金属元素,Y与W可形成离子化合物W2Y;G在Y的前一周期,其原子最外层比Y原子最外层少一个电子。
(1)X的原子结构示意图为___________ 。
(2)W、X的最高价氧化物的水化物相互反应的离子方程式为___________ 。
(3)G的气态氢化物的浓溶液与Z的气态氢化物浓溶液靠近会有何现象___________ ,实验室制备G的气态氢化物的方法(化学方程式表示)___________ 。
(4)在催化剂作用下,汽车尾气中G的氧化物GO与一氧化碳两种气体能相互反应转化为无污染、能参与大气循环的两种气体,写出有关反应的化学方程式___________ ;若有33.6L(已换算成标准状况)一氧化碳参加反应,转移的电子数为___________ 。
(5)X单质可以与NaNO3、NaOH混合溶液反应,产物中单质只有G的单质,写出反应的离子方程式___________ 。
(1)X的原子结构示意图为
(2)W、X的最高价氧化物的水化物相互反应的离子方程式为
(3)G的气态氢化物的浓溶液与Z的气态氢化物浓溶液靠近会有何现象
(4)在催化剂作用下,汽车尾气中G的氧化物GO与一氧化碳两种气体能相互反应转化为无污染、能参与大气循环的两种气体,写出有关反应的化学方程式
(5)X单质可以与NaNO3、NaOH混合溶液反应,产物中单质只有G的单质,写出反应的离子方程式
您最近一年使用:0次
名校
10 . 实验是化学的灵魂。用下列仪器或装置进行相应实验,能够达到实验目的的是
| 制作简单的燃料电池 | 制备并收集 | 除去 固体中少量的 固体中少量的 | 碳酸氢钠受热分解 |
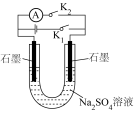 | 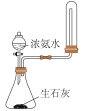 | 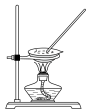 | 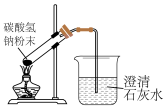 |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-23更新
|
207次组卷
|
3卷引用:新疆生产建设兵团第二中学2023-2024学年高三上学期12月月考化学题