名校
1 . 某化学实验小组为了探究氨气的性质设计了如图实验装置:
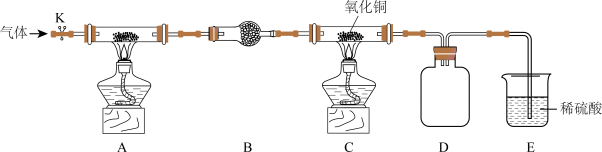
已知:CuO在高温时不稳定,会分解得到Cu2O,Cu2O粉末呈红色。
(1)实验前需先通入一段时间某气体,该气体可以是____ (填字母)。
a.空气b.氩气c.氢气
装置A用于制备氨气,选择的试剂通常是____ (填化学式)。
(2)装置D、E的作用分别是____ 、____ 。
(3)经实验测定NH3和CuO反应的产物有N2和Cu,则NH3和CuO反应的化学方程式为____ 。
(4)实验结束后装置c中黑色粉末变成红色,该红色粉末的成分能否确定?____ (填“能”或“否”)。请通过检验其他产物证明NH3和CuO发生了反应,简述实验方案:____ 。
(5)加热条件下,氨气可以与铝发生置换反应生成AlN;AlN性质稳定,加热时溶于浓碱溶液且可产生氨气。
①写出氨气与铝反应的化学方程式:____ 。
②称取AlN样品23.2g(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为14.56L(标准状况),则样品中AlN的质量分数为____ %(保留一位小数)。

已知:CuO在高温时不稳定,会分解得到Cu2O,Cu2O粉末呈红色。
(1)实验前需先通入一段时间某气体,该气体可以是
a.空气b.氩气c.氢气
装置A用于制备氨气,选择的试剂通常是
(2)装置D、E的作用分别是
(3)经实验测定NH3和CuO反应的产物有N2和Cu,则NH3和CuO反应的化学方程式为
(4)实验结束后装置c中黑色粉末变成红色,该红色粉末的成分能否确定?
(5)加热条件下,氨气可以与铝发生置换反应生成AlN;AlN性质稳定,加热时溶于浓碱溶液且可产生氨气。
①写出氨气与铝反应的化学方程式:
②称取AlN样品23.2g(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为14.56L(标准状况),则样品中AlN的质量分数为
您最近一年使用:0次
2022-07-12更新
|
390次组卷
|
3卷引用:河北省沧州市2021-2022学年高一下学期期末考试化学试题
2 . 氮化铬(CrN)是一种良好的耐磨材料,实验室可用如下装置进行模拟制备(省略夹持装置):

Ⅰ.完成下列填空:
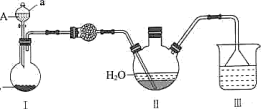
(1)干燥的NH3可选用以下装置制得,相应的连接顺序可以是_______→_______→_______(选填端口字母编号)。_______
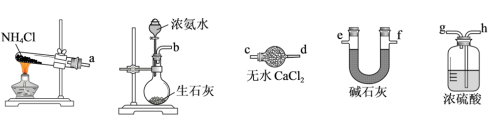
Ⅱ.固体X可用无水氯化铬(CrCl3)固体,主要反应为NH3+CrCl3 CrN+3HCl。
CrN+3HCl。
(2)无水氯化铬具有很强的吸水性,通常形成晶体CrCl3·6H2O。直接加热脱水往往得到Cr2O3,有关反应的化学方程式为_______ 。以氯化铬晶体制备无水氯化铬的方法是_______ 。
(3)实际进行实验时,发现上述装置存在一个缺陷,会导致危险,请简要说明。_______
Ⅲ.固体X也可用Cr2O3固体。通入NH3时先将氧化物还原为金属单质,然后金属单质与另一产物化合得到CrN,这些过程几乎同时进行。
(4)写出NH3与Cr2O3发生氧化还原反应的化学方程式:_______ 。
(5)CrN产品中含有Cr2N杂质,可利用如下方法进行纯度测定:取样品14.380g在空气中充分加热至反应完全,剩余固体全为Cr2O3,质量为16.720g。样品中CrN与Cr2N的物质的量之比为_______ 。
(6)证明样品已反应完全的操作名称是_______ ;若加热时长不足,则最终测定CrN的纯度将_______ (选填“偏大”“偏小”或“不变”)。

Ⅰ.完成下列填空:
(1)干燥的NH3可选用以下装置制得,相应的连接顺序可以是_______→_______→_______(选填端口字母编号)。

Ⅱ.固体X可用无水氯化铬(CrCl3)固体,主要反应为NH3+CrCl3
 CrN+3HCl。
CrN+3HCl。(2)无水氯化铬具有很强的吸水性,通常形成晶体CrCl3·6H2O。直接加热脱水往往得到Cr2O3,有关反应的化学方程式为
(3)实际进行实验时,发现上述装置存在一个缺陷,会导致危险,请简要说明。
Ⅲ.固体X也可用Cr2O3固体。通入NH3时先将氧化物还原为金属单质,然后金属单质与另一产物化合得到CrN,这些过程几乎同时进行。
(4)写出NH3与Cr2O3发生氧化还原反应的化学方程式:
(5)CrN产品中含有Cr2N杂质,可利用如下方法进行纯度测定:取样品14.380g在空气中充分加热至反应完全,剩余固体全为Cr2O3,质量为16.720g。样品中CrN与Cr2N的物质的量之比为
(6)证明样品已反应完全的操作名称是
您最近一年使用:0次
3 . 工业上用饱和食盐水吸收尾气 和
和 制备无水
制备无水 。同时得到副产物
。同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):

已知:浓硫酸的沸点为338℃。回答下列问题:
(1)仪器a的名称_______ ,导气管b的作用_______ 。
(2)装置A中发生的化学反应的化学方程式为_______ 。
(3)固、固加热制取氨气的发生装置可以选择下图中的_______ (填编号),反应的化学方程式为_______ 。

(4)利用各物质的溶解度曲线图(见图)分离产品,取出装置B中的溶液,蒸发浓缩,趁热过滤可得_______ ,然后将滤液_______ 、过滤、洗涤、干燥可得另一产物。

(5)产品中可能混有少量 和
和 杂质,混有
杂质,混有 杂质的原因可能是
杂质的原因可能是_______ ,检验产品中含有 的的实验方法:取少量样品于试管中,加入适量水溶解,
的的实验方法:取少量样品于试管中,加入适量水溶解,_______ 。
【可选试剂:稀硝酸、 溶液、酸性
溶液、酸性 溶液、
溶液、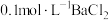 溶液、
溶液、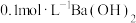 溶液、
溶液、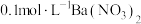 溶液】
溶液】
 和
和 制备无水
制备无水 。同时得到副产物
。同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
已知:浓硫酸的沸点为338℃。回答下列问题:
(1)仪器a的名称
(2)装置A中发生的化学反应的化学方程式为
(3)固、固加热制取氨气的发生装置可以选择下图中的

(4)利用各物质的溶解度曲线图(见图)分离产品,取出装置B中的溶液,蒸发浓缩,趁热过滤可得

(5)产品中可能混有少量
 和
和 杂质,混有
杂质,混有 杂质的原因可能是
杂质的原因可能是 的的实验方法:取少量样品于试管中,加入适量水溶解,
的的实验方法:取少量样品于试管中,加入适量水溶解,【可选试剂:稀硝酸、
 溶液、酸性
溶液、酸性 溶液、
溶液、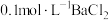 溶液、
溶液、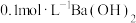 溶液、
溶液、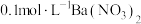 溶液】
溶液】
您最近一年使用:0次
2023-02-25更新
|
981次组卷
|
4卷引用:广东省茂名市电白区2021-2022学年高一下学期期末(选择性)考试化学试题
名校
4 . 叠氮化钠(NaN3)是一种重要的化工产品,可用于合成抗生素头孢菌素药物和用作汽车安全气囊的气源。实验室可通过以下流程制备叠氮化钠并测定其纯度。请回答以下问题:
I.制备氨基钠(反应原理为:2Na+2NH3 2NaNH2+H2)实验装置如图甲。
2NaNH2+H2)实验装置如图甲。
已知:氨基钠极易水解且易被空气氧化
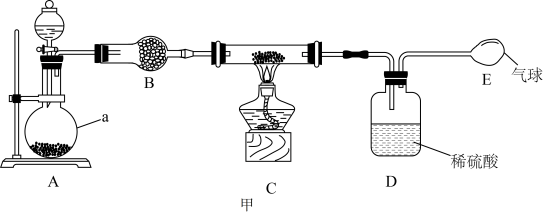
(1)仪器a的名称为___________ 。实验开始时,应先打开分液漏斗使浓氨水流下,目的是___________
(2)①B装置中的药品可选用___
A.P2O5 B.碱石灰 C.无水硫酸铜 D.无水氯化钙
②若无B装置,C中生成的氨基钠会发生的反应为___ (用化学方程式表示)
(3)某同学认为上述实验设计有缺陷,请对装置提出改正措施___
II.制备NaN3
(4)将I中制备的NaNH2与N2O在210-220℃的条件下反应生成NaN3、NaOH和氨气,反应容器不选用玻璃材质的原因是___________
III.测定NaN3的纯度
精确称量0.1500g NaN3样品,设计如图乙所示装置,连接好装置后使锥形瓶倾斜,使小试管中的NaN3样品与M溶液接触,测量产生的气体体积从而测定其纯度(不考虑溶剂的挥发)。
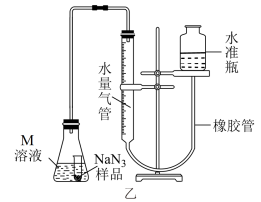
已知:2NaN3~3N2(其他产物略 ,反应中放出大量的热。
,反应中放出大量的热。
(5)对量气管读数时,反应前后都需要进行的操作是___________
(6)常温下测得产生气体的体积为54.00mL(N2的密度为1.400g/L),计算NaN3样品的纯度为___________ 。(保留三位有效数字)
I.制备氨基钠(反应原理为:2Na+2NH3
 2NaNH2+H2)实验装置如图甲。
2NaNH2+H2)实验装置如图甲。已知:氨基钠极易水解且易被空气氧化

(1)仪器a的名称为
(2)①B装置中的药品可选用
A.P2O5 B.碱石灰 C.无水硫酸铜 D.无水氯化钙
②若无B装置,C中生成的氨基钠会发生的反应为
(3)某同学认为上述实验设计有缺陷,请对装置提出改正措施
II.制备NaN3
(4)将I中制备的NaNH2与N2O在210-220℃的条件下反应生成NaN3、NaOH和氨气,反应容器不选用玻璃材质的原因是
III.测定NaN3的纯度
精确称量0.1500g NaN3样品,设计如图乙所示装置,连接好装置后使锥形瓶倾斜,使小试管中的NaN3样品与M溶液接触,测量产生的气体体积从而测定其纯度(不考虑溶剂的挥发)。

已知:2NaN3~3N2(其他产物略
 ,反应中放出大量的热。
,反应中放出大量的热。(5)对量气管读数时,反应前后都需要进行的操作是
(6)常温下测得产生气体的体积为54.00mL(N2的密度为1.400g/L),计算NaN3样品的纯度为
您最近一年使用:0次
2021-11-07更新
|
268次组卷
|
2卷引用:重庆市第八中学校2021-2022学年高三上学期第二次月考化学试题
5 . 硫氰化铵(NH4SCN)可以作为聚合反应和过氧化氢生产的催化剂,某化学实验小组在实验室条件下模拟制备少量样品,常压下的制备原理为: 。
。
步骤1:将装置Ⅰ中药品A以恒定的速度滴入装有药品B的烧瓶中,确保有稳定的氨气缓慢通入装置Ⅱ;
步骤2:装置Ⅱ加热至95°C,发生反应,观察到装置Ⅱ下层液体逐渐减少,直至近乎消失时停止通入氨气。
(1)取少量Ⅱ中反应后的溶液于试管中,滴加_______ 溶液,振荡,出现现象_______ ,得出结论产物中含有SCN-。
(2)设计实验证明产物中存在 :
:_______ (简述实验操作及现象)。
 。
。步骤1:将装置Ⅰ中药品A以恒定的速度滴入装有药品B的烧瓶中,确保有稳定的氨气缓慢通入装置Ⅱ;
步骤2:装置Ⅱ加热至95°C,发生反应,观察到装置Ⅱ下层液体逐渐减少,直至近乎消失时停止通入氨气。

(1)取少量Ⅱ中反应后的溶液于试管中,滴加
(2)设计实验证明产物中存在
 :
:
您最近一年使用:0次
6 . 工业上用饱和食盐水吸收尾气 和
和 制备无水
制备无水 ,同时得到副产物
,同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):

已知:浓硫酸的沸点为338℃.回答下列问题:
(1)仪器a的名称_______ ,导气管b的作用_______ .
(2)装置A中发生的化学反应的化学方程式为_______ .
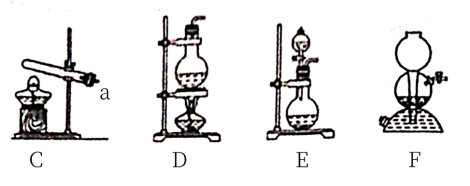
(3)氨气的发生装置可以选择下图中的_______ (填编号),反应的化学方程式为_______ .
(4)利用各物质的溶解度曲线图(见图)分离产品.取出装置B中的溶液,蒸发浓缩,趁热过滤可得_______ ,然后将滤液_______ 、过滤、洗涤、干燥可得另一产物.

(5)产品中可能混有少量 和
和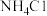 杂质,混有
杂质,混有 杂质的原因可能是
杂质的原因可能是_______ 检验产品中含有 的的实验方法:取少量样品于试管中,加入适量水溶解,
的的实验方法:取少量样品于试管中,加入适量水溶解,_______ 。【可选试剂:稀硝酸、 溶液、酸性
溶液、酸性 溶液、
溶液、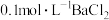 溶液、
溶液、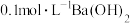 溶液、
溶液、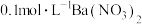 溶液】
溶液】
 和
和 制备无水
制备无水 ,同时得到副产物
,同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
已知:浓硫酸的沸点为338℃.回答下列问题:
(1)仪器a的名称
(2)装置A中发生的化学反应的化学方程式为
(3)氨气的发生装置可以选择下图中的

(4)利用各物质的溶解度曲线图(见图)分离产品.取出装置B中的溶液,蒸发浓缩,趁热过滤可得

(5)产品中可能混有少量
 和
和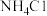 杂质,混有
杂质,混有 杂质的原因可能是
杂质的原因可能是 的的实验方法:取少量样品于试管中,加入适量水溶解,
的的实验方法:取少量样品于试管中,加入适量水溶解, 溶液、酸性
溶液、酸性 溶液、
溶液、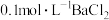 溶液、
溶液、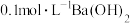 溶液、
溶液、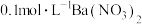 溶液】
溶液】
您最近一年使用:0次
名校
解题方法
7 . 某校实验小组的同学利用下图所示实验装置探究氨与氧化铜的反应(图中夹持、固定装置均略去)。
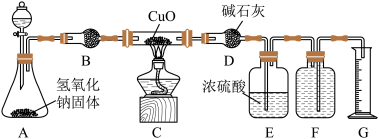
(1)按图设计组装好仪器,先__________________ ,再装入药品。
(2)A中分液漏斗内应装_________________ ,B中固体试剂为__________________ 。
(3)打开分液漏斗活塞,加入试剂,点燃C处的酒精灯,一段时间后,观察到C中氧化铜全部转化成光亮的红色固体,F中集气瓶内收集到一种无色气态单质。写出装置C中反应的化学方程式:______ 。
(4)E中浓硫酸的作用是__________________ 。
(5)用平衡移动原理解释A中产生气体的原因__________________________ 。(用相关的离子方程式和必要的文字描述)
(6)已知Cu2O也是红色的。下表为实验前后C装置的质量,通过计算可知反应后的产物中______ (填“有”、“无”或“无法确定”)Cu2O。

(1)按图设计组装好仪器,先
(2)A中分液漏斗内应装
(3)打开分液漏斗活塞,加入试剂,点燃C处的酒精灯,一段时间后,观察到C中氧化铜全部转化成光亮的红色固体,F中集气瓶内收集到一种无色气态单质。写出装置C中反应的化学方程式:
(4)E中浓硫酸的作用是
(5)用平衡移动原理解释A中产生气体的原因
(6)已知Cu2O也是红色的。下表为实验前后C装置的质量,通过计算可知反应后的产物中
| 空玻璃管 | 实验前(样品+玻璃管) | 实验后(样品+玻璃管) |
| 59.60 g | 65.60g | 64.64g |
您最近一年使用:0次



