名校
1 . 物质的类别和元素的化合价是研究物质性质的两个重要角度。回答下列问题:
I.硫元素在不同价态之间的转化为:
SO2 Na2SO3溶液
Na2SO3溶液 Na2S2O3溶液
Na2S2O3溶液
(1)“反应①”常使用NaOH溶液,该转化说明SO2的类别属于___________ 。
(2)欲制备Na2S2O3,从氧化还原的角度分析,“反应②”合理的是___________ (填标号)。
a.Na2SO3+Na2SO4 b.Na2SO3+S c.Na2SO3+Na2S2O5
II.某实验小组用铜片与浓硫酸反应并验证SO2性质的实验装置如图。
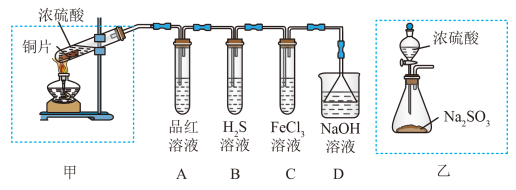
(3)装置A用于验证SO2的___________ 性,装置D的作用是___________ 。
(4)装置B的现象为___________ ,装置C的离子方程式为___________ 。
(5)若用装置乙代替装置甲,装置乙的优点是___________ (任写一点)。
(6)将28.8 g的铜片加入到25 mL 18 mol/L的硫酸中并加热,被还原的硫酸的物质的量为___________(填标号)。
I.硫元素在不同价态之间的转化为:
SO2
 Na2SO3溶液
Na2SO3溶液 Na2S2O3溶液
Na2S2O3溶液(1)“反应①”常使用NaOH溶液,该转化说明SO2的类别属于
(2)欲制备Na2S2O3,从氧化还原的角度分析,“反应②”合理的是
a.Na2SO3+Na2SO4 b.Na2SO3+S c.Na2SO3+Na2S2O5
II.某实验小组用铜片与浓硫酸反应并验证SO2性质的实验装置如图。

(3)装置A用于验证SO2的
(4)装置B的现象为
(5)若用装置乙代替装置甲,装置乙的优点是
(6)将28.8 g的铜片加入到25 mL 18 mol/L的硫酸中并加热,被还原的硫酸的物质的量为___________(填标号)。
| A.大于0.225 mol | B.等于0.225 mol |
| C.小于0.225 mol | D.在0.225 mol和0.45 mol之间 |
您最近一年使用:0次
2022-01-19更新
|
254次组卷
|
2卷引用:河南省南阳市邓州市第一高级中学校2023-2024学年高一上学期期末考试化学试题
名校
解题方法
2 . 下列实验目的、实验操作及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 验证肉桂醛中含碳碳双键 | 向肉桂醛( )中加入酸性KMnO4溶液 )中加入酸性KMnO4溶液 | 肉桂醛中含有碳碳双键 |
| B | 比较H2SO3与HClO的酸性强弱 | 往Ca(ClO)2溶液中通入SO2气体,有沉淀产生 | 酸性:H2SO3>HClO |
| C | 验证菠菜中含有铁元素 | 将新鲜菠菜剪碎、研磨、溶解、过滤,向滤液中加入几滴KSCN溶液,溶液不变红 | 说明菠菜中不含铁元素 |
| D | 判断强酸和弱酸 | NaHCO3溶液显碱性,NaHSO3溶液显酸性 | 可以确定H2CO3是弱酸,无法判断H2SO3是否为弱酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 .  2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
(1)硫酸亚铁加热至高温会分解,生成三种氧化物。为探究硫酸亚铁的分解产物,将无水硫酸亚铁装入反应管A并连接如图所示的装置,打开 1和
1和 2,缓缓通入
2,缓缓通入 2,加热。实验后反应管A中残留的固体为红色粉末
2,加热。实验后反应管A中残留的固体为红色粉末
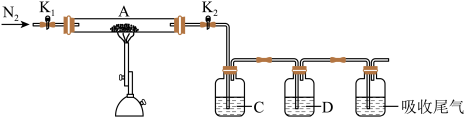
①装置C的溶液为_______ (填标号)。装置D可观察到的实验现象为_______ 。
a.品红 b.NaOH c. 2 d.
2 d. e.浓硫酸
e.浓硫酸
②写出硫酸亚铁高温分解的化学方程式_______ 。
(2)某兴趣小组用如图所示装置模拟测定空气中的二氧化硫的含量。当注入标准状况下VmL空气时,酸性 4溶液恰好褪色,停止实验。
4溶液恰好褪色,停止实验。
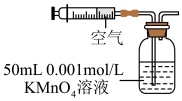
①二氧化硫和酸性 4溶液反应的离子方程式为
4溶液反应的离子方程式为_______ 。
②该空气中二氧化硫的体积分数为_______ (用含Ⅴ的代数式表示)。
(3)某化工厂用如图所示工艺流程除去燃煤产生的 2。
2。

①过程I发生的反应中,氧化剂与还原剂的物质的量之比为_______ 。
②过程Ⅱ发生反应的化学方程式为_______ 。
 2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:(1)硫酸亚铁加热至高温会分解,生成三种氧化物。为探究硫酸亚铁的分解产物,将无水硫酸亚铁装入反应管A并连接如图所示的装置,打开
 1和
1和 2,缓缓通入
2,缓缓通入 2,加热。实验后反应管A中残留的固体为红色粉末
2,加热。实验后反应管A中残留的固体为红色粉末
①装置C的溶液为
a.品红 b.NaOH c.
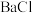 2 d.
2 d. e.浓硫酸
e.浓硫酸②写出硫酸亚铁高温分解的化学方程式
(2)某兴趣小组用如图所示装置模拟测定空气中的二氧化硫的含量。当注入标准状况下VmL空气时,酸性
 4溶液恰好褪色,停止实验。
4溶液恰好褪色,停止实验。
①二氧化硫和酸性
 4溶液反应的离子方程式为
4溶液反应的离子方程式为②该空气中二氧化硫的体积分数为
(3)某化工厂用如图所示工艺流程除去燃煤产生的
 2。
2。
①过程I发生的反应中,氧化剂与还原剂的物质的量之比为
②过程Ⅱ发生反应的化学方程式为
您最近一年使用:0次
解题方法
4 . 按要求填空。
(1)SO2性质多变,若将SO2气体通入H2S溶液中,能观察到的现象为_________ ,该反应中SO2表现出_________ 性;若将SO2气体通入酸性高锰酸钾溶液中,发生反应的离子方程式为_________ ,该反应中SO2表现出_________ 性。
(2)氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及氨催化氧化制硝酸的流程示意图。请回答下列问题。

①N2常用作保护气(如填充灯泡、焊接保护等),原因是_______ 。
②氧化炉中发生反应的化学方程式为_______ 。
③A为_______ (填化学式),向吸收塔中持续通入A的作用为_______ 。
④为避免硝酸工业尾气中氮的氧化物(以NO2为例)污染环境,可在“尾气处理装置”中盛装NaOH溶液(生成产物之一为NaNO2),相关反应的化学方程式为_______ 。
⑤汽车尾气中含有NO,NO产生的原因是_______ (用化学方程式表示)。
(1)SO2性质多变,若将SO2气体通入H2S溶液中,能观察到的现象为
(2)氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及氨催化氧化制硝酸的流程示意图。请回答下列问题。

①N2常用作保护气(如填充灯泡、焊接保护等),原因是
②氧化炉中发生反应的化学方程式为
③A为
④为避免硝酸工业尾气中氮的氧化物(以NO2为例)污染环境,可在“尾气处理装置”中盛装NaOH溶液(生成产物之一为NaNO2),相关反应的化学方程式为
⑤汽车尾气中含有NO,NO产生的原因是
您最近一年使用:0次
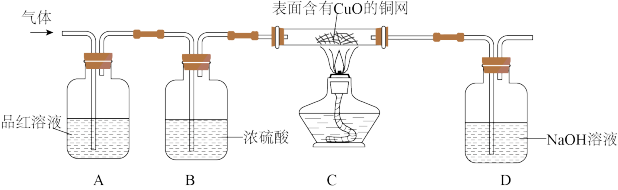
5 . 某化学兴趣小组进行锌与硫酸溶液反应的实验,并用大气球收集产生的气体。同学们在收集过程中闻到一股刺激性气味,同时发现充满气体的气球在空气中有些下沉,有些悬浮,还有些上浮。大家对这些现象很感兴趣,进行了相关探究活动。
【查阅资料】
(1)锌与浓硫酸反应生成硫酸锌、二氧化硫气体和水;铜与浓硫酸在加热的条件下生成硫酸铜、二氧化硫气体和水。
(2)SO2有刺激性气味,易溶于水,能使品红溶液褪色。SO2和CO2化学性质相似,都能和NaOH等碱溶液反应生成盐和水。
(3)相同条件下,气体的密度决定于该气体的相对分子质量,气体的相对分子质量越大密度也越大;空气的平均相对分子质量为29。
【提出猜想】
猜想一:气球内的气体为SO2;
猜想二:气球内的气体为SO2和H2;
猜想三:气球内的气体为H2。
【实验探究】针对上述猜想,同学们在老师的指导下设计了如图的装置(部分夹持器材略去),分别用不同气球内的气体进行探究。
(1)C装置在点燃酒精灯加热之前应先通一段时间的氮气,目的是___ 。
(2)甲同学观察到A中品红溶液褪色,C中无明显现象,说明猜想一正确。D瓶中氢氧化钠溶液的作用是___ 。
(3)乙同学观察到___ ,说明猜想二正确。
(4)丙同学观察到A中品红溶液无明显现象,C中铜网表面黑色物质变红,说明猜想三正确。
【实验结论】通过实验探究与充分思考,聪明的你应该对锌与硫酸溶液反应产生的气体填充气球活动中的异常现象能够很好的解释了。本次实验中锌粒与硫酸溶液反应先后生成二氧化硫气体和氢气。
【拓展反思】
(4)下列物质中不能由金属和稀硫酸反应直接得到的是___ 。
(5)浓硫酸与铜在加热的条件下反应生成硫酸铜、二氧化硫气体和水,而稀硫酸与铜即使加热也不能反应。这说明:某溶液的化学性质除了与溶质的性质有关外,还可能与下列中的有关___ (填序号)。
(6)锌与铜分别和浓硫酸在一定条件下都可以反应产生二氧化硫,若选择铜与浓硫酸在加热的条件下反应制取二氧化硫气体,其优点是___ 。
(7)实验中下沉的气球内一定含有的气体是___ 。(填化学式)
【查阅资料】
(1)锌与浓硫酸反应生成硫酸锌、二氧化硫气体和水;铜与浓硫酸在加热的条件下生成硫酸铜、二氧化硫气体和水。
(2)SO2有刺激性气味,易溶于水,能使品红溶液褪色。SO2和CO2化学性质相似,都能和NaOH等碱溶液反应生成盐和水。
(3)相同条件下,气体的密度决定于该气体的相对分子质量,气体的相对分子质量越大密度也越大;空气的平均相对分子质量为29。
【提出猜想】
猜想一:气球内的气体为SO2;
猜想二:气球内的气体为SO2和H2;
猜想三:气球内的气体为H2。
【实验探究】针对上述猜想,同学们在老师的指导下设计了如图的装置(部分夹持器材略去),分别用不同气球内的气体进行探究。
(1)C装置在点燃酒精灯加热之前应先通一段时间的氮气,目的是
(2)甲同学观察到A中品红溶液褪色,C中无明显现象,说明猜想一正确。D瓶中氢氧化钠溶液的作用是
(3)乙同学观察到
(4)丙同学观察到A中品红溶液无明显现象,C中铜网表面黑色物质变红,说明猜想三正确。
【实验结论】通过实验探究与充分思考,聪明的你应该对锌与硫酸溶液反应产生的气体填充气球活动中的异常现象能够很好的解释了。本次实验中锌粒与硫酸溶液反应先后生成二氧化硫气体和氢气。
【拓展反思】
(4)下列物质中不能由金属和稀硫酸反应直接得到的是
| A.Al2(SO4)3 | B.Fe2(SO4)3 | C.MgSO4 | D.ZnSO4 |
| A.溶质的质量分数 | B.溶液的质量 |
| C.溶液的体积 | D.溶质的相对分子质量 |
(7)实验中下沉的气球内一定含有的气体是
您最近一年使用:0次
2021-09-03更新
|
185次组卷
|
4卷引用:河南省南阳市镇平县第一高级中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
6 . 某化学兴趣小组利用如图1所示装置(夹持装置省略)制备MnSO4,已知MnSO4·H2O是一种易溶于水的白色或浅粉红色晶体,MnSO4在水中的溶解度与温度的关系如图所示。下列说法错误的是
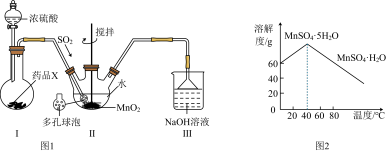
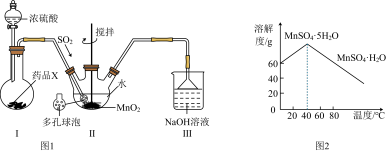
| A.装置I用来制备SO2,药品X为铜屑 |
| B.装置II中用到多孔球泡,这样可以增大SO2的吸收速率 |
| C.装置III用来吸收多余的SO2并可防止倒吸 |
| D.反应后的溶液经蒸发结晶、高于40℃趁热过滤、洗涤、干燥得晶体MnSO4·H2O |
您最近一年使用:0次
名校
解题方法
7 . 下列装置无法达到预期目的的是
A.喷泉实验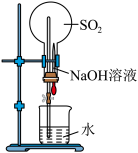 | B.干燥 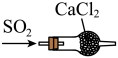 |
C.验证 的漂白性 的漂白性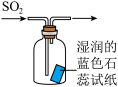 | D.制备 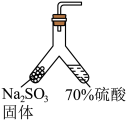 |
您最近一年使用:0次
名校
解题方法
8 . 下列装置可以用于相应实验的是
| A | B | C | D |
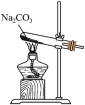 | 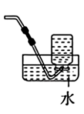 | 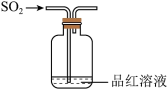 |  |
制备 | 收集NO2 | 验证 酸性 酸性 | 测量 体积 体积 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 某化学兴趣小组探究二氧化硫和氯气二者的制法和性质,做下列有关实验:
(一)实验室可由多种途径制取SO2。
途径I:Na2SO3固体与较浓的硫酸(约70%)反应制取;
途径II:铜与浓硫酸加热制取。
(1)如果要在实验室制取SO2,选用上述两种方法中的_____ (填“途径I”或“途径II”)更合理,你的理由是____________________ (答出一点就可)。
(2)用图1装置探究二氧化硫的性质:
①图1中倒扣漏斗的作用是__________________ 。
②写出途径I反应的化学方程式:____________________ 。
(二)如图3是用KMnO4与浓盐酸反应制取适量氯气的简易装置。
已知:2KMnO4+16HCI(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
(1)装置D的作用是:______________________ ;
(2)E中反应的离子方程式为____________________________ 。
(三)设计用下图装置探究二氧化硫、氯气的化学性质通过控制弹簧夹a、b,向装置A中分别通入不同气体,请完成如下问题:
(1)若关闭b,打开a,若X为品红溶液,则A中的现象为:________________ ,说明二氧化硫具有__________ 性。
(2)若关闭a,打开b,若X为紫色石蕊试液,则A中的现象为:________________ ,原因是________________ 。
(3)若同时打开a、b,且通入的气体体积比为1:1,若X为紫色石蕊试液,则A中的现象为___________________ 与②现象不同的原因是__________________ (书写相应的化学方程式)。
(一)实验室可由多种途径制取SO2。
途径I:Na2SO3固体与较浓的硫酸(约70%)反应制取;
途径II:铜与浓硫酸加热制取。
(1)如果要在实验室制取SO2,选用上述两种方法中的
(2)用图1装置探究二氧化硫的性质:
①图1中倒扣漏斗的作用是
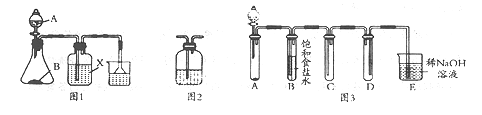
②写出途径I反应的化学方程式:
(二)如图3是用KMnO4与浓盐酸反应制取适量氯气的简易装置。
已知:2KMnO4+16HCI(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
(1)装置D的作用是:
(2)E中反应的离子方程式为
(三)设计用下图装置探究二氧化硫、氯气的化学性质通过控制弹簧夹a、b,向装置A中分别通入不同气体,请完成如下问题:
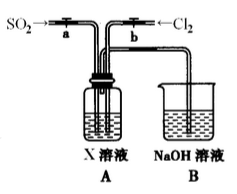
(1)若关闭b,打开a,若X为品红溶液,则A中的现象为:
(2)若关闭a,打开b,若X为紫色石蕊试液,则A中的现象为:
(3)若同时打开a、b,且通入的气体体积比为1:1,若X为紫色石蕊试液,则A中的现象为
您最近一年使用:0次
名校
解题方法
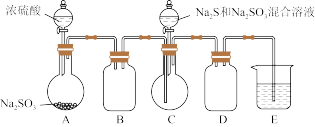
10 . 某小组同学用图装置 略去加热仪器等
略去加热仪器等 制备
制备 。
。
已知烧瓶 中发生反应如下:
中发生反应如下:
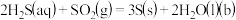

下列说法正确的是
 略去加热仪器等
略去加热仪器等 制备
制备 。
。
已知烧瓶
 中发生反应如下:
中发生反应如下:
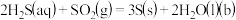

下列说法正确的是
A. 的稳定性比 的稳定性比 强 强 | B. 为 为 形分子 形分子 |
C. 与 与 的反应体现 的反应体现 的还原性 的还原性 | D. 、 、 的中心原子的轨道杂化类型为 的中心原子的轨道杂化类型为 |
您最近一年使用:0次
2022-09-10更新
|
169次组卷
|
3卷引用:河南省南阳市桐柏县实验高中2024届高三上学期阶段检测化学试题(12月)



