解题方法
1 . 如图是实验室制SO2并验证SO2某些性质的装置图,试回答:
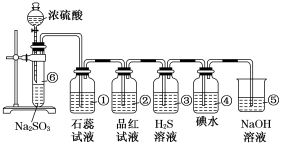
(1)①中实验现象为_______ ,证明SO2是 _______ 气体。
(2)②中品红溶液_______ ,证明SO2有_______ 性。
(3)③中现象是_______ ,证明SO2有_______ 性。
(4)④中现象是_______ ,证明SO2有_______ 性。
(5)⑤的作用是_______ ,反应的化学方程式为_______ 。

(1)①中实验现象为
(2)②中品红溶液
(3)③中现象是
(4)④中现象是
(5)⑤的作用是
您最近一年使用:0次
名校
解题方法
2 . 下面是某校化学研究性学习小组探究足量锌与浓硫酸反应的实验:
I.甲同学设计如图实验验证该反应产生的混合气体中含有SO2、H2、H2O,已知装置C中试剂过量。
A.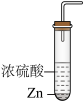 B.
B.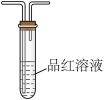 C.
C.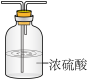 D.
D.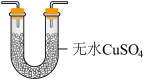 E.
E.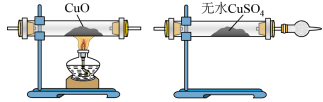 F.
F.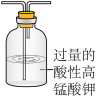
(1)写出A中生成SO2的化学方程式_______ 。
(2)若按气体从左到右的流向,气体流经的各装置连接顺序是_______ 。
(3)E中干燥管的作用是_______ 。
(4)证明混合气体中含有H2的实验现象为_______ 。
II.乙同学设计如下实验步骤测定44.8L(标准状况下)混合气体中SO2的体积分数。_______ (填序号)。
A.H2O2溶液 B.NaI溶液 C.溴水 D.浓硫酸
该混合气体中二氧化硫的体积分数为_______ (用含m的代数式表示)。
I.甲同学设计如图实验验证该反应产生的混合气体中含有SO2、H2、H2O,已知装置C中试剂过量。
A.
 B.
B. C.
C. D.
D. E.
E. F.
F.
(1)写出A中生成SO2的化学方程式
(2)若按气体从左到右的流向,气体流经的各装置连接顺序是
(3)E中干燥管的作用是
(4)证明混合气体中含有H2的实验现象为
II.乙同学设计如下实验步骤测定44.8L(标准状况下)混合气体中SO2的体积分数。
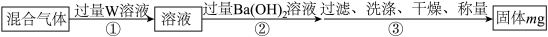
A.H2O2溶液 B.NaI溶液 C.溴水 D.浓硫酸
该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
2023-01-19更新
|
442次组卷
|
6卷引用:重庆市第八中学校2021-2022学年高一下学期第二次月考化学试题
重庆市第八中学校2021-2022学年高一下学期第二次月考化学试题河南省漯河市2020-2021学年高一上学期期末考试化学试题(已下线)5.1.2 硫酸 硫酸根离子的检验-2021-2022学年高一化学课后培优练(人教版2019必修第二册)(已下线)第04练 常见气体的制备与性质实验-2022年【暑假分层作业】高一化学(人教版2019必修第二册)山东省济宁市曲阜孔子高级中学2022-2023学年高一下学期4月月考化学试题湖南省岳阳市岳阳县第一中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
3 . 蛋白质是生命的物质基础。某学习小组通过实验探究一种蛋白质的元素组成。
I.确定该蛋白质中的某些组成元素
(1)为确定该蛋白质中含氮元素,将样品中有机氮转化成铵盐,能证明铵盐存在的实验方法是:____ 。
(2)为确定该蛋白质中含碳、氢、硫三种元素,采用如图装置进行研究,通入氧气使样品在装置A中充分燃烧,并使其产物依次缓缓通过其余装置。

①装置B中的试剂是_____ 。
②装置D的作用是____ 。
③当装置B、C、E、F依次出现下列现象:____ ,品红溶液褪色,____ ,出现白色浑浊;可证明燃烧产物中含有H2O、SO2、CO2。
结论:该蛋白质中含碳、氢、硫、氮等元素。
II.为测定该蛋白质中硫元素的质量分数,小组取蛋白质样品充分燃烧,先用足量碘水吸收二氧化硫,再取吸收液,以淀粉为指示剂,用硫代硫酸钠溶液滴定过量的碘。已知:2S2O +I2=S4O
+I2=S4O +2I—。
+2I—。
(3)写出二氧化硫与碘水反应的化学方程式:____ 。
(4)取蛋白质样品mg进行测定,采用c1mol·L–1的碘水V1mL进行吸收,滴定过量的碘时消耗c2mol·L–1硫代硫酸钠溶液V2mL。该蛋白质中的硫元素的质量分数为____ 。
(5)若燃烧时过量氧气进入吸收液中,可能会导致该蛋白质中的硫元素的质量分数测定值____ (填“偏大”或“偏小”或“无影响”)。
I.确定该蛋白质中的某些组成元素
(1)为确定该蛋白质中含氮元素,将样品中有机氮转化成铵盐,能证明铵盐存在的实验方法是:
(2)为确定该蛋白质中含碳、氢、硫三种元素,采用如图装置进行研究,通入氧气使样品在装置A中充分燃烧,并使其产物依次缓缓通过其余装置。

①装置B中的试剂是
②装置D的作用是
③当装置B、C、E、F依次出现下列现象:
结论:该蛋白质中含碳、氢、硫、氮等元素。
II.为测定该蛋白质中硫元素的质量分数,小组取蛋白质样品充分燃烧,先用足量碘水吸收二氧化硫,再取吸收液,以淀粉为指示剂,用硫代硫酸钠溶液滴定过量的碘。已知:2S2O
 +I2=S4O
+I2=S4O +2I—。
+2I—。(3)写出二氧化硫与碘水反应的化学方程式:
(4)取蛋白质样品mg进行测定,采用c1mol·L–1的碘水V1mL进行吸收,滴定过量的碘时消耗c2mol·L–1硫代硫酸钠溶液V2mL。该蛋白质中的硫元素的质量分数为
(5)若燃烧时过量氧气进入吸收液中,可能会导致该蛋白质中的硫元素的质量分数测定值
您最近一年使用:0次
名校
解题方法
4 . 某研究小组用如图装置制取 并对其性质进行相关实验(夹持装置已略去)。
并对其性质进行相关实验(夹持装置已略去)。
(1)装置A中发生反应的化学方程式为_______ 。
(2)D中观察到的现象是_______ ; 三支试管中的现象分别体现了
三支试管中的现象分别体现了 的漂白性、
的漂白性、_______ 性和_______ 性。
(3)写出C中反应的离子方程式:_______ 。
(4)仪器X的名称是_______ ;E装置的作用是_______ ,E装置中发生反应的化学方程式为_______ 。
(5)实验结束发现装置A中Y型试管产生白色固体,倾斜使左侧的物质全部转移到右侧水中,这时看到溶液的颜色为_______ 色。
 并对其性质进行相关实验(夹持装置已略去)。
并对其性质进行相关实验(夹持装置已略去)。
(1)装置A中发生反应的化学方程式为
(2)D中观察到的现象是
 三支试管中的现象分别体现了
三支试管中的现象分别体现了 的漂白性、
的漂白性、(3)写出C中反应的离子方程式:
(4)仪器X的名称是
(5)实验结束发现装置A中Y型试管产生白色固体,倾斜使左侧的物质全部转移到右侧水中,这时看到溶液的颜色为
您最近一年使用:0次
2022-10-08更新
|
220次组卷
|
2卷引用:重庆市巫山县官渡中学2021-2022学年高一下学期期末考试化学试题
5 . 下列关于实验现象与实验结论的描述正确的是
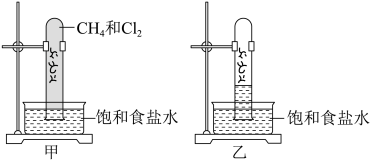

| A.实验室中用如图甲所示的装置进行甲烷与氯气在光照下反应的实验,光照下反应一段时间如图乙所示,说明黄绿色的氯气被消耗、有无色油状液体生成、试管内气体压强变小 |
| B.向溴水中加苯,震荡后溴水褪色,说明苯中含碳碳双键 |
C.向溴水中通入 气体,溴水褪色,说明 气体,溴水褪色,说明 有漂白性 有漂白性 |
D.向橙色的酸性 溶液中加入乙醇,溶液变为绿色(含 溶液中加入乙醇,溶液变为绿色(含 ),体现了乙醇的氧化性 ),体现了乙醇的氧化性 |
您最近一年使用:0次
名校
6 . 某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置略去)。
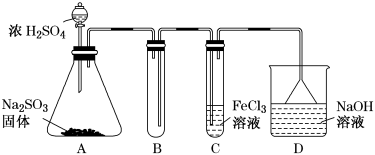
(1)通入足量SO2时C中观察到的现象为_______ 。
(2)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:_______ 。
②写出D溶液吸收尾气的离子方程式:_______ 。
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO 。该做法
。该做法_______ (填“合理”或“不合理”), 理由是_______ 。
(3)装置B的作用是_______ 。
(4)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有_______ (填序号)。
A.浓硫酸 B.酸性KMnO4溶液 C. NaCl 溶液 D.氯水 E.品红溶液

(1)通入足量SO2时C中观察到的现象为
(2)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:
②写出D溶液吸收尾气的离子方程式:
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO
 。该做法
。该做法(3)装置B的作用是
(4)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有
A.浓硫酸 B.酸性KMnO4溶液 C. NaCl 溶液 D.氯水 E.品红溶液
您最近一年使用:0次
名校
解题方法
7 . SO2是硫元素中一种重要物质。在生产生活中有着重要用途。
(1)某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。

①通入足量SO2时C中观察到的现象为____ 。
②根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
a.写出SO2与FeCl3溶液反应的离子方程式:____ 。
b.请设计实验方案检验溶液中是否还有Fe3+:____ 。
c.该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO 。该做法
。该做法____ (填“合理”或“不合理”),理由是____ 。
③为了验证SO2具有还原性,实验中可以代替FeCl3溶液的试剂有____ (填字母)。
A.浓硫酸 B.酸性KMnO4溶液 C.碘水 D.NaCl溶液
(2)某同学利用如图所示的装置研究SO2的性质:(熔点:SO2-76.1℃,SO316.8℃,沸点:SO2-10℃,SO345℃)

①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是____ 。
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅲ中溶液逐渐褪色,生成Mn2+,同时酸性增强,则该反应的离子方程式是(忽略O2的影响)____ 。
③乙同学按Ⅰ、Ⅱ、Ⅳ顺序连接装置,若装置Ⅳ中有50mL2.5mol·L-1NaOH溶液,反应后增重4.8g,则装置Ⅳ中发生反应的化学方程式是____ 。
(1)某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。

①通入足量SO2时C中观察到的现象为
②根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
a.写出SO2与FeCl3溶液反应的离子方程式:
b.请设计实验方案检验溶液中是否还有Fe3+:
c.该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO
 。该做法
。该做法③为了验证SO2具有还原性,实验中可以代替FeCl3溶液的试剂有
A.浓硫酸 B.酸性KMnO4溶液 C.碘水 D.NaCl溶液
(2)某同学利用如图所示的装置研究SO2的性质:(熔点:SO2-76.1℃,SO316.8℃,沸点:SO2-10℃,SO345℃)

①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅲ中溶液逐渐褪色,生成Mn2+,同时酸性增强,则该反应的离子方程式是(忽略O2的影响)
③乙同学按Ⅰ、Ⅱ、Ⅳ顺序连接装置,若装置Ⅳ中有50mL2.5mol·L-1NaOH溶液,反应后增重4.8g,则装置Ⅳ中发生反应的化学方程式是
您最近一年使用:0次
8 . 为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。

(1)该化学兴趣小组的同学为制取 、
、 气体,现采用
气体,现采用 与
与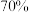 的硫酸为原料制取
的硫酸为原料制取 ,采用
,采用 和浓盐酸(12mol/L)为原料制取
和浓盐酸(12mol/L)为原料制取 。在此实验中,
。在此实验中, 仪器的作用是
仪器的作用是_______ ,E中应加入_______ 。
(2) 装置中主要反应的离子方程式为
装置中主要反应的离子方程式为_______ 。
(3)将适量的蔗糖放入烧杯中,加少量水拌匀,再加适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。“体积膨胀,并放出有刺激性气味的气体”,写出蔗糖变黑后与浓硫酸反应对应的化学方程式:_______ 。
(4)上述现象体现了浓硫酸的_______ (填序号)
①酸性 ②吸水性 ③脱水性 ④强氧化性
(5)向 浓硫酸中加入
浓硫酸中加入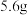 铜,加热一段时间后至不再反应为止,实验测得反应中共有
铜,加热一段时间后至不再反应为止,实验测得反应中共有 (标准状况下)
(标准状况下) 气体生成,反应中转移电子
气体生成,反应中转移电子_______  ,该反应中浓硫酸体现了
,该反应中浓硫酸体现了_______ 。

(1)该化学兴趣小组的同学为制取
 、
、 气体,现采用
气体,现采用 与
与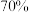 的硫酸为原料制取
的硫酸为原料制取 ,采用
,采用 和浓盐酸(12mol/L)为原料制取
和浓盐酸(12mol/L)为原料制取 。在此实验中,
。在此实验中, 仪器的作用是
仪器的作用是(2)
 装置中主要反应的离子方程式为
装置中主要反应的离子方程式为(3)将适量的蔗糖放入烧杯中,加少量水拌匀,再加适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。“体积膨胀,并放出有刺激性气味的气体”,写出蔗糖变黑后与浓硫酸反应对应的化学方程式:
(4)上述现象体现了浓硫酸的

①酸性 ②吸水性 ③脱水性 ④强氧化性
(5)向
 浓硫酸中加入
浓硫酸中加入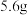 铜,加热一段时间后至不再反应为止,实验测得反应中共有
铜,加热一段时间后至不再反应为止,实验测得反应中共有 (标准状况下)
(标准状况下) 气体生成,反应中转移电子
气体生成,反应中转移电子 ,该反应中浓硫酸体现了
,该反应中浓硫酸体现了
您最近一年使用:0次
2022-04-02更新
|
443次组卷
|
2卷引用:重庆市实验中学2021-2022学年高一下学期第一次月考化学试题
名校
9 . 某实验小组利用如图装置模拟古法硫酸生产方法并进行SO2性质探究。
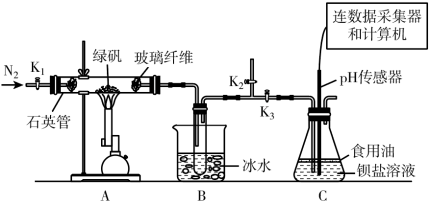
已知A中反应的化学方程式:2FeSO4·7H2O Fe2O3+SO2↑+SO3↑+14H2O,实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活塞K3,高温加热绿矾。
Fe2O3+SO2↑+SO3↑+14H2O,实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活塞K3,高温加热绿矾。
完成下列填空:
(1)C装置中覆盖食用油的目的是___________ ;B中所得硫酸溶液的质量分数理论值为___________ (保留三位有效数字)。
(2)该装置存在的不足之处为___________ 。
为探究SO2与钡盐溶液的反应,在装置C中先后四次加入不同的溶液:
得到如下pH-t图:

(3)曲线①呈缓慢下降趋势,这是因为___________ 。曲线②出现骤降,表明溶液中生成了___________ (填物质名称)。对比分析上述四组数据,可得出的结论是___________ (任写2条)。
(4)为对排气法收集到的SO2气体进行含量测定,将1120mL气体(已折算为标准状况)通入足量的Ba(NO3)2溶液中,经过滤、洗涤、烘干,最终得到沉淀10.718g.则SO2气体的体积分数为___________ (保留两位有效数字)。若该实验数据较实际值偏大,则可能的原因是___________ (选填序号)。
a.气体通入速率过快 b.沉淀未进行恒重操作
c.收集的气体中有CO2 d.未用食用油覆盖液面
(5)SO2属于大气污染物,还可用H2与其高温反应消除SO2带来的污染,其反应原理如图所示:
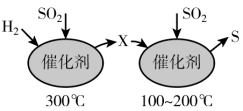
①反应原理过程中X为___________ (填名称)。
②写出检验X所需试剂及实验现象___________ 。

已知A中反应的化学方程式:2FeSO4·7H2O
 Fe2O3+SO2↑+SO3↑+14H2O,实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活塞K3,高温加热绿矾。
Fe2O3+SO2↑+SO3↑+14H2O,实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活塞K3,高温加热绿矾。完成下列填空:
(1)C装置中覆盖食用油的目的是
(2)该装置存在的不足之处为
为探究SO2与钡盐溶液的反应,在装置C中先后四次加入不同的溶液:
| ① | ② | ③ | ④ |
| 已煮沸的BaCl2溶液 | 未煮沸的BaCl2溶液 | 已煮沸的Ba(NO3)2溶液 | 未煮沸的Ba(NO3)2溶液 |
| 注:锥形瓶中溶液体积相同,钡盐溶液浓度相同;油层厚度一致,通入SO2流速一致。 | |||

(3)曲线①呈缓慢下降趋势,这是因为
(4)为对排气法收集到的SO2气体进行含量测定,将1120mL气体(已折算为标准状况)通入足量的Ba(NO3)2溶液中,经过滤、洗涤、烘干,最终得到沉淀10.718g.则SO2气体的体积分数为
a.气体通入速率过快 b.沉淀未进行恒重操作
c.收集的气体中有CO2 d.未用食用油覆盖液面
(5)SO2属于大气污染物,还可用H2与其高温反应消除SO2带来的污染,其反应原理如图所示:

①反应原理过程中X为
②写出检验X所需试剂及实验现象
您最近一年使用:0次
2022-03-19更新
|
597次组卷
|
3卷引用:重庆南开中学2021-2022学年高一下学期4月第一次月考化学试题
重庆南开中学2021-2022学年高一下学期4月第一次月考化学试题河南省六市2022届高三第一次联合调研检测理综化学试题 (已下线)预测卷07-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)
名校
解题方法
10 . SO2是硫元素的重要化合物,在生产、生活中有着广泛的应用。如图是实验室制取SO2并验证SO2的某些性质的装置(夹持装置和加热装置已略,气密性已检验),请回答下列问题:___________ ,单线桥标出上述反应中电子转移的方向和数目___________ ,生成标况下11.2LSO2,被还原的物质的质量为___________ g。
(2)i.②中的实验现象为___________ ,写出此化学反应方程式___________ 。
ii.④中的实验现象是___________ 。
iii.如何检验二氧化硫___________ 。
(3)能体现出SO2还原性的实验序号是___________ 。
(4)实验结束后需要通入N2,其目的是___________ 。

(2)i.②中的实验现象为
ii.④中的实验现象是
iii.如何检验二氧化硫
(3)能体现出SO2还原性的实验序号是
(4)实验结束后需要通入N2,其目的是
您最近一年使用:0次
2022-03-08更新
|
508次组卷
|
3卷引用:重庆南开中学2021-2022学年高一下学期4月第一次月考化学试题



