1 . 在实验室采用如图所示装置制备并收集气体,随开随用随关随停,其中合理的是


| 选项 | 化学试剂 | 制备的气体 |
| A | H2SO4(稀)+Zn | H2 |
| B | H2SO4(浓)+Na2SO3 | SO2 |
| C | HCl+CaCO3 | CO2 |
| D | HNO3(浓)+铝片 | NO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-10-18更新
|
360次组卷
|
2卷引用:2021年北京高考化学试题变式题1-10
2 . I.利用下图装置制备 ,并研究
,并研究 的性质。
的性质。
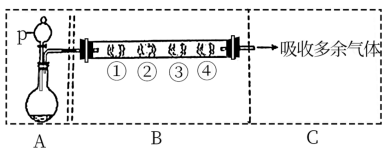
(1)A装置利用亚硫酸钠和硫酸反应制备 ,写出化学方程式
,写出化学方程式_______ 。
(2)填写下表
(3) 和氯气按照体积比
和氯气按照体积比 通入水中,溶液的漂白性
通入水中,溶液的漂白性_______ (填“增强”“减弱”“不变”)原因是_______ (用化学方程式表示)。
II.“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
,得到亚硫酸钠(Na2SO3)粗品。其流程如下:

(4)上述流程中,加入 后,发生反应的化学方程式为
后,发生反应的化学方程式为_______ 。
(5)亚硫酸钠粗品中含有少量 ,原因是
,原因是_______ 。
 ,并研究
,并研究 的性质。
的性质。
(1)A装置利用亚硫酸钠和硫酸反应制备
 ,写出化学方程式
,写出化学方程式(2)填写下表
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | 褪色 | 浅黄色 | ||
体现 的性质 的性质 |
(3)
 和氯气按照体积比
和氯气按照体积比 通入水中,溶液的漂白性
通入水中,溶液的漂白性II.“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为
 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
(4)上述流程中,加入
 后,发生反应的化学方程式为
后,发生反应的化学方程式为(5)亚硫酸钠粗品中含有少量
 ,原因是
,原因是
您最近一年使用:0次
名校
解题方法
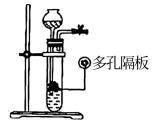
3 . 利用如图所示的装置制备气体可以控制反应,下列气体制备能选用如图所示装置的是

| 选项 | 试剂 | 制备气体 |
| A |  和 和 |  |
| B |  和稀硫酸 和稀硫酸 |  |
| C | 生石灰和浓氨水 |  |
| D |  和浓 和浓 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-08-29更新
|
1352次组卷
|
11卷引用:2021年北京高考化学试题变式题1-10
2021年北京高考化学试题变式题1-10甘肃省靖远县2021-2022学年高三上学期开学考试化学试题广东省大联考2022届高三上学期开学考试化学试题广东省2022届高三8月第二次联考化学试题河北省2022届高三上学期9月份开学摸底联考化学试题四川省广安市石永中学2021-2022学年高三上学期9月月考化学试题安徽省六安市第一中学2022届高三第二次月考化学试题(已下线)2021年高考全国乙卷化学试题变式题江西省宜春市上高二中2021-2022学年高三下学期第七次月考理综化学试题黑龙江省哈尔滨市第一中学校 2021-2022学年高三上学期期末考试理综化学试题 内蒙古莫力达瓦旗尼尔基第一中学2021-2022学年高三上学期期末考试化学试题
4 . 有试验装置如图,将Mg放在导热性良好的惰性金属片上置于C管中进行实验。实验步骤为:先关闭K,使A管中反应进行,加热玻璃管C,可观察到C管中发出耀眼的白光,管壁上附有淡黄色物质。实验完成后将C管中固体全部加入盐酸中,有臭鸡蛋气味的气体生成。B为橡胶气胆。
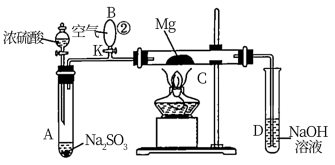
(1)C管中的Mg应放在不锈钢垫片上而不能直接接触管壁,这是因为_______ 。
(2)停止实验时,先打开K,再停止滴加浓硫酸并熄灭酒精灯。橡胶气胆B在实验中的作用是_______ 。
(3)C中全部反应产物有_______ 。
(4)检验气密性并盛放药品后,实验前应采取的措施是_______ ,其目的是_______ 。

(1)C管中的Mg应放在不锈钢垫片上而不能直接接触管壁,这是因为
(2)停止实验时,先打开K,再停止滴加浓硫酸并熄灭酒精灯。橡胶气胆B在实验中的作用是
(3)C中全部反应产物有
(4)检验气密性并盛放药品后,实验前应采取的措施是
您最近一年使用:0次
解题方法
5 . 硫和硒 在元素周期表中位于同一主族,均是生产生活中重要的非金属元素。
在元素周期表中位于同一主族,均是生产生活中重要的非金属元素。
(1)含 价硫元素的化合物有
价硫元素的化合物有 ,
, 和
和 等。
等。
① 能使品红溶液褪色,说明
能使品红溶液褪色,说明 具有的化学性质是
具有的化学性质是_______ 。
②已知 属于钠盐。写出
属于钠盐。写出 转化为
转化为 的化学方程式:
的化学方程式:_______ 。
③从下列试剂中任选一种试剂:浓硫酸、酸性高锰酸钾溶液、氯水、硫化钠溶液,设计实验证明 中硫元素的化合价在化学反应中可以发生变化,填写表格(写出一种方案即可)。
中硫元素的化合价在化学反应中可以发生变化,填写表格(写出一种方案即可)。
(2)以工业硒为原料制备高纯硒时的主要物质转化如图。
工业硒(Se)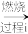 SeO2
SeO2 H2SeO3
H2SeO3 Se
Se 高纯硒
高纯硒
①下列说法正确的是_______ (填字母序号)。
a.硒原子的最外层有6个电子
b.硒元素的非金属性强于硫元素的非金属性
c. 属于酸性氧化物
属于酸性氧化物
d.过程ⅰ中硒被氧化
②过程ⅲ中使用的还原剂为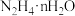 ,对应产物是
,对应产物是 。理论上,过程ⅰ消耗的
。理论上,过程ⅰ消耗的 与过程ⅲ消耗的
与过程ⅲ消耗的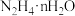 的物质的量之比为
的物质的量之比为_______ (工业硒中杂质与 的反应可忽略)。
的反应可忽略)。
 在元素周期表中位于同一主族,均是生产生活中重要的非金属元素。
在元素周期表中位于同一主族,均是生产生活中重要的非金属元素。(1)含
 价硫元素的化合物有
价硫元素的化合物有 ,
, 和
和 等。
等。①
 能使品红溶液褪色,说明
能使品红溶液褪色,说明 具有的化学性质是
具有的化学性质是②已知
 属于钠盐。写出
属于钠盐。写出 转化为
转化为 的化学方程式:
的化学方程式:③从下列试剂中任选一种试剂:浓硫酸、酸性高锰酸钾溶液、氯水、硫化钠溶液,设计实验证明
 中硫元素的化合价在化学反应中可以发生变化,填写表格(写出一种方案即可)。
中硫元素的化合价在化学反应中可以发生变化,填写表格(写出一种方案即可)。| 选择的试剂 | 转化后的含硫微粒 | 预期现象 |
(2)以工业硒为原料制备高纯硒时的主要物质转化如图。
工业硒(Se)
 SeO2
SeO2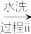 H2SeO3
H2SeO3 Se
Se 高纯硒
高纯硒①下列说法正确的是
a.硒原子的最外层有6个电子
b.硒元素的非金属性强于硫元素的非金属性
c.
 属于酸性氧化物
属于酸性氧化物d.过程ⅰ中硒被氧化
②过程ⅲ中使用的还原剂为
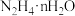 ,对应产物是
,对应产物是 。理论上,过程ⅰ消耗的
。理论上,过程ⅰ消耗的 与过程ⅲ消耗的
与过程ⅲ消耗的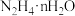 的物质的量之比为
的物质的量之比为 的反应可忽略)。
的反应可忽略)。
您最近一年使用:0次
6 . 利用下图所示装置制备气体,所用药品、收集方法均正确的是
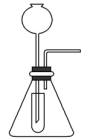

| 选项 | 制备气体 | 药品 | 除杂试剂 | 收集方法 |
| A | NH3 | 浓氨水、生石灰 | 碱石灰 | 排饱和NH4Cl溶液 |
| B | SO2 | 亚硫酸钠、浓硫酸 | Na2SO3溶液 | 向上排空气法 |
| C | CO2 | 石灰石、盐酸 | NaOH溶液 | 向上排空气法 |
| D | NO | 铜和稀硝酸 | 水 | 排水法 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-07-13更新
|
460次组卷
|
2卷引用:2021年北京高考化学试题变式题1-10
名校
7 . 某学习小组用下图所示实验检验浓硫酸与铜反应产生的二氧化硫(图中夹持装置已略去)。
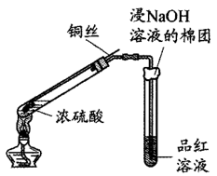
已知:浓硫酸的沸点为338℃,酒精灯外焰温度一般为500℃左右。
(1)浸有NaOH溶液的棉团作用是___________ 。
(2)能证明铜丝与浓硫酸反应产生了SO2的实验现象为___________ 。铜丝与浓硫酸反应的化学方程式为___________ 。
(3)将品红溶液换为Ba(OH)2溶液,发现其中产生白色沉淀。小组同学认为此现象不足以说明Cu和浓硫酸反应产生了SO2,其原因是___________ 。

已知:浓硫酸的沸点为338℃,酒精灯外焰温度一般为500℃左右。
(1)浸有NaOH溶液的棉团作用是
(2)能证明铜丝与浓硫酸反应产生了SO2的实验现象为
(3)将品红溶液换为Ba(OH)2溶液,发现其中产生白色沉淀。小组同学认为此现象不足以说明Cu和浓硫酸反应产生了SO2,其原因是
您最近一年使用:0次
2021-06-20更新
|
237次组卷
|
2卷引用:北京市海淀区2020-2021学年高一下学期学业水平合格性考试适应练习化学试题
名校
解题方法
8 . 实验小组设计图所示装置,验证SO2性质,对实验现象分析不正确的是

| A.通入SO2一段时间后,试管内时的CCl4溶液逐渐褪色,说明SO2具有还原性 |
| B.一段时间后试管内有白色沉淀,说明SO2与BaCl2反应生成BaSO3沉淀 |
| C.试管中的红色花瓣颜色变浅,说明SO2溶于水具有漂白性 |
| D.滴有酚酞的NaOH溶液红色变浅,说明SO2能与碱溶液反应 |
您最近一年使用:0次
2021-05-22更新
|
2254次组卷
|
11卷引用:北京市石景山区2021届高三一模化学试题
北京市石景山区2021届高三一模化学试题2021年北京高考化学试题变式题1-10(已下线)【浙江新东方】高中化学20210513-041【2021】【高一下】(已下线)第13讲 硫及其化合物(精练)-2022年高考化学一轮复习讲练测(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)江苏省苏州实验中学2021-2022学年第高一上学期12月月考调研化学试题广东省潮州市潮安区宝山中学2021-2022学年高一下学期期中考试化学试题(已下线)第13讲 硫及其化合物(练)-2023年高考化学一轮复习讲练测(全国通用)湖北省武汉海淀外国语实验学校2022-2023学年高三上学期10月月考化学试题安徽省当涂第一中学2023-2024学年高二上学期开学考试化学试题
名校
9 . 某小组同学用如图所示装置进行铜与浓硫酸的反应,并探究产物的性质。(夹持装置已略去)
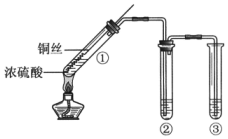
(1)试管①中反应的化学方程式是___________ ;
(2)若试管②中的试剂为品红溶液, 实验中观察到的现象是___________ ;若试管②中的试剂为酸性KMnO4溶液,实验时,观察到溶液褪色,则说明生成的气体具有___________ 性。
(3)试管③中的试剂为NaOH溶液,反应的离子方程式是___________ 。

(1)试管①中反应的化学方程式是
(2)若试管②中的试剂为品红溶液, 实验中观察到的现象是
(3)试管③中的试剂为NaOH溶液,反应的离子方程式是
您最近一年使用:0次
2021-05-13更新
|
121次组卷
|
2卷引用:北京三中2020-2021学年高一下学期期中考试化学试题
10 . 某实验小组欲探究SO2和Cl2能否发生反应,设计如图所示的实验装置进行实验。
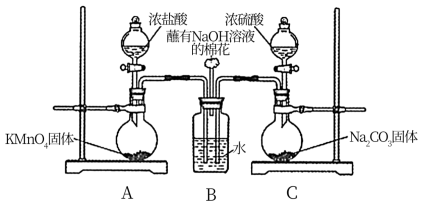
(1)装置A用来制备_______ 。
(2)装置C中发生复分解反应制取SO2,该反应的化学方程式:_______ 。
(3)为验证SO2和Cl2发生了反应,小组同学又继续如下实验。
①甲同学认为若SO2和Cl2反应,生成了Cl-,只要检验到生成的Cl-即可。
②乙同学认为甲同学的结论不合理,认为应该在装置A、B间增加一个洗气瓶,然后再按甲同学的方法实验即可得到正确结论。洗气瓶中盛有试剂的名称是_______ 。
③丙同学认为按乙同学的建议改进实验也不合理,理由是:_______ 。
④丁同学则认为甲、乙同学的结论均不合理。丁同学取适量B中溶液于试管中,向其中滴加少量溶液X,生成白色沉淀,得出结论:SO2与Cl2同时通入水中,可以发生反应。溶液X是_______ (填选项序号)。
a.BaCl2溶液b.Ba(OH)2溶液c.氯水d.石蕊溶液
 SO2与Cl2同时通入水中反应的化学方程式是
SO2与Cl2同时通入水中反应的化学方程式是_______

(1)装置A用来制备
(2)装置C中发生复分解反应制取SO2,该反应的化学方程式:
(3)为验证SO2和Cl2发生了反应,小组同学又继续如下实验。
①甲同学认为若SO2和Cl2反应,生成了Cl-,只要检验到生成的Cl-即可。
②乙同学认为甲同学的结论不合理,认为应该在装置A、B间增加一个洗气瓶,然后再按甲同学的方法实验即可得到正确结论。洗气瓶中盛有试剂的名称是
③丙同学认为按乙同学的建议改进实验也不合理,理由是:
④丁同学则认为甲、乙同学的结论均不合理。丁同学取适量B中溶液于试管中,向其中滴加少量溶液X,生成白色沉淀,得出结论:SO2与Cl2同时通入水中,可以发生反应。溶液X是
a.BaCl2溶液b.Ba(OH)2溶液c.氯水d.石蕊溶液
 SO2与Cl2同时通入水中反应的化学方程式是
SO2与Cl2同时通入水中反应的化学方程式是
您最近一年使用:0次



