名校
解题方法
1 . 磁性氧化铁因其特殊的超顺磁性,在巨磁电阻、磁性液体和磁记录、软磁、永磁、磁致冷、巨磁阻抗材料以及磁光器件、磁探测器等方面具有广阔的应用前景。以高硫铝土矿(主要含Al2O3、Fe2O3、SiO2和少量的FeS2等)为原料提取氧化铝和磁性氧化铁的流程如图:
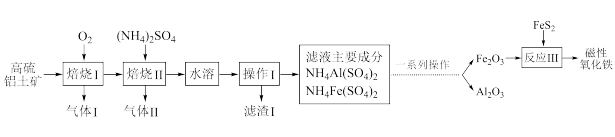
(1)磁性氧化铁的化学式为____ ;写出滤渣I中主要成分的一种用途:____ 。
(2)操作I在实验中要用到的玻璃仪器有____ 。
(3)焙烧I中,FeS2发生反应的化学方程式为____ 。
(4)焙烧I的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是____ (任答一点)。

(5)焙烧II中氧化铝参与反应的化学方程式为_____ 。
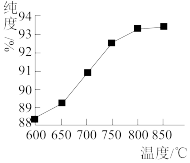
(6)反应III中加入FeS2的目的是作_____ (填“氧化剂”或“还原剂”)。反应Ⅲ的煅烧温度对磁性氧化铁的纯度有很大影响。已知温度对磁性氧化铁纯度的影响如图所示,则煅烧时,温度最好控制在____ ℃。
(7)滤液经过一系列操作可获得Al2O3,请简述这一系列操作的具体过程:_____ 。

(1)磁性氧化铁的化学式为
(2)操作I在实验中要用到的玻璃仪器有
(3)焙烧I中,FeS2发生反应的化学方程式为
(4)焙烧I的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是

(5)焙烧II中氧化铝参与反应的化学方程式为
(6)反应III中加入FeS2的目的是作

(7)滤液经过一系列操作可获得Al2O3,请简述这一系列操作的具体过程:
您最近一年使用:0次
2022-10-01更新
|
271次组卷
|
5卷引用:辽宁省县级重点高中联合体2022-2023学年高三上学期期中考试化学试题
名校
2 . 某厂利用富锗 烟尘(还含有
烟尘(还含有 等)生产储精矿和碱式碳酸锌
等)生产储精矿和碱式碳酸锌 。其流程如下:
。其流程如下:

已知:I.酸浸时,锰与铅元素被还原为 价,锗以
价,锗以 存在。
存在。
II. :
: 、
、 。
。
请回答下列问题:
(1)浸渣①主要含有___________ ;
(2)采取下列哪些措施可以提高锗的浸出率___________ (填代号);
A.增大烟尘与硫酸的固液比 B.多次反复浸出 C.适当进行搅拌
(3)流程中,“I”加入 粉主要是为了置换
粉主要是为了置换___________ (填离子符号);
(4)流程中,“II”控制 最高为
最高为___________ (溶液中金属离子浓度均按 计算),该步骤
计算),该步骤 不宜过低,除了考虑到锰的形态可能发生变化外,主要原因可能是
不宜过低,除了考虑到锰的形态可能发生变化外,主要原因可能是___________ ;
(5)流程中,“II”除锰反应的离子方程式为___________ ;
(6)沉锌的化学方程式为___________ 。
 烟尘(还含有
烟尘(还含有 等)生产储精矿和碱式碳酸锌
等)生产储精矿和碱式碳酸锌 。其流程如下:
。其流程如下:
已知:I.酸浸时,锰与铅元素被还原为
 价,锗以
价,锗以 存在。
存在。II.
 :
: 、
、 。
。请回答下列问题:
(1)浸渣①主要含有
(2)采取下列哪些措施可以提高锗的浸出率
A.增大烟尘与硫酸的固液比 B.多次反复浸出 C.适当进行搅拌
(3)流程中,“I”加入
 粉主要是为了置换
粉主要是为了置换(4)流程中,“II”控制
 最高为
最高为 计算),该步骤
计算),该步骤 不宜过低,除了考虑到锰的形态可能发生变化外,主要原因可能是
不宜过低,除了考虑到锰的形态可能发生变化外,主要原因可能是(5)流程中,“II”除锰反应的离子方程式为
(6)沉锌的化学方程式为
您最近一年使用:0次
2022-09-08更新
|
729次组卷
|
3卷引用:辽宁省鞍山市普通高中2022-2023学年高三第一次质量监测化学试题
解题方法
3 . 工业上重铬酸钾(K2Cr2O7)大量用于鞣革、印染、颜料、电镀等方面。以铬铁矿(主要成分可表示为FeO·Cr2O3,还含有Al2O3、Fe2O3、SiO2等杂质)为原料制备重铬酸钾(K2Cr2O7)的流程图如图所示:

提示:①Na2CrO4遇到酸性溶液会转化为Na2Cr2O7。
②重铬酸钾溶于水,不溶于乙醇。
(1)熔融物为块状固体,若想加快“水浸”时可溶性物质的溶解速度,可以采取的方法是_______ 。
(2)碱性溶液中硅的存在形式是_______ (写化合物),写出“调pH”除去水溶液中硅元素的离子方程式_______ 。
(3)写出酸化的目的是_______ 。
(4)Na2Cr2O7和K2Cr2O7两者相比,_______ 的溶解度的更高。
(5)写出从加入KCl反应之后得到的悬浊液中,提取干燥而纯净的K2Cr2O7晶体的操作步骤_______ 。
(6)写出在铬铁矿熔炉中生成Na2CrO4的化学方程式_______ 。

提示:①Na2CrO4遇到酸性溶液会转化为Na2Cr2O7。
②重铬酸钾溶于水,不溶于乙醇。
(1)熔融物为块状固体,若想加快“水浸”时可溶性物质的溶解速度,可以采取的方法是
(2)碱性溶液中硅的存在形式是
(3)写出酸化的目的是
(4)Na2Cr2O7和K2Cr2O7两者相比,
(5)写出从加入KCl反应之后得到的悬浊液中,提取干燥而纯净的K2Cr2O7晶体的操作步骤
(6)写出在铬铁矿熔炉中生成Na2CrO4的化学方程式
您最近一年使用:0次
4 . 钼系催化剂主要用于石油炼制和化学工业中。从废催化剂(主要成分为MoS、V2O5和Al2O3)中提取比较贵重的金属钒和钼,工艺流程如下:
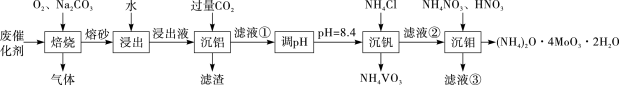
回答下列问题:
(1)“焙烧”时需对废催化剂进行粉碎,目的是_______ 。
(2)“焙烧”过程中MoS、V2O5和Al2O3均转化为对应的钠盐,写出MoS转化为Na2MoO4的化学方程式_______ 。
(3)“滤渣”的化学式为_______ 。滤液①的主要成分为Na2MoO4、_______ 。
(4)“沉钼”的离子方程式为_______ 。
(5)高温用 还原
还原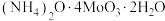 得金属钼,氧化剂与还原剂物质的量之比为
得金属钼,氧化剂与还原剂物质的量之比为_______ 。

回答下列问题:
(1)“焙烧”时需对废催化剂进行粉碎,目的是
(2)“焙烧”过程中MoS、V2O5和Al2O3均转化为对应的钠盐,写出MoS转化为Na2MoO4的化学方程式
(3)“滤渣”的化学式为
(4)“沉钼”的离子方程式为
(5)高温用
 还原
还原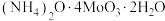 得金属钼,氧化剂与还原剂物质的量之比为
得金属钼,氧化剂与还原剂物质的量之比为
您最近一年使用:0次
2022-04-14更新
|
1666次组卷
|
4卷引用:辽宁省铁岭市六校协作体2022-2023学年高三上学期第一次联考化学试题
辽宁省铁岭市六校协作体2022-2023学年高三上学期第一次联考化学试题山东省青岛市2021-2022学年高三下学期第一次模拟考试化学试题(已下线)微专题25 化学工艺流程题-----原料的预处理-备战2023年高考化学一轮复习考点微专题(已下线)微专题26 化学工艺流程题-----核心反应与条件控制-备战2023年高考化学一轮复习考点微专题
名校
5 . 硫酸铁是一种重要的化工原料,用铁矿石(主要成分为 ,还含有少量的FeO、
,还含有少量的FeO、 、
、 、有机杂质)制备硫酸铁的流程如下:
、有机杂质)制备硫酸铁的流程如下: 既不与酸反应,也不与水反应。
既不与酸反应,也不与水反应。
(1)请写出“浸出”过程中 与
与 反应的离子方程式:
反应的离子方程式:_______ ;浸出时,一边加入稀硫酸,一边搅拌的目的是_______ 。
(2)“滤渣X”的成分为_______ 。
(3)“氧化”的目的是_______ ;过程中发生的离子方程式为_______ 。
(4)证明滤液中 已沉淀完全的实验操作和结论为
已沉淀完全的实验操作和结论为_______ 。
(5)用相似的工艺还可以制取另一种含铁硫酸盐晶体——绿矾。绿矾产品可以制取摩尔盐,摩尔盐是一种重要的化工原料,广泛应用于医药冶金等领域,其化学组成可表示为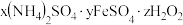 。为确定摩尔盐的组成,进行如下实验:
。为确定摩尔盐的组成,进行如下实验:
步骤一:称取一定量的新制摩尔盐,溶于水配制成100.00mL溶液A。
步骤二:准确量取10.00mL溶液A,加入足量 溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。
溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。
步骤三:另取10.00mL溶液A,加入0.0500
 酸性溶液,发生反应:
酸性溶液,发生反应: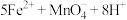
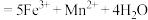 ,当两者恰好完全反应时,消耗
,当两者恰好完全反应时,消耗 溶液的体积为40.00mL。
溶液的体积为40.00mL。
通过计算确定摩尔盐中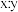 的值:
的值:_______ (写出计算过程)。
 ,还含有少量的FeO、
,还含有少量的FeO、 、
、 、有机杂质)制备硫酸铁的流程如下:
、有机杂质)制备硫酸铁的流程如下: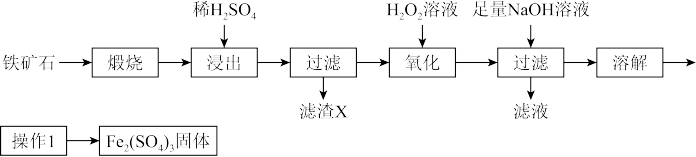
 既不与酸反应,也不与水反应。
既不与酸反应,也不与水反应。(1)请写出“浸出”过程中
 与
与 反应的离子方程式:
反应的离子方程式:(2)“滤渣X”的成分为
(3)“氧化”的目的是
(4)证明滤液中
 已沉淀完全的实验操作和结论为
已沉淀完全的实验操作和结论为(5)用相似的工艺还可以制取另一种含铁硫酸盐晶体——绿矾。绿矾产品可以制取摩尔盐,摩尔盐是一种重要的化工原料,广泛应用于医药冶金等领域,其化学组成可表示为
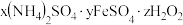 。为确定摩尔盐的组成,进行如下实验:
。为确定摩尔盐的组成,进行如下实验:步骤一:称取一定量的新制摩尔盐,溶于水配制成100.00mL溶液A。
步骤二:准确量取10.00mL溶液A,加入足量
 溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。
溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。步骤三:另取10.00mL溶液A,加入0.0500

 酸性溶液,发生反应:
酸性溶液,发生反应: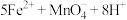
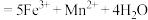 ,当两者恰好完全反应时,消耗
,当两者恰好完全反应时,消耗 溶液的体积为40.00mL。
溶液的体积为40.00mL。通过计算确定摩尔盐中
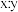 的值:
的值:
您最近一年使用:0次
2022-02-23更新
|
372次组卷
|
4卷引用:辽宁省朝阳市凌源市2021-2022学年高一上学期期末考试化学试题
辽宁省朝阳市凌源市2021-2022学年高一上学期期末考试化学试题吉林省梅河口市第五中学2021-2022学年高一上学期期末联考化学试题吉林省松原市重点高中2021-2022学年高一3月联考化学试题(已下线)综合突破02 期末压轴80题之非选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
6 . 碳酸铈[ ]是一种优良的环保材料,可用作汽车尾气净化催化剂。磷铈镧矿中铈(Ce)主要以
]是一种优良的环保材料,可用作汽车尾气净化催化剂。磷铈镧矿中铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以磷铈镧矿为原料制备
等物质。以磷铈镧矿为原料制备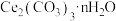 的工艺流程如下:
的工艺流程如下:
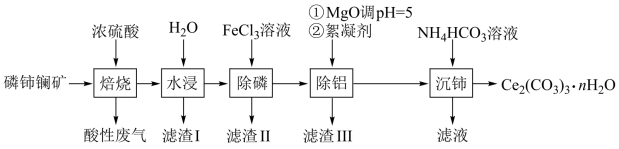
回答下列问题:。
(1)铈的核电荷数为58,其某种核素含有82个中子,该核素的符号为___________ 。
(2)焙烧时不能使用陶瓷容器的原因是___________ 。
(3)滤渣III的主要成分能溶于NaOH溶液,所得产物的化学式是___________ 。
(4)滤渣II的主要成分 在高温条件与
在高温条件与 、葡萄糖(
、葡萄糖( )反应可制备电极材料
)反应可制备电极材料 ,同时生成CO和
,同时生成CO和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(5)沉铈过程中生成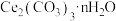 的离子方程式为
的离子方程式为___________ ,分离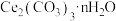 的操作名称是
的操作名称是___________ 。
 ]是一种优良的环保材料,可用作汽车尾气净化催化剂。磷铈镧矿中铈(Ce)主要以
]是一种优良的环保材料,可用作汽车尾气净化催化剂。磷铈镧矿中铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以磷铈镧矿为原料制备
等物质。以磷铈镧矿为原料制备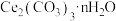 的工艺流程如下:
的工艺流程如下:
回答下列问题:。
(1)铈的核电荷数为58,其某种核素含有82个中子,该核素的符号为
(2)焙烧时不能使用陶瓷容器的原因是
(3)滤渣III的主要成分能溶于NaOH溶液,所得产物的化学式是
(4)滤渣II的主要成分
 在高温条件与
在高温条件与 、葡萄糖(
、葡萄糖( )反应可制备电极材料
)反应可制备电极材料 ,同时生成CO和
,同时生成CO和 ,该反应的化学方程式为
,该反应的化学方程式为(5)沉铈过程中生成
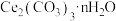 的离子方程式为
的离子方程式为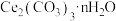 的操作名称是
的操作名称是
您最近一年使用:0次
2021-10-11更新
|
818次组卷
|
7卷引用:一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)
(已下线)一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)(已下线)2022年湖南卷高考真题变式题(15-19)山东省潍坊市2022届高三10月份阶段性检测化学试题山东省潍坊市五县市2022届高三上学期第一次联考化学试题山东省济南市2021-2022学年高三上学期10月阶段性检测化学试题山东省济南市山东师范大学附属中学2021-2022学年高三上学期期中考试化学试题山东省菏泽市第一中学2023-2024学年高三上学期9月月考化学试题
名校
7 . 硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如图:
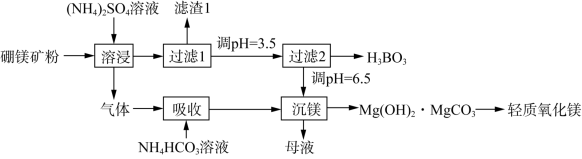
已知:H3BO3的解离反应:H3BO3+H2O H++[B(OH)4]-,Ka=5.81×10-10。下列说法不正确的是
H++[B(OH)4]-,Ka=5.81×10-10。下列说法不正确的是

已知:H3BO3的解离反应:H3BO3+H2O
 H++[B(OH)4]-,Ka=5.81×10-10。下列说法不正确的是
H++[B(OH)4]-,Ka=5.81×10-10。下列说法不正确的是| A.在95℃“溶浸”硼镁矿粉,产生的气体为NH3 |
| B.可选用KCSN溶液检验“过滤1”后的滤液中是否含有Fe3+离子 |
| C.在“过滤2”前,将溶液pH调节至3.5,主要目的是除去Fe3+和Al3+ |
| D.H3BO3与足量NaOH溶液反应的化学方程式:NaOH+H3BO3=Na[B(OH)4] |
您最近一年使用:0次
2021-05-23更新
|
1104次组卷
|
6卷引用:辽宁省沈阳市第二中学2022-2023学年高三10月月考化学试题
辽宁省沈阳市第二中学2022-2023学年高三10月月考化学试题湖南省湘潭市湘潭县第一中学2021-2022学年高三下学期5月月考化学试题(已下线)易错点08 金属材料-备战2023年高考化学考试易错题重庆市江津中学、铜梁中学、长寿中学等七校联盟2021届高三下学期第三次模拟考试化学试题重庆市长寿中学2021届高三5月考前模拟化学试题(已下线)2021年秋季高三开学摸底考化学试卷01(江苏专用)



