名校
解题方法
1 . 铝土矿(主要成分为 ,还含有
,还含有 、
、 )是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如图。
)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如图。

(1)沉淀A的化学式为_______ ,试剂b的化学式为_______ 。
(2)检验滤液甲中 时使用的试剂为
时使用的试剂为_______ 。
(3)步骤②中加入过量b时,生成沉淀B的离子反应方程式为_______ ;得到滤液乙的离子反应方程式为_______ 。
(4)步骤③中通入过量 气体而不加入过量盐酸的理由是
气体而不加入过量盐酸的理由是_______ 。
(5)准确称取8g铝土矿样品,加入一定量试剂a的溶液,使其中的 、
、 ,恰好溶解;然后向滤液中加入
,恰好溶解;然后向滤液中加入 的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中
的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中 的质量分数为
的质量分数为_______ 。

 ,还含有
,还含有 、
、 )是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如图。
)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如图。
(1)沉淀A的化学式为
(2)检验滤液甲中
 时使用的试剂为
时使用的试剂为(3)步骤②中加入过量b时,生成沉淀B的离子反应方程式为
(4)步骤③中通入过量
 气体而不加入过量盐酸的理由是
气体而不加入过量盐酸的理由是(5)准确称取8g铝土矿样品,加入一定量试剂a的溶液,使其中的
 、
、 ,恰好溶解;然后向滤液中加入
,恰好溶解;然后向滤液中加入 的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中
的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中 的质量分数为
的质量分数为
您最近一年使用:0次
2022-12-28更新
|
227次组卷
|
2卷引用:陕西省渭南市华阴市2021-2022学年高一上学期期末考试化学试题
名校
解题方法
2 . 电解铝技术的出现与成熟让铝从皇家珍品变成汽车、轮船、航天航空制造、化工生产等行业的重要材料。工业上用铝土矿(主要成分为Al2O3,Fe2O3、SiO2等(二氧化硅是酸性氧化物))提取纯Al2O3做冶炼铝的原料,某研究性学习小组设计了如下提取流程图

(1)固体Ⅰ、Ⅱ的化学式分别为____________ 、________________ ;
(2)操作Ⅰ所需玻璃仪器有____________________ ;
(3)写出流程③主要离子方程式______________________ ;
(4)验证滤液Ⅰ中是否含Fe3+,可取少量滤液A并加入_______ (填试剂名称),现象是_______ ;
(5)从铝土矿中提取铝的过程不涉及的化学反应类型是__________;
(6)生产过程中除CaO、CO2可以循环使用外,还可以循环使用的物质有________ ;(填化学式)
(7)若向滤液I中逐滴滴入NaOH溶液至过量,产生沉淀随NaOH滴入关系正确的是_______

(1)固体Ⅰ、Ⅱ的化学式分别为
(2)操作Ⅰ所需玻璃仪器有
(3)写出流程③主要离子方程式
(4)验证滤液Ⅰ中是否含Fe3+,可取少量滤液A并加入
(5)从铝土矿中提取铝的过程不涉及的化学反应类型是__________;
| A.复分解反应 | B.氧化还原反应 | C.置换反应 | D.分解反应 |
(7)若向滤液I中逐滴滴入NaOH溶液至过量,产生沉淀随NaOH滴入关系正确的是_______
A. | B.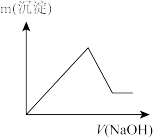 |
C. | D. |
您最近一年使用:0次
2022-12-16更新
|
260次组卷
|
3卷引用:陕西省西安市西北工业大学附属中学2022-2023学年高一上学期第二次月考化学试题
名校
解题方法
3 . 为探索工业含铝、铁、铜合金废料的再利用,某同学设计的回收利用方案如下:

(1)滤渣 的主要成分为
的主要成分为__________ ,溶液F的主要成分为__________ 。
(2)检验滤液 是否含有
是否含有 的方法为
的方法为__________ 。
(3)从滤液 得到绿矾晶体,须进行的操作为:
得到绿矾晶体,须进行的操作为:__________ 、__________ 、过滤洗涤、干燥。
(4)试剂 可能为__________。
可能为__________。
(5)若气体 为
为 ,请写出“滤液
,请写出“滤液 ”与过量气体
”与过量气体 反应的离子方程式:
反应的离子方程式:__________ 。

(1)滤渣
 的主要成分为
的主要成分为(2)检验滤液
 是否含有
是否含有 的方法为
的方法为(3)从滤液
 得到绿矾晶体,须进行的操作为:
得到绿矾晶体,须进行的操作为:(4)试剂
 可能为__________。
可能为__________。| A.NO | B.O2 | C.SO2 | D.H2O2 |
 为
为 ,请写出“滤液
,请写出“滤液 ”与过量气体
”与过量气体 反应的离子方程式:
反应的离子方程式:
您最近一年使用:0次
2022-12-12更新
|
96次组卷
|
2卷引用:陕西省咸阳市高新一中2022—2023学年高三上学期第四次质量检测化学试题
名校
4 . 某工业矿渣中主要含有Cu2O,还有少部分Al2O3、Fe2O3、SiO2 ,从该矿渣中提取铜的操作流程如下:(已知:Cu2O+2H+═Cu+Cu2++H2O)

(1)固体混合物B与氢氧化钠溶液反应的化学方程式为_______ 。
(2)滤液A中铁元素的存在形式只能为Fe2+,理由是(用涉及反应的离子方程式解释,不必书写Cu2O与盐酸的反应)_______ 、_______ 。检验滤液A中Fe2+的试剂为_______ 。
(3)若将滤液C中的铝元素以沉淀形式析出,可选用的最佳试剂为_______(填序号)。
(4)金属E与固体F某一成分发生的反应可用于焊接钢轨,该反应的化学方程式_______

(1)固体混合物B与氢氧化钠溶液反应的化学方程式为
(2)滤液A中铁元素的存在形式只能为Fe2+,理由是(用涉及反应的离子方程式解释,不必书写Cu2O与盐酸的反应)
(3)若将滤液C中的铝元素以沉淀形式析出,可选用的最佳试剂为_______(填序号)。
| A.氢氧化钠溶液 | B.硫酸溶液 | C.氨水 | D.二氧化碳 |
您最近一年使用:0次
名校
解题方法
5 . 某研究小组以工厂废渣(Fe3O4、Al2O3、SiO2)为原料制取Fe2O3工艺流程如图。回答下列问题:
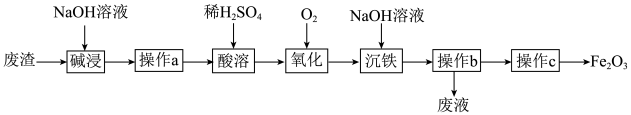
(1)“碱浸”时可能发生的反应有____ 个。“酸溶”时发生反应的化学方程式为______ 。
(2)“操作a”的名称为____ ,用到的玻璃仪器有玻璃棒、______ 。
(3)写出“氧化”时的离子方程式_______ 。检验氧化是否完全可加入的试剂是_______ 。
(4)操作c包括洗涤等一系列操作,洗涤时证明沉淀洗涤干净的操作_______ 。
(5)“沉铁”步骤可观察到现象是_______ 。

(1)“碱浸”时可能发生的反应有
(2)“操作a”的名称为
(3)写出“氧化”时的离子方程式
(4)操作c包括洗涤等一系列操作,洗涤时证明沉淀洗涤干净的操作
(5)“沉铁”步骤可观察到现象是
您最近一年使用:0次
解题方法
6 . 我国的铝资源丰富,铝产量居全球第一,工业上以铝土矿(主要成分是 ,含杂质
,含杂质 和
和 )为原料生产铝。其生产流程如图:
)为原料生产铝。其生产流程如图:
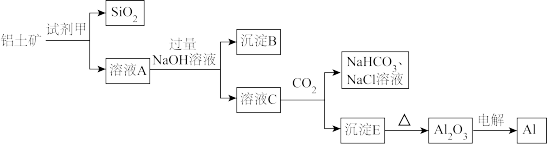
回答下列问题:
(1)试剂甲的化学式是_______ 。
(2)在溶液A中加入过量NaOH溶液的目的是_______ 。
(3)溶液C中通入二氧化碳生成沉淀E的离子方程式为_______ 。
(4)以石墨为电极,通过电解熔融 可制得金属铝。长时间电解后,需要更换新的石墨电极的
可制得金属铝。长时间电解后,需要更换新的石墨电极的_______ 极(填“阴”或“阳”)。
(5) 是制备晶体硅的原料。工业上在高温下用炭粉还原
是制备晶体硅的原料。工业上在高温下用炭粉还原 制备晶体硅的化学方程式为
制备晶体硅的化学方程式为_______ ;若有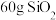 参加反应,生成气体的体积为
参加反应,生成气体的体积为_______ L(标准状况下)。
 ,含杂质
,含杂质 和
和 )为原料生产铝。其生产流程如图:
)为原料生产铝。其生产流程如图:
回答下列问题:
(1)试剂甲的化学式是
(2)在溶液A中加入过量NaOH溶液的目的是
(3)溶液C中通入二氧化碳生成沉淀E的离子方程式为
(4)以石墨为电极,通过电解熔融
 可制得金属铝。长时间电解后,需要更换新的石墨电极的
可制得金属铝。长时间电解后,需要更换新的石墨电极的(5)
 是制备晶体硅的原料。工业上在高温下用炭粉还原
是制备晶体硅的原料。工业上在高温下用炭粉还原 制备晶体硅的化学方程式为
制备晶体硅的化学方程式为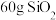 参加反应,生成气体的体积为
参加反应,生成气体的体积为
您最近一年使用:0次
名校
解题方法
7 . 工业上常以高硫铝土矿(主要成分为 、
、 ,还含有少量
,还含有少量 等)为原料,生产
等)为原料,生产 和铝单质的工艺流程如图:
和铝单质的工艺流程如图:

已知:高硫铝土矿粉中含有的 在“焙烧Ⅰ”过程中,发生的反应为
在“焙烧Ⅰ”过程中,发生的反应为 ;“焙烧Ⅱ”在隔绝空气的条件下进行。
;“焙烧Ⅱ”在隔绝空气的条件下进行。
(1) 中硫的化合价为
中硫的化合价为_______ 价;“焙烧Ⅰ”时,加入少量 的主要作用为
的主要作用为_______ 。
(2)矿粉经过“焙烧Ⅰ”后,所得的大块烧渣需要进行“碱浸”,为了加快浸取的速率,可采取的措施为_______ 、_______ 。(任写两点)
(3)当反应 中生成标准状况下4.48L
中生成标准状况下4.48L 时,转移了
时,转移了_______ mol电子。
(4)“焙烧Ⅱ”过程中产生的污染性气体是_______ (填化学式),大量排放该气体造成的主要环境问题是_______ 。
(5)“焙烧Ⅲ”发生反应的化学方程式为_______ 。
(6)工业上,以物质X为原料冶炼金属Al的方法为_______ ,发生反应的化学方程式为_______ 。
 、
、 ,还含有少量
,还含有少量 等)为原料,生产
等)为原料,生产 和铝单质的工艺流程如图:
和铝单质的工艺流程如图:
已知:高硫铝土矿粉中含有的
 在“焙烧Ⅰ”过程中,发生的反应为
在“焙烧Ⅰ”过程中,发生的反应为 ;“焙烧Ⅱ”在隔绝空气的条件下进行。
;“焙烧Ⅱ”在隔绝空气的条件下进行。(1)
 中硫的化合价为
中硫的化合价为 的主要作用为
的主要作用为(2)矿粉经过“焙烧Ⅰ”后,所得的大块烧渣需要进行“碱浸”,为了加快浸取的速率,可采取的措施为
(3)当反应
 中生成标准状况下4.48L
中生成标准状况下4.48L 时,转移了
时,转移了(4)“焙烧Ⅱ”过程中产生的污染性气体是
(5)“焙烧Ⅲ”发生反应的化学方程式为
(6)工业上,以物质X为原料冶炼金属Al的方法为
您最近一年使用:0次
2022-07-10更新
|
281次组卷
|
3卷引用:陕西省商洛市2021-2022学年高一下学期期末教学质量检测化学试题
名校
8 . 铝土矿的主要成分是Al2O3,含有Fe2O3、SiO2等杂质,按下列操作从铝土矿中提取Al2O3。

回答下列问题:
(1)写出沉淀物的化学式:a_______ ;d_______ ;
(2)写出加入过量NaOH溶液时所发生主要反应的离子方程式:_______ 、_______ 。
(3)写出通入气体B(过量)时溶液c中发生反应的离子方程式:_______ 、_______ 。
(4)气体B能否改用试剂A代替?_______ (填“能”或“不能”);原因是_______ 。
(5)用石墨做电极电解提取的熔融的Al2O3,从阳极表面可以得到两种气体分别是_______ 、_______ (用化学式表示)
(6)KAl(SO4)2·12H2O(明矾)是一种复盐,明矾溶液与Ba(OH)2溶液反应, 恰好完全沉淀其离子方程式为
恰好完全沉淀其离子方程式为_______ ,反应后溶液的pH_______ (填“>”“=”或“<”)7。

回答下列问题:
(1)写出沉淀物的化学式:a
(2)写出加入过量NaOH溶液时所发生主要反应的离子方程式:
(3)写出通入气体B(过量)时溶液c中发生反应的离子方程式:
(4)气体B能否改用试剂A代替?
(5)用石墨做电极电解提取的熔融的Al2O3,从阳极表面可以得到两种气体分别是
(6)KAl(SO4)2·12H2O(明矾)是一种复盐,明矾溶液与Ba(OH)2溶液反应,
 恰好完全沉淀其离子方程式为
恰好完全沉淀其离子方程式为
您最近一年使用:0次
解题方法
9 . 明矾晶体[ ]在生产、生活中有广泛用途,如饮用水的净化、造纸工业的施胶剂、食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、
]在生产、生活中有广泛用途,如饮用水的净化、造纸工业的施胶剂、食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、 及少量
及少量 和
和 )可制备明矾,工艺流程如图:
)可制备明矾,工艺流程如图:

回答下列问题:
(1)“滤渣①”的主要成分是___________ (填化学式);操作Ⅱ用到的玻璃仪器有玻璃棒、___________ 。
(2)滤液A中含有的阳离子有:___________ ,加入 的作用是:
的作用是:___________ 。
(3)写出流程图丁中 在水溶液中的电离方程式:
在水溶液中的电离方程式:___________ 。
(4)若将流程图甲中的过量稀硫酸改成过量的氢氧化钾溶液,所得溶液的溶质除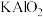 外,还含有
外,还含有___________ (填化学式);写出铝灰与过量的氢氧化钾溶液反应生成气体的化学方程式:___________ 。
(5)向流程图丁的 溶液中逐滴滴入NaOH溶液至过量,下列表示NaOH加入量与溶液中沉淀的量的关系示意图中,正确的是___________。(填字母)
溶液中逐滴滴入NaOH溶液至过量,下列表示NaOH加入量与溶液中沉淀的量的关系示意图中,正确的是___________。(填字母)
 ]在生产、生活中有广泛用途,如饮用水的净化、造纸工业的施胶剂、食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、
]在生产、生活中有广泛用途,如饮用水的净化、造纸工业的施胶剂、食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、 及少量
及少量 和
和 )可制备明矾,工艺流程如图:
)可制备明矾,工艺流程如图:
回答下列问题:
(1)“滤渣①”的主要成分是
(2)滤液A中含有的阳离子有:
 的作用是:
的作用是:(3)写出流程图丁中
 在水溶液中的电离方程式:
在水溶液中的电离方程式:(4)若将流程图甲中的过量稀硫酸改成过量的氢氧化钾溶液,所得溶液的溶质除
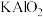 外,还含有
外,还含有(5)向流程图丁的
 溶液中逐滴滴入NaOH溶液至过量,下列表示NaOH加入量与溶液中沉淀的量的关系示意图中,正确的是___________。(填字母)
溶液中逐滴滴入NaOH溶液至过量,下列表示NaOH加入量与溶液中沉淀的量的关系示意图中,正确的是___________。(填字母)A. | B. |
C. | D. |
您最近一年使用:0次
名校
解题方法
10 . 铝是一种重要的金属,在生产、生活中具有许多重要的用途,下图是用铝土矿(主要成分是 ,此外还含有少量
,此外还含有少量 、
、 等杂质)制备铝的工艺流程:
等杂质)制备铝的工艺流程:
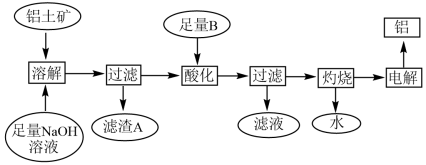
已知:溶液中的硅酸钠能与偏铝酸钠反应,生成硅铝酸盐沉淀,反应的化学方程式为 。
。
(1)铝土矿中的 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为___________ 。
(2)在工艺流程中“酸化”时,加入的最佳物质B是___________ ,理由是___________ 。
(3)工业上用 与C、
与C、 在高温条件下反应制取
在高温条件下反应制取 ,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为
,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为___________ 。
(4)某同学为验证铝与氧化铁发生铝热反应得到的熔融物中还含有 ,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有
,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有 。则物质甲是
。则物质甲是___________ (填化学式),该同学设计的实验方案___________ (填“合理”或“不合理”),原因是___________ (若合理,则不用填写)。
 ,此外还含有少量
,此外还含有少量 、
、 等杂质)制备铝的工艺流程:
等杂质)制备铝的工艺流程:
已知:溶液中的硅酸钠能与偏铝酸钠反应,生成硅铝酸盐沉淀,反应的化学方程式为
 。
。(1)铝土矿中的
 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为(2)在工艺流程中“酸化”时,加入的最佳物质B是
(3)工业上用
 与C、
与C、 在高温条件下反应制取
在高温条件下反应制取 ,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为
,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为(4)某同学为验证铝与氧化铁发生铝热反应得到的熔融物中还含有
 ,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有
,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有 。则物质甲是
。则物质甲是
您最近一年使用:0次
2021-12-17更新
|
268次组卷
|
2卷引用:陕西省榆林市第一中学2021-2022学年高一下学期期中考试化学试题



