名校
解题方法
1 . 磁性氧化铁因其特殊的超顺磁性,在巨磁电阻、磁性液体和磁记录、软磁、永磁、磁致冷、巨磁阻抗材料以及磁光器件、磁探测器等方面具有广阔的应用前景。以高硫铝土矿(主要含Al2O3、Fe2O3、SiO2和少量的FeS2等)为原料提取氧化铝和磁性氧化铁的流程如图:
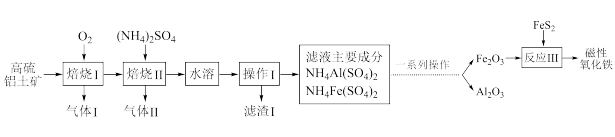
(1)磁性氧化铁的化学式为____ ;写出滤渣I中主要成分的一种用途:____ 。
(2)操作I在实验中要用到的玻璃仪器有____ 。
(3)焙烧I中,FeS2发生反应的化学方程式为____ 。
(4)焙烧I的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是____ (任答一点)。

(5)焙烧II中氧化铝参与反应的化学方程式为_____ 。
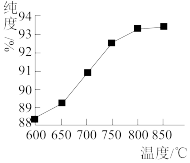
(6)反应III中加入FeS2的目的是作_____ (填“氧化剂”或“还原剂”)。反应Ⅲ的煅烧温度对磁性氧化铁的纯度有很大影响。已知温度对磁性氧化铁纯度的影响如图所示,则煅烧时,温度最好控制在____ ℃。
(7)滤液经过一系列操作可获得Al2O3,请简述这一系列操作的具体过程:_____ 。

(1)磁性氧化铁的化学式为
(2)操作I在实验中要用到的玻璃仪器有
(3)焙烧I中,FeS2发生反应的化学方程式为
(4)焙烧I的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是

(5)焙烧II中氧化铝参与反应的化学方程式为
(6)反应III中加入FeS2的目的是作

(7)滤液经过一系列操作可获得Al2O3,请简述这一系列操作的具体过程:
您最近一年使用:0次
2022-10-01更新
|
271次组卷
|
5卷引用:内蒙古自治区部分学校2023届高三上学期9月联考化学试题
2 . 某混合物可能含有Al、Cu、 、
、 ,为探究该混合物成分,某兴趣小组设计如图分析方案。下列分析不正确的是
,为探究该混合物成分,某兴趣小组设计如图分析方案。下列分析不正确的是

 、
、 ,为探究该混合物成分,某兴趣小组设计如图分析方案。下列分析不正确的是
,为探究该混合物成分,某兴趣小组设计如图分析方案。下列分析不正确的是
A.已知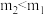 ,则混合物中一定含有 ,则混合物中一定含有 和Al 和Al |
B.蓝绿色溶液中含有的阳离子没有 |
| C.固体P一定是纯净物 |
| D.向溶液N中滴加足量盐酸没有白色沉淀生成 |
您最近一年使用:0次
名校
解题方法
3 . 某铜矿石的主要成分是Cu2O,还含有少量的Al2O3、Fe2O3和SiO2.某工厂利用此矿石炼制粗铜的工艺流程如图所示(已知:Cu2O+2H+=Cu+Cu2++H2O).

请结合流程图回答下列问题:
(1)滤液A中铁元素的存在形式为_______ (填离子符号),生成该离子的离子方程式为_______ .
(2)已知滤液C的主要成分为NaAlO2溶液,请写出由滤液A生成滤液C的离子方程式_______ .
(3)固体E中有两种物质,一种是黑色固体,另一种为_______ (填化学式),生成黑色固体的化学方程式为_______ .
(4)金属单质Al与固体混合物E在高温条件下生成Cu的化学反应方程式为_______ .
(5)已知废液的主要成分是Na2SiO3溶液.固体混合物B中加入NaOH溶液发生反应的离子方程式为_______ ;反应后,实现铜与废液分离的实验操作为_______ (填操作名称).

请结合流程图回答下列问题:
(1)滤液A中铁元素的存在形式为
(2)已知滤液C的主要成分为NaAlO2溶液,请写出由滤液A生成滤液C的离子方程式
(3)固体E中有两种物质,一种是黑色固体,另一种为
(4)金属单质Al与固体混合物E在高温条件下生成Cu的化学反应方程式为
(5)已知废液的主要成分是Na2SiO3溶液.固体混合物B中加入NaOH溶液发生反应的离子方程式为
您最近一年使用:0次
4 . 下列除杂质的操作中不正确的是
A. 溶液中混有 溶液中混有 加入过量 加入过量 粉,过滤 粉,过滤 |
B. 中混有 中混有 :加入过量 :加入过量 溶液充分反应,过滤 溶液充分反应,过滤 |
C. 中混有 中混有 :通入 :通入 溶液洗气,干燥 溶液洗气,干燥 |
D. 溶液中混有少量 溶液中混有少量 :往溶液中通入过量 :往溶液中通入过量 |
您最近一年使用:0次
名校
解题方法
5 . 铝是一种重要金属,从铝土矿(主要成分为Al2O3,Fe2O3、SiO2等)中冶炼Al的工业生产流程如下图:
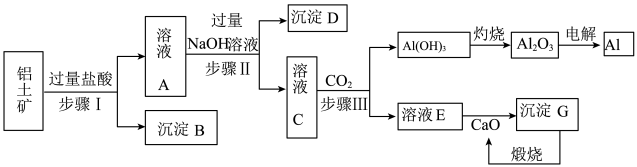
(1)溶液A中含的阳离子主要有________ .
(2)写出步骤II生成溶液C 的离子方程式________ ,步骤I、II、III都要用到的分离方法是________ .
(3)生产过程中,除CaO可以循环使用外,还可以循环使用的物质有________ (填化学式).
(4)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:________ .
(5)经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中Al2O3的纯度(质量分数)________ (用含a、b的最简式表示).

(1)溶液A中含的阳离子主要有
(2)写出步骤II生成溶液C 的离子方程式
(3)生产过程中,除CaO可以循环使用外,还可以循环使用的物质有
(4)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:
(5)经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中Al2O3的纯度(质量分数)
您最近一年使用:0次
2020-08-28更新
|
304次组卷
|
4卷引用:内蒙古鄂尔多斯市第一中学2022-2023 学年高一上学期期末考试化学试题
2014·江苏南通·二模
6 . 某铝土矿中主要含有Al2O3、Al(OH)3、AlO(OH),还含有Fe2O3等杂质。利用拜耳法生产氧化铝的流程如图所示:
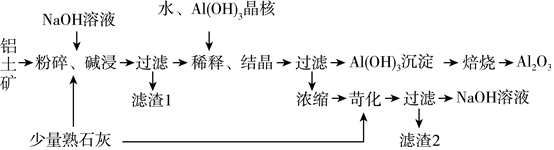
请回答下列问题:
(1)粉碎后的铝土矿碱浸时应在高温下进行,其目的是_______ 。
(2)AlO(OH)与NaOH溶液反应的化学方程式为___________ 。
(3)在稀释、结晶过程中,稀释的目的是_____________ ;加Al(OH)3晶核的目的是促进Al(OH)3的析出。上述“稀释、结晶”工艺,也可用通入足量的________ 气体的方法来代替。
(4)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化反应除去,写出苛化反应的化学方程式:__________ 。
(5)该生产流程能实现________ (填化学式)的循环利用。

请回答下列问题:
(1)粉碎后的铝土矿碱浸时应在高温下进行,其目的是
(2)AlO(OH)与NaOH溶液反应的化学方程式为
(3)在稀释、结晶过程中,稀释的目的是
(4)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化反应除去,写出苛化反应的化学方程式:
(5)该生产流程能实现
您最近一年使用:0次



