名校
解题方法
1 . 以高硫铝土矿(主要成分为Fe2O3、Al2O3、SiO2,少量FeS2和硫酸盐)为原料制备聚合硫酸铁[Fe2(OH)x(SO4)y]n和明矾的部分工艺流程如下:
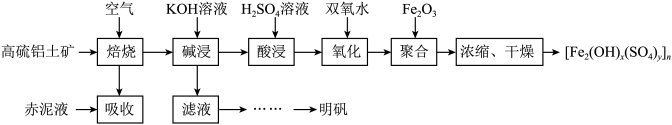
已知:赤泥液的主要成分为Na2CO3.下列说法错误的是

已知:赤泥液的主要成分为Na2CO3.下列说法错误的是
| A.赤泥液的作用是吸收“焙烧”阶段中产生的SO2 |
| B.从“滤液”到“明矾”的过程中还应有“除硅”步骤 |
| C.聚合硫酸铁可用于净化自来水,与其组成中的Fe3+具有氧化性有关 |
| D.在“聚合”阶段,若增加Fe2O3用量,会使[Fe2(OH)x(SO4)y]n中x变大 |
您最近一年使用:0次
2023-08-28更新
|
315次组卷
|
7卷引用:江苏省苏北三市2022-2023学年高二上学期阶段调研测试化学试题
名校
2 . 工业上从铝土矿[主要成分为Al2O3,杂质为Fe2O3、SiO2(不溶于盐酸)等]中提取Al2O3作冶炼铝的原料。提取的操作流程可表示为:
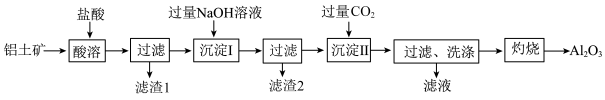
(1)滤渣Ⅰ为___________ (填化学式)。
(2)写出“酸溶”过程Al2O3与盐酸反应的离子方程式:___________
(3)沉淀Ⅰ是红褐色,写出生成“沉淀Ⅰ”的离子方程式为___________ 。
(4)沉淀Ⅱ为氢氧化铝,过滤洗涤后,检验洗涤已经干净的方法是___________ 。
(5)沉淀Ⅱ为氢氧化铝,写出“灼烧”反应的化学方程式为___________ 。

(1)滤渣Ⅰ为
(2)写出“酸溶”过程Al2O3与盐酸反应的离子方程式:
(3)沉淀Ⅰ是红褐色,写出生成“沉淀Ⅰ”的离子方程式为
(4)沉淀Ⅱ为氢氧化铝,过滤洗涤后,检验洗涤已经干净的方法是
(5)沉淀Ⅱ为氢氧化铝,写出“灼烧”反应的化学方程式为
您最近一年使用:0次
3 . 氧化镁是优质的耐高温材料。某兴趣小组利用菱镁矿(主要成分为MgCO3,还含有少量SiO2、Al2O3等杂质)设计制备氧化镁的流程如图:

(1)步骤(Ⅰ)中分离操作的名称是_______ 。
(2)步骤(I)分离出的滤渣中主要含有_______ ,它属于_______ (填“酸性”或“碱性”)氧化物。
(3)写出步骤(II)生成Mg(OH)2的离子方程式:_______ 。

(1)步骤(Ⅰ)中分离操作的名称是
(2)步骤(I)分离出的滤渣中主要含有
(3)写出步骤(II)生成Mg(OH)2的离子方程式:
您最近一年使用:0次
22-23高一上·江苏南通·期中
名校
解题方法
4 . 一种利用含铁废料(主要含Fe2O3、Al2O3)制备磁性Fe3O4纳米粒子的工艺流程如下。

下列有关说法正确的是

下列有关说法正确的是
| A.“碱洗”的目的是溶解废料中的Al2O3 |
| B.“还原”过程中,铁粉应过量 |
| C.加热沉铁时分别发生复分解反应和分解反应 |
| D.溶液X中的溶质为FeSO4溶液 |
您最近一年使用:0次
解题方法
5 . 由制铝工业废渣(主要含Fe、Ca、Si、Al等的氧化物)制取聚合硫酸铁铝净水剂的流程如下:(硅的氧化物与硫酸不反应)

下列有关说法不正确 的是

下列有关说法
| A.控制适当反应温度并不断搅拌,有利于提高铁、铝浸取率 |
B.浸取后的溶液中含有的阳离子为 和 和 |
C.滤渣的成分为 和 和 |
| D.聚合硫酸铁铝溶于水产生胶体吸附杂质 |
您最近一年使用:0次
2022-09-13更新
|
285次组卷
|
3卷引用:江苏省海安市2021-2022学年高一上学期学业质量检测化学试题
江苏省海安市2021-2022学年高一上学期学业质量检测化学试题(已下线)题型03 重要元素及其化合物的相关实验及工艺流程-学易金卷:备战2023-2024学年高一化学期末真题分类汇编(江苏专用)安徽省滁州市部分学校2022-2023学年高二下学期5月联考化学试题
解题方法
6 . 以铝土矿(主要成分为 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如下:
等杂质)为原料制备铝的一种工艺流程如下:不正确 的是
 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如下:
等杂质)为原料制备铝的一种工艺流程如下:
| A.将铝土矿粉碎有利于加快碱溶速率 |
B.滤渣的主要成分为 和 和 |
C.过滤Ⅱ所得滤液中主要存在的离子为 、 、 |
D. 与冰晶石共熔电解得到单质铝 与冰晶石共熔电解得到单质铝 |
您最近一年使用:0次
2022-08-29更新
|
510次组卷
|
3卷引用:江苏省苏州市2021-2022学年高一下学期期末学业质量阳光指标调研(延期到8月)化学试题
江苏省苏州市2021-2022学年高一下学期期末学业质量阳光指标调研(延期到8月)化学试题17 2024年苏州昆山周市高级中学高一3月月考(已下线)专题04 金属与人类文明-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
名校
解题方法
7 . 以含钴废渣(主要成分为CoO和Co2O3,含少量Al2O3和ZnO)为原料制备锂电池的电极材料CoCO3的工艺流程如下:

下列说法错误的是

下列说法错误的是
A.通入SO2发生反应的离子方程式:2Co3++SO2+2H2O=2Co2++SO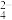 +4H+ +4H+ |
| B.加入适量Na2CO3调节pH,是利用几种氢氧化物Ksp的不同来除锌 |
| C.若萃取剂的总量一定,则分多次加入萃取比一次加入萃取效果更好 |
| D.将含Co2+的溶液缓慢滴加到Na2CO3溶液中沉钴,以提高CoCO3的产率 |
您最近一年使用:0次
2022-08-23更新
|
594次组卷
|
7卷引用:江苏省徐州市铜山区2021-2022学年高二下学期期中学情调研化学试题
江苏省徐州市铜山区2021-2022学年高二下学期期中学情调研化学试题江苏省常州市2021届高三下学期期初调研考试化学试题湖南省耒阳市第一中学2022届高三下学期5月月考化学试题江苏省扬州中学2023届高三下学期模拟预测化学试题(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(浙江专用)河南省周口恒大中学2023-2024学年高二上学期10月月考化学试题
解题方法
8 . 铝土矿的主要成分是 ,还有部分
,还有部分 、
、 ,以及少量不溶于酸碱溶液的其它杂质,工业上从铝土矿中提取铝可采取如下工艺流程:
,以及少量不溶于酸碱溶液的其它杂质,工业上从铝土矿中提取铝可采取如下工艺流程:

已知: 是难溶于水的酸性氧化物,下列说法中正确的是
是难溶于水的酸性氧化物,下列说法中正确的是
 ,还有部分
,还有部分 、
、 ,以及少量不溶于酸碱溶液的其它杂质,工业上从铝土矿中提取铝可采取如下工艺流程:
,以及少量不溶于酸碱溶液的其它杂质,工业上从铝土矿中提取铝可采取如下工艺流程:
已知:
 是难溶于水的酸性氧化物,下列说法中正确的是
是难溶于水的酸性氧化物,下列说法中正确的是| A.①~⑤中,属于氧化还原反应的是①⑤ |
B.沉淀Ⅰ是 和少量不溶于酸碱溶液的其它杂质 和少量不溶于酸碱溶液的其它杂质 |
C.溶液Ⅱ中含有的阴离子只有 |
D.生成沉淀Ⅲ的离子方程式为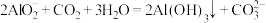 |
您最近一年使用:0次
2022·江苏·模拟预测
9 . 以铝土矿粉(主要含Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐);为原料生产Al2O3和Fe3O4的部分流程如下,已知有一种立方型晶体FeS2的结构如下图所示:

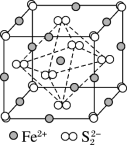
下列说法正确的是


下列说法正确的是
| A.“焙烧I”时,加入少量CaO可提高矿粉中硫的去除率 |
B.用NaOH溶液吸收过量SO2的离子方程式为:2OH- +SO2=SO +H2O +H2O |
| C.滤液中通入足量CO2,过滤后可得到Al2O3 |
D.与Fe2+距离最近且相等距离的S 的数目为6 的数目为6 |
您最近一年使用:0次
名校
解题方法
10 . 铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:

注: SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为___________ 。
(2)向“过滤I”所得滤液中加入NaHCO3溶液,写出该反应的离子方程式___________ 。
(3)“电解I”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是_____ 。
(4)铝粉在1 000° C时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是______ 。

注: SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为
(2)向“过滤I”所得滤液中加入NaHCO3溶液,写出该反应的离子方程式
(3)“电解I”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是
(4)铝粉在1 000° C时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是
您最近一年使用:0次



