18. KI可用于分析试剂、感光材料、制药等,其制备原理如下:
反应I:3I
2+6KOH=KIO
3+5KI+3H
2O
反应Ⅱ:3H
2S+KIO
3=3S↓+KI+3H
2O

请回答有关问题。
(1)装置中盛装30%氢氧化钾溶液的仪器名称是
___________。
(2)关闭启普发生器活塞,先滴入30%的KOH溶液。待观察到三颈烧瓶中溶液颜色由棕黄色变为
___________(填现象),停止滴人KOH溶液;然后打开启普发生器活塞,待三颈烧瓶和烧杯中产生气泡的速率接近相等时停止通气。
(3)滴入硫酸溶液,并对三颈烧瓶中的溶液进行水浴加热,其目的是
___________。
(4)把三颈烧瓶中的溶液倒入烧杯中,加入碳酸钡,在过滤器中过滤,过滤得到的沉淀中除含有过量碳酸钡外,还含有单质硫和
___________(填名称)。合并滤液和洗涤液,蒸发至析出结晶,干燥得成品。
(5)碘被称为“智力元素”,科学合理地补充碘可防治碘缺乏病,KIO
3用于加碘盐中。实验室模拟工业制备KIO
3流程如下:
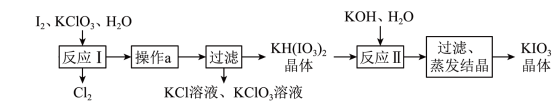
几种物质的溶解度见下表:
| KCl | KH(IO3)2 | KClO3 |
| 25℃时的溶解度 | 20.8 | 0.8 | 7.5 |
| 80℃时的溶解度 | 37.1 | 12.4 | 16.2 |
①由上表数据分析可知,“操作a”为
___________。
②反应Ⅰ中,两种还原产物得电子数相等,请写出发生的化学反应方程式
___________。
(6)某同学测定上述流程生产的KIO
3样品的纯度。
取1.00g样品溶于蒸馏水中并用硫酸酸化,再加入过量的KI和少量的淀粉溶液,逐滴滴加2.0mol·L
-1Na
2S
2O
3溶液,恰好完全反应时共消耗12.60mLNa
2S
2O
3溶液。该样品中KIO
3的质量分数为
___________(已知反应:I
2+2Na
2S
2O
3=2NaI+Na
2S
4O
6)。