名校
1 . 高铝粉煤灰是火力发电厂燃煤锅炉排放出的固体废物,含有较多的Al2O3,少MgO、CaO、铁的氧化物及其他不溶性杂质。从粉煤灰中提取Al2O3的工艺流程如图:
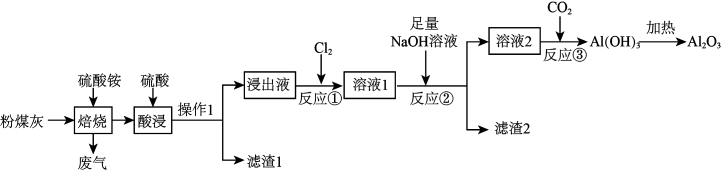
(1)操作1的名称是____ ;滤渣1中除了原不溶性杂质外,还有____ 。
(2)检验浸出液中含有Fe2+的操作与现象是____ 。
(3)反应①的离子方程式为____ ,反应①中还可以用____ (填试剂化学式)替代Cl2。
(4)滤渣2的主要成分有____ 。
(5)溶液2中含铝元素的化合物与过量CO2反应的产物还有NaHCO3,该反应的化学方程式为____ 。
(6)实验室配制100mL2.00mol•L-1H2SO4溶液。
①需要18.00mol/L浓H2SO4的体积为____ mL。
②下述仪器中必须用到的有____ (填标号),还缺少的玻璃仪器为____ (填名称)。


(1)操作1的名称是
(2)检验浸出液中含有Fe2+的操作与现象是
(3)反应①的离子方程式为
(4)滤渣2的主要成分有
(5)溶液2中含铝元素的化合物与过量CO2反应的产物还有NaHCO3,该反应的化学方程式为
(6)实验室配制100mL2.00mol•L-1H2SO4溶液。
①需要18.00mol/L浓H2SO4的体积为
②下述仪器中必须用到的有

您最近一年使用:0次
2022-11-03更新
|
363次组卷
|
2卷引用:四川省泸县第四中学2022-2023学年高一上学期期末考试化学试题
解题方法
2 . 铝氢化钠(NaAlH4)是有机合成中的一种重要还原剂。 以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝氢化钠的一种工艺流程如图:

下列说法中不正确的是

下列说法中不正确的是
| A.为了提高“碱溶”效率,在“碱溶”前对铝土矿进行粉碎 |
| B.“反应III”为氧化还原反应 |
| C.“滤渣”的主要成分在高温下可与铝单质发生化学反应 |
| D.“滤渣”的主要成分为氧化铁 |
您最近一年使用:0次
名校
解题方法
3 . 高铝粉煤灰是火力发电厂燃煤锅炉排放出的固体废物,含有较多的Al2O3,少量MgO、CaO、 铁的氧化物及其他不溶性杂质。从粉煤灰中提取Al2O3的工艺流程如图。
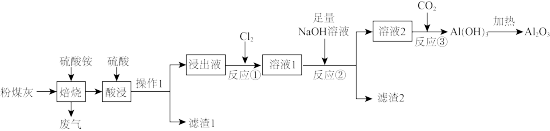
(1)操作1的名称是_______ , 滤渣1中除了原不溶性杂质外,还有_______ 。
(2)检验浸出液中含有Fe2+的操作与现象是_______ 。
(3)反应①的离子方程式为_______ ,反应①中还可以用_______ (填试剂化学式)替代Cl2。
(4)滤渣2的主要成分有_______ 。
(5)溶液2中含铝元素的化合物与过量CO2反应的化学方程式为_______ 。
(6)实验室配制100mL 2.00mol/L H2SO4溶液。
①需要18.00mol/L浓H2SO4的体积为_______ mL。(计算结果保留1位小数)
②下列仪器中,需要的有_______ (填标号),还缺少的玻璃仪器为_______ 。(填仪器名称)
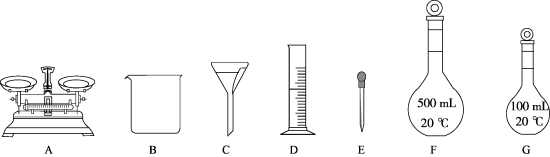

(1)操作1的名称是
(2)检验浸出液中含有Fe2+的操作与现象是
(3)反应①的离子方程式为
(4)滤渣2的主要成分有
(5)溶液2中含铝元素的化合物与过量CO2反应的化学方程式为
(6)实验室配制100mL 2.00mol/L H2SO4溶液。
①需要18.00mol/L浓H2SO4的体积为
②下列仪器中,需要的有

您最近一年使用:0次
解题方法
4 . 根据流程回答问题:
Ⅰ.从海带(含KI)中提取碘, 某研究性学习小组设计了以下流程:

(1)步骤①中灼烧海带是在_______ ( 填仪器名称)中进行。
(2)步骤③、⑤的实验操作分别为_______ 、_______ 。
(3)反应④的离子方程式为_______ 。
Ⅱ.工业上用铝土矿(主要成分为Al2O3,Al2O3的含量为a%,其中含有Fe2O3 杂质)为原料冶炼铝的工艺流程如下(所加试剂均过量):

(4)试剂b是_______ (填化学式)。
(5)反应①的离子方程式为_______ 。
(6)过程④的化学方程式为_______ 。
(7)工业上生产1 t Al,在生产过程中Al的损失率 为b%,理论上需投入铝土矿_______ (列出计算表达式即可)。
Ⅰ.从海带(含KI)中提取碘, 某研究性学习小组设计了以下流程:

(1)步骤①中灼烧海带是在
(2)步骤③、⑤的实验操作分别为
(3)反应④的离子方程式为
Ⅱ.工业上用铝土矿(主要成分为Al2O3,Al2O3的含量为a%,其中含有Fe2O3 杂质)为原料冶炼铝的工艺流程如下(所加试剂均过量):

(4)试剂b是
(5)反应①的离子方程式为
(6)过程④的化学方程式为
(7)工业上生产1 t Al,在生产过程中Al的
您最近一年使用:0次
名校
解题方法
5 . 某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(
,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体( )和胆矾晶体(
)和胆矾晶体( )。
)。

请回答:
(1)步骤Ⅰ中,发生的氧化还原反应的离子方程式为_______ ,涉及到的分离操作是_______ 。
(2)试剂X是_______ ;溶液D是_______ 。
(3)溶液E在空气中易被氧化,请设计一个简单的实验方案检验溶液E是否被氧化_______ 。
(4)在步骤Ⅱ时,若用大理石与浓盐酸制取 并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体减少,可采取的改进措施是
并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体减少,可采取的改进措施是_______ 。
(5)从 溶液中获得胆矾的操作是
溶液中获得胆矾的操作是_______ 。
(6)工业上常用溶液E制取净水剂 ,流程如图:
,流程如图:

写出由 制取
制取 的离子方程式
的离子方程式_______ 。
 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(
,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体( )和胆矾晶体(
)和胆矾晶体( )。
)。
请回答:
(1)步骤Ⅰ中,发生的氧化还原反应的离子方程式为
(2)试剂X是
(3)溶液E在空气中易被氧化,请设计一个简单的实验方案检验溶液E是否被氧化
(4)在步骤Ⅱ时,若用大理石与浓盐酸制取
 并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体减少,可采取的改进措施是
并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体减少,可采取的改进措施是(5)从
 溶液中获得胆矾的操作是
溶液中获得胆矾的操作是(6)工业上常用溶液E制取净水剂
 ,流程如图:
,流程如图:
写出由
 制取
制取 的离子方程式
的离子方程式
您最近一年使用:0次
2022-07-17更新
|
607次组卷
|
2卷引用:四川省成都市树德中学2021-2022学年高一下学期期末考试化学试题
名校
解题方法
6 . 工业上以铝土矿(主要成分为 ,含少量氧化铁和二氧化硅)为原料生产铝的流程如图所示,下列叙述不正确的是
,含少量氧化铁和二氧化硅)为原料生产铝的流程如图所示,下列叙述不正确的是

 ,含少量氧化铁和二氧化硅)为原料生产铝的流程如图所示,下列叙述不正确的是
,含少量氧化铁和二氧化硅)为原料生产铝的流程如图所示,下列叙述不正确的是 
A.物质a可以是 或氨水 或氨水 |
B.滤渣①的主要成分是 |
| C.滤液1和滤液2中铝元素的化合价相同 |
D.步骤Ⅰ发生反应的化学方程式为: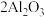 (熔融) (熔融) |
您最近一年使用:0次
2022-07-07更新
|
229次组卷
|
2卷引用:四川省乐山市2021-2022学年高一下学期期末教学质量检测化学试题
名校
解题方法
7 . 铝土矿是工业上制备金属铝的主要原料,其主要成分是Al2O3,同时还含有SiO2和Fe2O3。工业上可使用碱浸法提取铝土矿中的 Al2O3,其工业流程如图所示。根据图示信息,回答下列问题。

(1)为了提高铝土矿的浸取效率,可采用的方法是_______ 。(任写一条均可)
(2)第一次沉淀时发生了一系列离子反应,除了生成固体 B 的反应外,还有另外两个反应,请分别写出它们的离子方程式_______ ,_______ 。
(3)液体试剂 a 的化学式为_______ 。
(4)该工艺的副产品存在于滤液 X 中,除 Na2SO4外,其主要成分是_______ (填化学式)。试列举一项该副产品在工业生产或日常生活中的用途_______ 。
(5)操作①的名称为_______ 。若在实验室中进行该操作,样品应放置在_______ 中。
(6)取 10.0 g 铝土矿按照上述工艺进行处理,并在工艺中使用 5.0 mol/L的稀硫酸。第一次沉淀时所得沉淀的质量与加入硫酸的体积变化关系如图所示。则该铝土矿样品中 Al2O3的质量分数为_______ 。


(1)为了提高铝土矿的浸取效率,可采用的方法是
(2)第一次沉淀时发生了一系列离子反应,除了生成固体 B 的反应外,还有另外两个反应,请分别写出它们的离子方程式
(3)液体试剂 a 的化学式为
(4)该工艺的副产品存在于滤液 X 中,除 Na2SO4外,其主要成分是
(5)操作①的名称为
(6)取 10.0 g 铝土矿按照上述工艺进行处理,并在工艺中使用 5.0 mol/L的稀硫酸。第一次沉淀时所得沉淀的质量与加入硫酸的体积变化关系如图所示。则该铝土矿样品中 Al2O3的质量分数为

您最近一年使用:0次
名校
解题方法
8 . 工业上以铝土矿(主要成分是氧化铝,含氧化铁杂质)为原料冶炼铝的工艺流程如下:

下列叙述正确的是

下列叙述正确的是
| A.铝热反应就是指Al与Fe2O3高温条件下发生的反应 |
B.试剂Y是二氧化碳,它与AlO 反应生成氢氧化铝,滤液B中溶质主要是碳酸钠 反应生成氢氧化铝,滤液B中溶质主要是碳酸钠 |
| C.图中所示转化反应中包含1个氧化还原反应 |
| D.滤渣C可溶于稀硫酸,滴加硫氰化钾溶液,将产生血红色沉淀 |
您最近一年使用:0次
解题方法
9 . 铝是应用广泛的金属。以铝土矿(主要成分为 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如图所示:
等杂质)为原料制备铝的一种工艺流程如图所示:
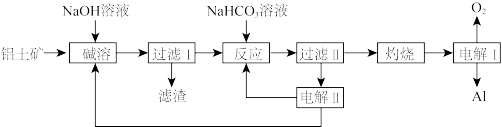
注: 在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。
(1)铝土矿“碱溶”时,氧化铝转化为_______ 进入溶液,提高铝土矿浸取速率的措施有_______ (任答两点)。
(2)向“过滤Ⅰ”所得滤液中加入 溶液,溶液的pH
溶液,溶液的pH_______ (填“增大”“减小”或“不变”),发生反应的离子方程式为_______ 。
(3)“电解Ⅰ”是电解熔融的 ,标准状况下每产生
,标准状况下每产生 转移的电子数为
转移的电子数为_______ 。
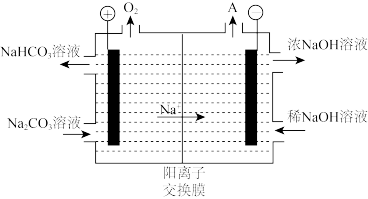
(4)“电解Ⅱ”是电解 溶液,其原理如图所示,阳极的电极反应式为
溶液,其原理如图所示,阳极的电极反应式为_______ 。
 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如图所示:
等杂质)为原料制备铝的一种工艺流程如图所示:
注:
 在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。(1)铝土矿“碱溶”时,氧化铝转化为
(2)向“过滤Ⅰ”所得滤液中加入
 溶液,溶液的pH
溶液,溶液的pH(3)“电解Ⅰ”是电解熔融的
 ,标准状况下每产生
,标准状况下每产生 转移的电子数为
转移的电子数为(4)“电解Ⅱ”是电解
 溶液,其原理如图所示,阳极的电极反应式为
溶液,其原理如图所示,阳极的电极反应式为
您最近一年使用:0次
名校
解题方法
10 . 铝硅合金材料性能优良。铝土矿(含30% 、40.8%
、40.8% 和少量
和少量 等)干法制取该合金的工艺如下:
等)干法制取该合金的工艺如下:

(1)若湿法处理铝土矿,用强酸浸取时,所得溶液中阳离子有_______ 。
(2)焙烧除铁反应: (
( 部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为
部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为_______ 。指出气体Ⅰ的用途_______ (任写一种)。

(3)操作①包括:加水溶解、_______ 。若所得溶液中加入过量NaOH溶液,含铝微粒发生反应的离子方程式为_______ 。
(4)用焦炭还原 、
、 会产生中间体SiC、
会产生中间体SiC、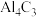 。任写一个高温下中间体又与
。任写一个高温下中间体又与 反应生成铝、硅单质的化学方程式
反应生成铝、硅单质的化学方程式_______ 。
(5)不计损失,投入1 t铝土矿,当加入27 kg纯铝后,铝硅合金中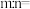
_______ (摩尔质量: ——60 g/mol
——60 g/mol  ——102 g/mol)
——102 g/mol)
 、40.8%
、40.8% 和少量
和少量 等)干法制取该合金的工艺如下:
等)干法制取该合金的工艺如下:
(1)若湿法处理铝土矿,用强酸浸取时,所得溶液中阳离子有
(2)焙烧除铁反应:
 (
( 部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为
部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为
(3)操作①包括:加水溶解、
(4)用焦炭还原
 、
、 会产生中间体SiC、
会产生中间体SiC、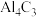 。任写一个高温下中间体又与
。任写一个高温下中间体又与 反应生成铝、硅单质的化学方程式
反应生成铝、硅单质的化学方程式(5)不计损失,投入1 t铝土矿,当加入27 kg纯铝后,铝硅合金中
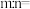
 ——60 g/mol
——60 g/mol  ——102 g/mol)
——102 g/mol)
您最近一年使用:0次
2022-04-12更新
|
248次组卷
|
2卷引用:四川省成都市树德中学2021-2022学年高一下学期4月阶段性测试化学试题



