1 . 已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,C、F是无色无味的气体,M为红褐色固体,D为具有磁性的黑色固体,请回答下列问题:
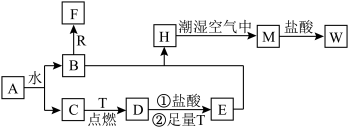
(1)A中含有的化学键类型有_______ 。A与 反应,生成气体为11.2L(标准状况下测定)时,转移到电子数为
反应,生成气体为11.2L(标准状况下测定)时,转移到电子数为_______ 。
(2)请写出R与B溶液反应的离子方程式_______ 。
(3)检验W溶液中金属阳离子的试剂为_______ (填化学式)
(4)反应①发生反应的离子方程式为_______ 。
(5)H生成M的现象为_______ ,反应的化学方程式为_______ 。

(1)A中含有的化学键类型有
 反应,生成气体为11.2L(标准状况下测定)时,转移到电子数为
反应,生成气体为11.2L(标准状况下测定)时,转移到电子数为(2)请写出R与B溶液反应的离子方程式
(3)检验W溶液中金属阳离子的试剂为
(4)反应①发生反应的离子方程式为
(5)H生成M的现象为
您最近一年使用:0次
名校
2 . 由实验操作和现象可得出相应正确结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向某溶液中先加入几滴KSCN溶液,再通入氯气 | 开始无明显现象,后溶液变红 | 溶液中一定含Fe2+,一定不含Fe3+ |
| B | 向两支均盛有5mL0.1mol·L−1的H2O2溶液的试管中分别加入2滴0.05 mol·L−1的Fe2(SO4)3;溶液和0.1mol·L−1CuCl2溶液 | 前者产生气泡较快 | 催化能力:Fe3+>Cu2+ |
| C | 铂丝蘸取某无色溶液后在火焰上灼烧 | 火焰呈黄色 | 该无色溶液中阳离子只含Na+ |
| D | 将含有二氧化硫的气体通入酸性高锰酸钾中,然后加入足量氯化钡溶液 | 产生白色沉淀 | 通过测定白色沉淀的质量,可推算二氧化硫的物质的量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 下列物质的存放方法合理的是
| A.氢氟酸存放在带有橡胶塞的棕色玻璃瓶中 | B.氢氧化钠溶液保存在磨口玻璃试剂瓶中 |
| C.氯化铁溶液存放在铜制容器中 | D.浓硫酸常温下用铁槽车储存运输 |
您最近一年使用:0次
2023·湖南长沙·一模
名校
解题方法
4 . 工业上制一元弱酸——硼酸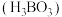 常采用硼镁矿(含
常采用硼镁矿(含 、
、 及少量
及少量 、
、 )经
)经 溶液溶浸后通过一系列反应制得。下列有关反应及离子方程式均正确的是
溶液溶浸后通过一系列反应制得。下列有关反应及离子方程式均正确的是
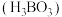 常采用硼镁矿(含
常采用硼镁矿(含 、
、 及少量
及少量 、
、 )经
)经 溶液溶浸后通过一系列反应制得。下列有关反应及离子方程式均正确的是
溶液溶浸后通过一系列反应制得。下列有关反应及离子方程式均正确的是A.硼酸的解离反应方程式: |
B.用 溶液检验溶浸后溶液是否含有 溶液检验溶浸后溶液是否含有 : : |
C. 溶于 溶于 溶液: 溶液: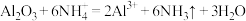 |
D. 溶于 溶于 溶液: 溶液: |
您最近一年使用:0次
2023-05-07更新
|
551次组卷
|
4卷引用:云南师范大学附属中学2023-2024学年高二上学期开学考试化学试题
(已下线)云南师范大学附属中学2023-2024学年高二上学期开学考试化学试题云南师范大学附属中学2023-2024学年高二上学期开学考试化学试题湖南省长沙市长郡中学2022-2023学年高三模拟试卷(一)化学试题江西省宜春市丰城市第九中学2023-2024学年高三上学期12月月考化学试题
解题方法
5 . 某实验小组以含铁污泥(主要成分为Fe2O3、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(FeSO4•7H2O)和柠檬酸铁铵。
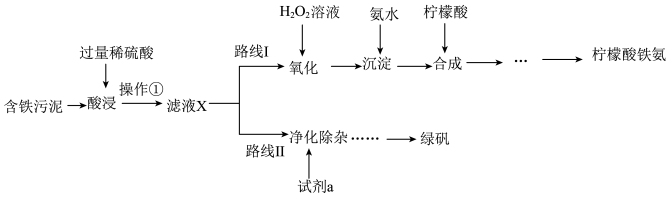
根据所学知识,回答下列问题:
(1)操作①的名称______ ,路线I中,加入H2O2溶液的目的是______ 。
(2)写出“酸浸”时,Fe2O3与硫酸反应的化学方程式:______ ;检验含有Fe3+的方法是______ 。
(3)“滤液X”中一定含有的阳离子为_______ 。
(4)实验室中配制FeSO4溶液时通常需加入少量的试剂a,目的是_____ ,请写出相应的离子方程式:______ 。

根据所学知识,回答下列问题:
(1)操作①的名称
(2)写出“酸浸”时,Fe2O3与硫酸反应的化学方程式:
(3)“滤液X”中一定含有的阳离子为
(4)实验室中配制FeSO4溶液时通常需加入少量的试剂a,目的是
您最近一年使用:0次
6 . 某化学兴趣小组对含某些离子(如表)的工业废水进行研究,废水中各离子的物质的量浓度相等,均为 。
。
(1)该溶液为无色溶液,则一定不存在的离子是_______ 。
(2)向废水中加入过量KOH溶液微热,有白色沉淀和无色气体产生,则沉淀是_______ (填化学式,下同),气体是_______ 。
(3)若向废水中加入过量盐酸,会生成遇空气变为红棕色的无色气体和 ,写出生成该无色气体和
,写出生成该无色气体和 的离子方程式:
的离子方程式:_______ 。一定条件下红棕色气体与(2)中产生的气体能反应生成无污染的气体,该反应的化学方程式为_______ 。
(4)向(3)中最后所得的溶液中加入过量的 溶液,充分反应后观察到有白色沉淀产生。
溶液,充分反应后观察到有白色沉淀产生。
①白色沉淀是_______ 。
②_______ (填“能”或“不能”)仅依据该现象判断废水中存在白色沉淀中的阴离子,理由是_______ 。
(5)结合(1)(2)(3),该废水中一定存在的离子是_______ 。
 。
。| 阳离子 |  、 、 、 、 、 、 |
| 阴离子 |  、 、 、 、 、 、 、 、 |
(2)向废水中加入过量KOH溶液微热,有白色沉淀和无色气体产生,则沉淀是
(3)若向废水中加入过量盐酸,会生成遇空气变为红棕色的无色气体和
 ,写出生成该无色气体和
,写出生成该无色气体和 的离子方程式:
的离子方程式:(4)向(3)中最后所得的溶液中加入过量的
 溶液,充分反应后观察到有白色沉淀产生。
溶液,充分反应后观察到有白色沉淀产生。①白色沉淀是
②
(5)结合(1)(2)(3),该废水中一定存在的离子是
您最近一年使用:0次
2023-04-27更新
|
91次组卷
|
2卷引用:云南省楚雄州2022-2023学年高一下学期期中学业质量监测化学试题
7 . 为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸,再进行以下,其结论正确的选项是
| A.假设再滴加KSCN溶液,溶液未变红,再滴加氯水,溶液变红,说明铁粉变质 |
| B.假设再滴加KSCN溶液,溶液未变红,说明铁粉未变质 |
| C.假设再依次滴加氯水、KSCN溶液,溶液变红,说明铁粉变质 |
| D.假设再滴加KSCN溶液,溶液变红,说明铁粉变质 |
您最近一年使用:0次
名校
8 . 下列除杂所选用的试剂或操作方法中正确的是
| 选项 | 物质 | 杂质 | 除杂试剂或操作方法 |
| A | FeCl2溶液 | FeCl3 | 加入过量铜粉,再过滤 |
| B | CO2气体 | HCl | 将气体通过盛有碱石灰的干燥管 |
| C | Cl2气体 | 水蒸气 | 将气体通过盛有浓硫酸的洗气瓶 |
| D | MgO固体 | Al2O3 | 加入过量的盐酸溶液,再过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-22更新
|
214次组卷
|
3卷引用:云南省昆明市西山区2022-2023学年高一上学期1月期末考试化学试题
9 . 为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
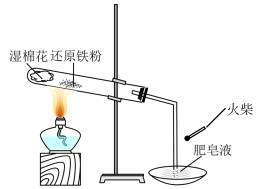
(1)高温下,让铁粉与水蒸气反应,见题图。试管中发生反应的化学方程式是___________ ,其中___________ 为氧化剂。
(2)根据图回答问题

①往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色A___________ 、B___________ 。
②写出上述过程中有关反应的化学方程式:
Fe2O3→A___________ ;A→B___________ 。
③B→C可看到的现象是___________ 。
④将A的饱和溶液滴入沸水中并不断加热,可制得___________ 胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为___________ 效应。

(1)高温下,让铁粉与水蒸气反应,见题图。试管中发生反应的化学方程式是
(2)根据图回答问题

①往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色A
②写出上述过程中有关反应的化学方程式:
Fe2O3→A
③B→C可看到的现象是
④将A的饱和溶液滴入沸水中并不断加热,可制得
您最近一年使用:0次
名校
解题方法
10 . 常温下,下列各组离子在指定条件下一定能大量共存的是
A.0.1mol/LFeCl3液中:K+、NH 、I-、SCN- 、I-、SCN- |
B.加入铝粉有气泡冒出的溶液中:Cl-、Na+、NH 、K+ 、K+ |
C.0.1mol/LNa2CO3的溶液中:Ca2+、Na+、Cl-、NO |
D.pH=1的溶液中:Mg2+、SO 、K+、Cl- 、K+、Cl- |
您最近一年使用:0次
2023-04-06更新
|
110次组卷
|
2卷引用:云南省玉溪第一中学2022-2023学年高一上学期第一月考化学试题



