1 . 下列有关物质检验方法不合理的是
| A.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含有Fe2+ |
| B.用酸性KMnO4溶液检验Fe2(SO4)3溶液中是否含有FeSO4 |
| C.检验绿矾晶体是否已氧化变质,可将绿矾晶体溶于稀H2SO4后滴加KSCN溶液,再观察溶液是否变红 |
D.向某溶液中加入适量BaCl2溶液,产生白色沉淀,说明溶液中含有 |
您最近一年使用:0次
解题方法
2 . 下列离子方程式正确的是
A.钠与水反应: |
B. 溶液和过量澄清石灰水混合: 溶液和过量澄清石灰水混合: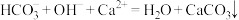 |
C.氯化铁溶液与碘化钾溶液反应: |
D.氯化镁溶液与氨水反应: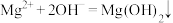 |
您最近一年使用:0次
解题方法
3 . 某化学实验室产生的废液中含有 、
、 、
、 三种金属离子,实验室设计如图所示方案对废液进行处理,以回收金属并制得氧化铁,保护环境。
三种金属离子,实验室设计如图所示方案对废液进行处理,以回收金属并制得氧化铁,保护环境。
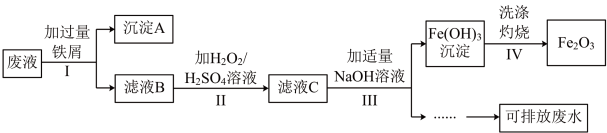
回答下列问题:
(1)步骤Ⅰ中分离沉淀A和滤液B的操作是_____ ,在实验室进行该操作时需要的玻璃仪器有_____ 。
(2)沉淀A中含有的金属单质是铁、_____ (填名称)。
(3)步骤Ⅱ中加入 溶液目的是
溶液目的是_____ (用离子方程式表示)。
(4)请检验步骤Ⅲ中 是否沉淀完全
是否沉淀完全_____
(5)“可排放废水”中含有的主要离子是_____ (填离子符号)。
 、
、 、
、 三种金属离子,实验室设计如图所示方案对废液进行处理,以回收金属并制得氧化铁,保护环境。
三种金属离子,实验室设计如图所示方案对废液进行处理,以回收金属并制得氧化铁,保护环境。
回答下列问题:
(1)步骤Ⅰ中分离沉淀A和滤液B的操作是
(2)沉淀A中含有的金属单质是铁、
(3)步骤Ⅱ中加入
 溶液目的是
溶液目的是(4)请检验步骤Ⅲ中
 是否沉淀完全
是否沉淀完全(5)“可排放废水”中含有的主要离子是
您最近一年使用:0次
解题方法
4 . 下列实验设计不能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 检验溶液中FeSO4是否被氧化 | 取少量待测液,滴加KSCN溶液,观察溶液颜色变化 |
| B | 净化实验室制备的Cl2 | 气体依次通过盛有饱和NaCl溶液、浓H2SO4的洗气瓶 |
| C | 测定NaOH溶液的pH | 将待测液滴在湿润的pH试纸上,与标准比色卡对照 |
| D | 验证Br2的氧化性比12强 | 将少量溴水加入KI溶液中,再加入几滴淀粉溶,振荡,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 分别依据下列实验事实,得出的结论正确的是
| 实验事实 | 结论 | |
| A | 向某钾盐溶液中加入浓盐酸产生的气体能使品红褪色 | 该钾盐只能是K2SO3或KHSO3 |
| B | 铝热剂加入盐酸后再加入KSCN溶液,溶液变红色 | 铝热剂中一定含有氧化铁 |
| C | 铜放入稀硫酸中,无明显现象,再加入硝酸钠固体,溶液变蓝,有明显的气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 向2mL0.1mol/L的硝酸银溶液中加入2mL0.1mol/LNaCl溶液,出现白色沉淀,再加入几滴0.1mol/LNa2S溶液,有黑色沉淀生成 | 氯化银的溶解度大于硫化银 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 某化学实验室产生的废液中含有 Fe3+、Cu2+、Ag+三种金属离子,甲同学设计了如图所示的方案对废液进行处理,以回收金属,下列说法正确的是
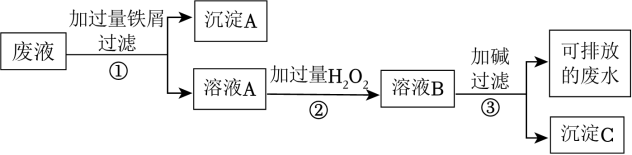

| A.沉淀A中含有2种金属单质 |
| B.可用KSCN溶液来检验溶液B中所含的金属离子 |
| C.溶液A若只经过操作③最终将无法得到沉淀C |
| D.操作①②③中都需要用到玻璃棒、漏斗 |
您最近一年使用:0次
2024-03-19更新
|
121次组卷
|
20卷引用:云南省楚雄天人中学2019-2020学年高一上学期12月月考化学试题
云南省楚雄天人中学2019-2020学年高一上学期12月月考化学试题江西省上高县第二中学2019-2020学年高一上学期第三次月考化学试题河北省安平中学2019-2020学年高一上学期第四次月考化学试题河北省保定市涞水波峰中学2019-2020学年高一下学期第三次质检考试化学试题山西省太原市第五中学2020-2021学年高一上学期12月阶段性检测化学试题宁夏石嘴山市第三中学2020-2021学年高一上学期第二次月考化学试题(已下线)【浙江新东方】在线化学 (14)(已下线)【浙江新东方】在线化学33浙江省淳安县汾口中学2020-2021学年高二12月月考化学试题四川师范大学附属中学2020-2021学年高一上学期12月月考化学试题云南省玉溪师范学院附属中学2021-2022学年高一下学期开学测试化学试题湖南省常德市桃源县第一中学2022-2023学年高三上学期9月月考化学试题甘肃省张掖市高台县第一中学2022-2023学年高一下学期开学检测化学试题浙江省淳安县汾口中学2023-2024学年高二上学期12月检测化学试题 浙江省温州市新力量联盟2018-2019学年高一上学期期末考试化学试题贵州省思南中学2018-2019学年高一下学期期末考试化学试题江苏省盐城市大丰区新丰中学2019-2020学年高一上学期期末考试化学试题(已下线)练习9 铁的多样性-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)河北省廊坊市第一中学2022~2023 学年高一上学期期末考试化学试题广东省广州天省实验学校2022-2023学年高一上学期期末考试化学试卷
7 . 碳酸锰可用作脱硫的催化剂,是合成二氧化锰和制造其他锰盐的原料。工业上从锰泥(主要含 和少量
和少量 、
、 、
、 等)中回收
等)中回收 的流程如图所示:
的流程如图所示:

回答下列问题:
(1)滤渣1中的主要成分是___________ 。
(2) 能将
能将 还原为.
还原为. .,写出该反应的离子方程式:
.,写出该反应的离子方程式:___________ 。
为检验 是否被氧化,可往滤液1中加入
是否被氧化,可往滤液1中加入___________ 溶液(填化学式)。
(3)写出加入氨水和过量 生成
生成 沉淀的离子方程式:
沉淀的离子方程式:___________ 。
(4)处理锰泥时, 、
、 混合溶液中
混合溶液中 比值不宜过大,请从节约药品的角度分析,原因是
比值不宜过大,请从节约药品的角度分析,原因是 ___________ 。
 和少量
和少量 、
、 、
、 等)中回收
等)中回收 的流程如图所示:
的流程如图所示:
回答下列问题:
(1)滤渣1中的主要成分是
(2)
 能将
能将 还原为.
还原为. .,写出该反应的离子方程式:
.,写出该反应的离子方程式:为检验
 是否被氧化,可往滤液1中加入
是否被氧化,可往滤液1中加入(3)写出加入氨水和过量
 生成
生成 沉淀的离子方程式:
沉淀的离子方程式:(4)处理锰泥时,
 、
、 混合溶液中
混合溶液中 比值不宜过大,请从节约药品的角度分析,原因是
比值不宜过大,请从节约药品的角度分析,原因是
您最近一年使用:0次
名校
8 . 下列“类比”合理的是
A. 与 与 固体在一定条件下生成 固体在一定条件下生成 ,则 ,则 与 与 在一定条件下生成 在一定条件下生成 |
B. 溶液与 溶液与 反应生成 反应生成 和 和 ,则 ,则 溶液与 溶液与 反应生成 反应生成 和 和 |
C.根据反应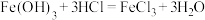 ,类比推出反应 ,类比推出反应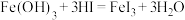 |
D. 固体与浓 固体与浓 加热可制 加热可制 ,则 ,则 固体与浓 固体与浓 加热制 加热制 |
您最近一年使用:0次
名校
9 . 自古至今,铁及其化合物在人类生产生活中的使用发挥了巨大的作用。铁元素的“价—类”二维图如图所示:
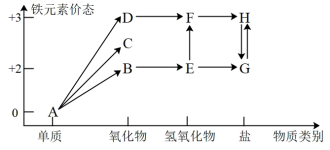
(1)E→F反应的化学方程式是________ ;反应过程的现象为_________ ;为制备并长时间观察物质E的颜色,某同学设计如下图的装置,请选择试管I中的药品为__________ 。(可供选择的药品为稀硫酸,氢氧化钠溶液,铁屑)

(2)某小组同学设计如下实验,研究亚铁盐与H2O2溶液的反应。
试剂:酸化的0.5 mol·L-1 G溶液,5% H2O2溶液
①上述实验中H2O2溶液与G溶液反应的离子方程式是___________ 。
②某同学认为上述实验中还可以进行改进:在2 mL酸化的G溶液中,先加入0.5mL煤油,再于液面下加入5滴5% H2O2溶液和KSCN溶液,煤油的作用是________ 。
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:________ 。
(4)高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾(K2FeO4)。在碱性条件下,用Fe(OH)3和次氯酸钾溶液来制备高铁酸钾,请写出制备高铁酸钾的离子方程式_____ 。
(5)某矿石中铁元素含量的测定:取2g该矿石用稀硫酸溶解,加入足量碘化钾溶液,再用浓度为0.1000 mol·L-1 Na2S2O3标准溶液去测定生成的I2的含量,原理为 2
2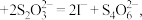 消耗20.00mLNa2S2O3,则该矿石中铁元素的含量为
消耗20.00mLNa2S2O3,则该矿石中铁元素的含量为___________ 。(用质量分数表示)

(1)E→F反应的化学方程式是

(2)某小组同学设计如下实验,研究亚铁盐与H2O2溶液的反应。
试剂:酸化的0.5 mol·L-1 G溶液,5% H2O2溶液
| 操作 | 现象 |
| 取2 mL酸化的G溶液于试管中,加入5滴5% H2O2溶液 | 溶液立即变为棕黄色,稍后,产生气体 |
| 向反应后的溶液中加入KSCN溶液 | 溶液变红 |
②某同学认为上述实验中还可以进行改进:在2 mL酸化的G溶液中,先加入0.5mL煤油,再于液面下加入5滴5% H2O2溶液和KSCN溶液,煤油的作用是
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
(4)高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾(K2FeO4)。在碱性条件下,用Fe(OH)3和次氯酸钾溶液来制备高铁酸钾,请写出制备高铁酸钾的离子方程式
(5)某矿石中铁元素含量的测定:取2g该矿石用稀硫酸溶解,加入足量碘化钾溶液,再用浓度为0.1000 mol·L-1 Na2S2O3标准溶液去测定生成的I2的含量,原理为
 2
2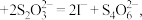 消耗20.00mLNa2S2O3,则该矿石中铁元素的含量为
消耗20.00mLNa2S2O3,则该矿石中铁元素的含量为
您最近一年使用:0次
名校
解题方法
10 . 铁是人类较早使用的金属之一、运用所学知识,回答下列问题。
(1)用赤铁矿来进行高炉炼铁,总共消耗了标况下6.72 LCO气体,则生成Fe的质量为_____ 。
(2)不仅溶液中Fe2+易被氧化成Fe2+,溶液中白色沉淀Fe(OH)2更易被O2氧化,请写出反应的化学方程式_________ ,现象为_________ 。
(3)某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
①甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变血红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为________ 。
②乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_________ 。
③丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为_________ 。
(1)用赤铁矿来进行高炉炼铁,总共消耗了标况下6.72 LCO气体,则生成Fe的质量为
(2)不仅溶液中Fe2+易被氧化成Fe2+,溶液中白色沉淀Fe(OH)2更易被O2氧化,请写出反应的化学方程式
(3)某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
①甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变血红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为
②乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
③丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次



