解题方法
1 . 铁及其重要化合物之间的部分转化关系如图所示。
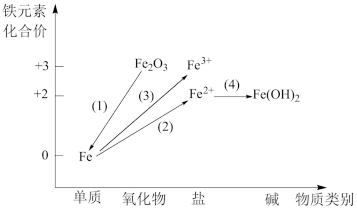
(1)下列金属矿物中用于冶炼金属铁的是___________ (填序号);
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
(2)实现Fe转化为Fe2+可选用足量的___________ (填序号);
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
(3)在加热的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为___________ 色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为___________ ;
(4)某同学将FeSO4溶液与NaOH溶液混合,未观察到白色沉淀,分析原因是生成的Fe(OH)2易被空气中的O2氧化,写出Fe(OH)2被氧化的化学方程式___________ ,请你设计一个防止Fe(OH)2被O2氧化的实验方案 ___________ 。

(1)下列金属矿物中用于冶炼金属铁的是
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
(2)实现Fe转化为Fe2+可选用足量的
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
(3)在加热的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为
(4)某同学将FeSO4溶液与NaOH溶液混合,未观察到白色沉淀,分析原因是生成的Fe(OH)2易被空气中的O2氧化,写出Fe(OH)2被氧化的化学方程式
您最近一年使用:0次
解题方法
2 . 某工厂的废金属屑中主要成分为 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,为变废为宝,该工厂利用废金属制取氯化铝、绿矾晶体
,为变废为宝,该工厂利用废金属制取氯化铝、绿矾晶体 和胆矾晶体
和胆矾晶体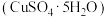 。
。

(1)步骤Ⅰ中,发生的非氧化还原反应的离子方程式为_______ ,涉及到的分离操作是_______ ,该分离操作中常用的玻璃仪器有_______ 。
(2)步骤Ⅱ中,发生反应的离子方程式为_______ 。若用大理石与浓盐酸制取 并通入溶液
并通入溶液 中,一段时间后,观察到溶液中产生的白色沉淀逐渐减少,为避免固体
中,一段时间后,观察到溶液中产生的白色沉淀逐渐减少,为避免固体 减少,可采取的改进措施是
减少,可采取的改进措施是_______ 。
(3)试剂 是
是_______ ,溶液 在空气中易被氧化,设计一个简单的实验方案检验溶液
在空气中易被氧化,设计一个简单的实验方案检验溶液 是否被氧化
是否被氧化_______ 。选择合理试剂确定溶液 未被全部氧化,可选择
未被全部氧化,可选择_______ 试剂。
①氯水② 溶液③
溶液③ 溶液④
溶液④ 酸性溶液
酸性溶液
(4) 溶液制取胆矾晶体需经过
溶液制取胆矾晶体需经过_______ 、冷却结晶、过滤、干燥得到胆矾晶体。
(5)若实验室称取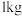 废金属
废金属 含铁元素
含铁元素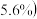 进行实验,假设每个过程反应都恰好完全进行,且忽略损失,则理论上得到
进行实验,假设每个过程反应都恰好完全进行,且忽略损失,则理论上得到_______  绿矾
绿矾 。
。
 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,为变废为宝,该工厂利用废金属制取氯化铝、绿矾晶体
,为变废为宝,该工厂利用废金属制取氯化铝、绿矾晶体 和胆矾晶体
和胆矾晶体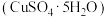 。
。
(1)步骤Ⅰ中,发生的非氧化还原反应的离子方程式为
(2)步骤Ⅱ中,发生反应的离子方程式为
 并通入溶液
并通入溶液 中,一段时间后,观察到溶液中产生的白色沉淀逐渐减少,为避免固体
中,一段时间后,观察到溶液中产生的白色沉淀逐渐减少,为避免固体 减少,可采取的改进措施是
减少,可采取的改进措施是(3)试剂
 是
是 在空气中易被氧化,设计一个简单的实验方案检验溶液
在空气中易被氧化,设计一个简单的实验方案检验溶液 是否被氧化
是否被氧化 未被全部氧化,可选择
未被全部氧化,可选择①氯水②
 溶液③
溶液③ 溶液④
溶液④ 酸性溶液
酸性溶液(4)
 溶液制取胆矾晶体需经过
溶液制取胆矾晶体需经过(5)若实验室称取
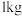 废金属
废金属 含铁元素
含铁元素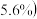 进行实验,假设每个过程反应都恰好完全进行,且忽略损失,则理论上得到
进行实验,假设每个过程反应都恰好完全进行,且忽略损失,则理论上得到 绿矾
绿矾 。
。
您最近一年使用:0次
名校
解题方法
3 . 下列说法不正确的是
| A.常用氯化铁溶液与铜反应制作印刷电路板 |
| B.硬铝是制造飞机和宇宙飞船的理想材料 |
| C.不锈钢是常见的合金钢,其合金元素主要是铬和镍 |
| D.储氢合金利用金属对氢气的物理吸附来达到储存氢气的目的 |
您最近一年使用:0次
4 . 实验室常采用点滴板来完成部分实验,这样既可以节约药品的用量,又便于观察实验现象。图中所示的实验点滴板上描述的实验现象或推论正确的是
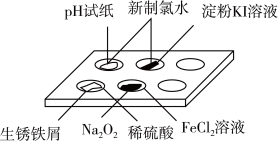
A.新制氯水滴加到 试纸以及淀粉 试纸以及淀粉 溶液孔穴中,都体现新制氯水的漂白性 溶液孔穴中,都体现新制氯水的漂白性 |
B.生锈铁屑加入过量稀硫酸反应后,若加入 后溶液褪色,说明该溶液中有 后溶液褪色,说明该溶液中有 存在 存在 |
C. 固体中滴加 固体中滴加 溶液后最终为白色沉淀 溶液后最终为白色沉淀 |
| D.生锈铁屑加入足量稀硫酸后,若加入KSCN溶液,溶液一定变血红色 |
您最近一年使用:0次
2023-10-03更新
|
782次组卷
|
12卷引用:浙江省北斗联盟2021-2022学年高一下学期期中联考化学试题
浙江省北斗联盟2021-2022学年高一下学期期中联考化学试题(已下线)第07练 铁及其化合物-2023年高考化学一轮复习小题多维练(全国通用)(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(1-10)河北省石家庄二中实验学校2023-2024学年高一上学期12月月考化学试题河北省部分重点高中2023-2024学年高三上学期第一次综合素养测评化学试题广东省河源中学2023-2024学年上学期高三年级一调考试化学试题河北省衡水中学2023-2024学年高三上学期一调考试化学试题河北省石家庄市部分名校2024届高三上学期一调考试化学试题内蒙古赤峰二中2023-2024学年高三上学期第三次月考化学试题辽宁省沈阳市第二中学2023-2024学年高三上学期期末模拟考试化学试题河北省唐山市第二十三中2023-2024学年高三上学期期中考试化学试题(已下线)专题3 金属及其化合物-钠及其重要化合物
解题方法
5 . 除去下列物质中的杂质,所用试剂和方法均正确的是
| 序号 | 物质 | 杂质 | 除杂所用试剂和方法 |
| A |  |  | 先加入过量铁粉,再过滤 |
| B |  溶液 溶液 |  溶液 溶液 | 先加入适量澄清石灰水,再过滤 |
| C |  |  | 先加入过量 溶液,再过滤 溶液,再过滤 |
| D |  |  | 在空气中加热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 下列各组离子能在溶液中,一定能大量共存的是
A.使 变红的溶液中: 变红的溶液中: 、 、 、 、 、 、 |
B.使酚酞变红的溶液中: 、 、 、 、 、 、 |
C.与Al反应放出 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.澄清透明的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
7 . 绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。
(1)检验久置绿矾是否变质可用试剂___________ 。
(2)①工业上常用FeCl3溶液刻蚀铜电路板,反应的离子方程式为___________ 。腐蚀废液含FeCl3 、FeCl2 、CuCl2 ,某小组欲从腐蚀废液中回收铜及制绿矾,工艺流程如下:

②操作Ⅰ中使用的玻璃仪器除烧杯、玻璃棒外还有___________ ;腐蚀废液中加入过量铁粉的目的___________ 。
③固体A中含有___________ ;操作Ⅱ的过程是:蒸发至出现一层晶膜、___________ 、过滤、___________ 、常温晾干。
④反应Ⅰ中生成FeCO3沉淀同时有气体生成,反应的离子方程式为___________ 。
(3)绿矾可用于缺铁性贫血 补铁剂,医生建议与维生素C同服。某同学探究维生素C的作用,取少量 Fe2(SO4)3溶液于试管中,加入维生素C片2片,并振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论
补铁剂,医生建议与维生素C同服。某同学探究维生素C的作用,取少量 Fe2(SO4)3溶液于试管中,加入维生素C片2片,并振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论___________ 。
(4)绿矾中结晶水含量测定:称量干燥坩埚的质量为m1,加入绿矾后总质量为m2,将坩埚加热后,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为m3;根据实验数据,绿矾分子中结晶水的个数为___________ (写表达式)。
(5)下列操作中,会导致结晶水数目测定值偏高的是___________ (填标号)。
①绿矾未充分干燥 ②坩埚未置于干燥器中冷却 ③加热时有少绿矾迸溅出来
(1)检验久置绿矾是否变质可用试剂
(2)①工业上常用FeCl3溶液刻蚀铜电路板,反应的离子方程式为

②操作Ⅰ中使用的玻璃仪器除烧杯、玻璃棒外还有
③固体A中含有
④反应Ⅰ中生成FeCO3沉淀同时有气体生成,反应的离子方程式为
(3)绿矾可用于缺铁性贫血
 补铁剂,医生建议与维生素C同服。某同学探究维生素C的作用,取少量 Fe2(SO4)3溶液于试管中,加入维生素C片2片,并振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论
补铁剂,医生建议与维生素C同服。某同学探究维生素C的作用,取少量 Fe2(SO4)3溶液于试管中,加入维生素C片2片,并振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论(4)绿矾中结晶水含量测定:称量干燥坩埚的质量为m1,加入绿矾后总质量为m2,将坩埚加热后,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为m3;根据实验数据,绿矾分子中结晶水的个数为
(5)下列操作中,会导致结晶水数目测定值偏高的是
①绿矾未充分干燥 ②坩埚未置于干燥器中冷却 ③加热时有少绿矾迸溅出来
您最近一年使用:0次
名校
解题方法
8 . 下列离子方程式书写正确的是
A.硫酸铝溶液中加入过量的氨水:Al3+ +4NH3·H2O=AlO +4NH +4NH + 2H2O + 2H2O |
B.稀硫酸与氢氧化钡反应:Ba2++OH-+H++SO =BaSO4↓+H2O =BaSO4↓+H2O |
C.过量SO2通入NaClO溶液中:ClO-+SO2+H2O=SO +Cl-+2H+ +Cl-+2H+ |
| D.FeCl3溶液与KSCN溶液反应:Fe3++3SCN- =Fe(SCN)3 ↓ |
您最近一年使用:0次
9 . 铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态,设计并进行了如下实验:
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是_______ (填名称),试剂2是_______ (填名称)。
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有_______ (填离子符号)。
(3)能证明溶液①中含有Fe2+的实验现象是_______ 。
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:_______ 。
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的 与NaClO发生了化学反应。
与NaClO发生了化学反应。
a.甲同学猜测的依据是_______ 。
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是_______ 。
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有
(3)能证明溶液①中含有Fe2+的实验现象是
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的
 与NaClO发生了化学反应。
与NaClO发生了化学反应。a.甲同学猜测的依据是
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是
您最近一年使用:0次
名校
解题方法
10 . 下列实验能达到目的或结论正确的是
| 选项 | 实验 | 方案设计 |
| A | 收集干燥纯净的N2 (杂质O2、CO2) | 将混合气体依次通过足量的氢氧化钠溶液、灼热的铜网,最后用真空气囊收集 |
| B | 探究Na2SO3是否变质 | 取少量固体溶于水,加入足量稀硝酸酸化,再加入BaCl2溶液 |
| C | 浓硫酸滴入蔗糖中,产生的气体导入澄清石灰水 | 蔗糖变黑、体积膨胀,澄清石灰水变浑浊,说明浓硫酸具有脱水性和强氧化性 |
| D | 过量铁粉加入稀硝酸中,充分反应后,滴加 溶液 溶液 | 有无色气泡产生,溶液呈血红色,稀硝酸能将 2+氧化成 2+氧化成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



