名校
1 . 实验室以含锌废液(主要成分为ZnSO4,含少量的Fe2+、Mn2+)为原料制备ZnCO3·2Zn(OH)2的实验流程如下:
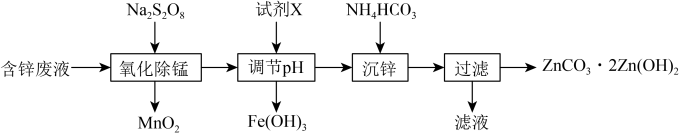
| A.溶液中的Fe2+可以用KSCN溶液检验 |
B.氧化除锰后的溶液中存在:Na+、Zn2+、Fe2+、SO |
| C.调节pH时试剂X可以选用Zn、ZnO、ZnCO3等物质 |
D.沉锌时的离子方程式为3Zn2++6HCO = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O |
您最近一年使用:0次
2 . Fe3O4呈黑色,有磁性,应用广泛。以Fe3O4为吸附剂去除水中含磷物质是一种新的除磷措施。请回答下列问题:
(1)检验Fe3O4中铁元素的价态:用盐酸溶解Fe3O4,再进行下列步骤:
①取少量溶液滴加KSCN溶液,溶液变_____ (填“红色”或“淡蓝色”),则证明Fe3O4中含有_____ 价的铁元素。
②另取少量溶液滴加K3[Fe(CN)6]溶液,产生化学式Fe3[Fe(CN)6]2的蓝色沉淀。则证明Fe3O4中含有_____ 价的铁元素。
(2)Fe3O4制备方法有多种,下面用氧化—沉淀法制备Fe3O4:
①向稀硫酸中加入过量铁粉,得到FeSO4溶液。空气中存在O2,由于_____ (用离子方程式表示),可产生Fe3+。过量铁粉的作用是除去Fe3+;
②在N2保护下,向热NaOH溶液中加入FeSO4溶液,搅拌,得到Fe(OH)2浊液。将NaNO3溶液滴入浊液中,充分反应得到Fe3O4.,用湿润红色石蕊试纸检验产物,试纸变_____ (填“红色”或“蓝色”),证明生成了NH3,发生的反应离子方程式为:12Fe(OH)2+ =4Fe3O4+NH3↑+X+10H2O,则X的化学式为
=4Fe3O4+NH3↑+X+10H2O,则X的化学式为_____ 。
(3)含磷各微粒在溶液中的物质的量分数与pH的关系如下图1所示。下列分析正确的是_____ 。
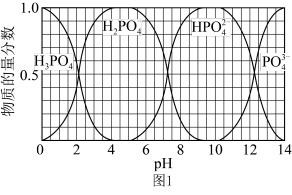
A.KH2PO4的水溶液中:c(H+)>c(OH-)
B.K2HPO4溶液显碱性
C.H3PO4是强电解质,在溶液中完全电离
(4)将Fe3O4加到KH2PO4溶液中,调节溶液的pH。Fe3O4由于异种电荷吸附而去除水中含磷物种,pH对吸附剂表面所带电荷的影响:pH<6.8,Fe3O4表面带正电荷;pH=6.8,Fe3O4表面不带电荷;pH>6.8,Fe3O4表面带负电荷。Fe3O4对含磷微粒的去除率随pH的变化如图2.则:

①pH=4~5时,吸附的主要微粒是_____ 。
②去除率的大小与吸附剂和含磷的主要微粒之间的静电排斥作用有关。与pH=5时相比,pH=9时的去除率明显下降,说明吸附剂和含磷的主要微粒之间的静电排斥作用:pH=9时_____ (填“强于”或“弱于”pH=5时)
(1)检验Fe3O4中铁元素的价态:用盐酸溶解Fe3O4,再进行下列步骤:
①取少量溶液滴加KSCN溶液,溶液变
②另取少量溶液滴加K3[Fe(CN)6]溶液,产生化学式Fe3[Fe(CN)6]2的蓝色沉淀。则证明Fe3O4中含有
(2)Fe3O4制备方法有多种,下面用氧化—沉淀法制备Fe3O4:
①向稀硫酸中加入过量铁粉,得到FeSO4溶液。空气中存在O2,由于
②在N2保护下,向热NaOH溶液中加入FeSO4溶液,搅拌,得到Fe(OH)2浊液。将NaNO3溶液滴入浊液中,充分反应得到Fe3O4.,用湿润红色石蕊试纸检验产物,试纸变
 =4Fe3O4+NH3↑+X+10H2O,则X的化学式为
=4Fe3O4+NH3↑+X+10H2O,则X的化学式为(3)含磷各微粒在溶液中的物质的量分数与pH的关系如下图1所示。下列分析正确的是

A.KH2PO4的水溶液中:c(H+)>c(OH-)
B.K2HPO4溶液显碱性
C.H3PO4是强电解质,在溶液中完全电离
(4)将Fe3O4加到KH2PO4溶液中,调节溶液的pH。Fe3O4由于异种电荷吸附而去除水中含磷物种,pH对吸附剂表面所带电荷的影响:pH<6.8,Fe3O4表面带正电荷;pH=6.8,Fe3O4表面不带电荷;pH>6.8,Fe3O4表面带负电荷。Fe3O4对含磷微粒的去除率随pH的变化如图2.则:

①pH=4~5时,吸附的主要微粒是
②去除率的大小与吸附剂和含磷的主要微粒之间的静电排斥作用有关。与pH=5时相比,pH=9时的去除率明显下降,说明吸附剂和含磷的主要微粒之间的静电排斥作用:pH=9时
您最近一年使用:0次
名校
解题方法
3 . 某化学实验室产生的废液中含有 Fe3+、Cu2+、Ag+三种金属离子,甲同学设计了如图所示的方案对废液进行处理,以回收金属,下列说法正确的是
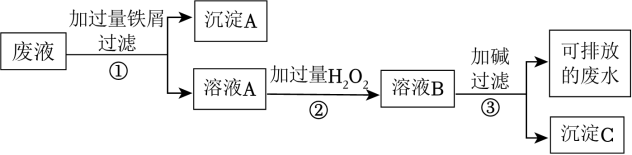

| A.沉淀A中含有2种金属单质 |
| B.可用KSCN溶液来检验溶液B中所含的金属离子 |
| C.溶液A若只经过操作③最终将无法得到沉淀C |
| D.操作①②③中都需要用到玻璃棒、漏斗 |
您最近一年使用:0次
2024-03-19更新
|
89次组卷
|
20卷引用:湖南省常德市桃源县第一中学2022-2023学年高三上学期9月月考化学试题
湖南省常德市桃源县第一中学2022-2023学年高三上学期9月月考化学试题云南省玉溪师范学院附属中学2021-2022学年高一下学期开学测试化学试题河北省廊坊市第一中学2022~2023 学年高一上学期期末考试化学试题广东省广州天省实验学校2022-2023学年高一上学期期末考试化学试卷浙江省温州市新力量联盟2018-2019学年高一上学期期末考试化学试题贵州省思南中学2018-2019学年高一下学期期末考试化学试题江西省上高县第二中学2019-2020学年高一上学期第三次月考化学试题河北省安平中学2019-2020学年高一上学期第四次月考化学试题江苏省盐城市大丰区新丰中学2019-2020学年高一上学期期末考试化学试题河北省保定市涞水波峰中学2019-2020学年高一下学期第三次质检考试化学试题山西省太原市第五中学2020-2021学年高一上学期12月阶段性检测化学试题宁夏石嘴山市第三中学2020-2021学年高一上学期第二次月考化学试题(已下线)【浙江新东方】在线化学 (14)(已下线)练习9 铁的多样性-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)(已下线)【浙江新东方】在线化学33浙江省淳安县汾口中学2020-2021学年高二12月月考化学试题云南省楚雄天人中学2019-2020学年高一上学期12月月考化学试题四川师范大学附属中学2020-2021学年高一上学期12月月考化学试题甘肃省张掖市高台县第一中学2022-2023学年高一下学期开学检测化学试题浙江省淳安县汾口中学2023-2024学年高二上学期12月检测化学试题
名校
4 . 实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁性材料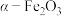 。其主要实验流程如下:
。其主要实验流程如下:
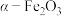 。其主要实验流程如下:
。其主要实验流程如下:
| A.酸浸:用一定浓度的硫酸浸取铁泥,能提高铁元素浸出率的措施有适当升高温度,加快搅拌速度 |
B.还原:向“酸浸”后的滤液中加入过量铁粉,可用KSCN溶液检验 是否完全还原 是否完全还原 |
C.沉铁:将提纯后的 溶液与氨水 溶液与氨水 混合溶液反应,生成 混合溶液反应,生成 沉淀的离子方程式为 沉淀的离子方程式为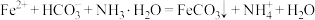 |
D.沉铁步骤中为防止生成 ,应在搅拌下向氨水 ,应在搅拌下向氨水 混合溶液中缓慢加入 混合溶液中缓慢加入 溶液 溶液 |
您最近一年使用:0次
2024-02-29更新
|
564次组卷
|
5卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期末测试化学试题
名校
解题方法
5 . 某实验小组测定铁的氧化物 的化学式,已知该氧化物中铁元素只有+2和+3两种价态,
的化学式,已知该氧化物中铁元素只有+2和+3两种价态, ,实验步骤如图,下列说法正确的是
,实验步骤如图,下列说法正确的是

 的化学式,已知该氧化物中铁元素只有+2和+3两种价态,
的化学式,已知该氧化物中铁元素只有+2和+3两种价态, ,实验步骤如图,下列说法正确的是
,实验步骤如图,下列说法正确的是
| A.步骤①和步骤②都发生了氧化还原反应 | B.溶液a中阳离子只有 和 和 |
C.溶液b中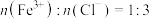 | D.计算可得该氧化物的化学式为: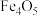 |
您最近一年使用:0次
2024-01-05更新
|
330次组卷
|
9卷引用:天津市新华中学2022-2023学年高三上学期第二次月考化学试题
天津市新华中学2022-2023学年高三上学期第二次月考化学试题辽宁省实验中学2022-2023学年高一上学期期中阶段测试化学试题北京市第五中学2022-2023学年高一上学期第二次阶段检测化学试题北京市海淀区第二十中学2022-2023学年高一上学期11月月考化学试题浙江省杭州第十四中学2022-2023学年高一上学期期末考试化学试题(已下线)高二上期末考化学194浙江省金华第一中学2023-2024学年高一上学期11月期中考试化学试题(已下线)寒假作业07 铁及其化合物-【寒假分层作业】2024年高一化学寒假培优练(人教版2019必修第一册)广西钦州市第四中学2023-2024学年高一上学期11月考试化学试卷
名校
6 . 化学小组探究Cu与Fe2(SO4)3溶液的反应,实验如下:
已知:经检验白色沉淀为CuSCN。
(1)实验i中发生反应的离子方程式为___________
(2)实验i中检测到Fe3+,依据的实验现象是___________
(3)对实验ii中Fe3+产生的原因作如下假设:
假设1:Cu与Fe2(SO4)3的反应是一个可逆反应
假设2:溶液中的Fe2+被___________ 氧化
假设3:在实验ii的条件下,Fe2+被Cu2+氧化
①将假设2补充完整
②通过查找___________ 数据,可定量判断Cu与Fe2(SO4)3的反应是否为可逆反应。
(4)设计实验验证假设。
资料:还原反应中,增大反应物浓度或降低生成物浓度,氧化剂氧化性增强,还原反应越易发生。
①假设1不成立的实验证据是___________
②实验iii的目的是___________
③溶液a是___________
④结合电极反应以及资料,解释实验ii中Fe3+产生的原因___________
| 序号 | 实验方案 | 实验现象 |
| 实验i |  | 振荡试管,观察到溶液变为蓝色,待反应充分后,试管底部有 Cu粉剩余。 |
| 实验ii | 取实验i中的上层清液,向其中滴加0.1mol·L-1 KSCN溶液 | 溶液局部变红,同时产生白色沉淀,振荡试管,红色消失。 |
(1)实验i中发生反应的离子方程式为
(2)实验i中检测到Fe3+,依据的实验现象是
(3)对实验ii中Fe3+产生的原因作如下假设:
假设1:Cu与Fe2(SO4)3的反应是一个可逆反应
假设2:溶液中的Fe2+被
假设3:在实验ii的条件下,Fe2+被Cu2+氧化
①将假设2补充完整
②通过查找
(4)设计实验验证假设。
资料:还原反应中,增大反应物浓度或降低生成物浓度,氧化剂氧化性增强,还原反应越易发生。
| 序号 | 实验iii | 实验iv |
| 方案 | 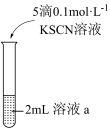 | 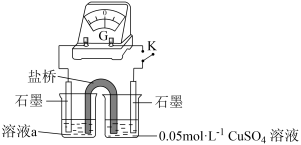 |
| 现象 | 放置较长时间,溶液颜色不变红 | 闭合开关K,电流计指针不动,向右侧CuSO4溶液中滴加0.1mol·L-1KSCN,指针向右大幅度偏转,溶液中有白色浑浊物产生。取出左侧溶液,滴加0.1mol·L-1KSCN,溶液变红。 |
②实验iii的目的是
③溶液a是
④结合电极反应以及资料,解释实验ii中Fe3+产生的原因
您最近一年使用:0次
名校
7 . 超顺磁性的Fe3O4粒子(平均直径为25nm)在医疗上有重要作用,实验室制备方法如下:在有N2保护和剧烈搅拌条件下,向FeCl3、FeCl2的混合溶液中滴加氨水,可得到黑色的Fe3O4。实验装置如图所示:

请回答下列问题:
(1)恒压滴液漏斗的作用是___________ 。
(2)Fe3O4中铁元素的化合价为___________ ,通入N2的目的是___________ 。
(3)制备超顺磁性的Fe3O4粒子反应原理的离子方程式为___________ 。
(4)充分反应后,将三颈烧瓶中的混合物通过离心分离,然后水洗,最后用无水乙醇洗涤。为了检验超顺磁性粒子中含有+2价的铁元素,需要的化学试剂为___________(填序号)。
(5)实验制得的超顺磁性的Fe3O4粒子中含有少量的Fe(OH)3,为测定Fe3O4的含量,称取mg试样放在小烧杯中,用足量稀硫酸溶解后定容于100mL容量瓶中,准确量取20.00mL溶液置于锥形瓶中,然后用cmol·L-1KMnO4溶液进行滴定,当___________ 时停止滴定,然后重复滴定操作,平均消耗KMnO4溶液VmL,该样品的纯度为___________ 。

请回答下列问题:
(1)恒压滴液漏斗的作用是
(2)Fe3O4中铁元素的化合价为
(3)制备超顺磁性的Fe3O4粒子反应原理的离子方程式为
(4)充分反应后,将三颈烧瓶中的混合物通过离心分离,然后水洗,最后用无水乙醇洗涤。为了检验超顺磁性粒子中含有+2价的铁元素,需要的化学试剂为___________(填序号)。
| A.KSCN溶液 | B.HCl溶液 | C.H2O2溶液 | D.K3[Fe(CN)6]溶液 |
(5)实验制得的超顺磁性的Fe3O4粒子中含有少量的Fe(OH)3,为测定Fe3O4的含量,称取mg试样放在小烧杯中,用足量稀硫酸溶解后定容于100mL容量瓶中,准确量取20.00mL溶液置于锥形瓶中,然后用cmol·L-1KMnO4溶液进行滴定,当
您最近一年使用:0次
8 . 实验室常采用点滴板来完成部分实验,这样既可以节约药品的用量,又便于观察实验现象。图中所示的实验点滴板上描述的实验现象或推论正确的是
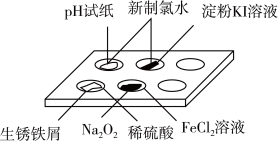

A.新制氯水滴加到 试纸以及淀粉 试纸以及淀粉 溶液孔穴中,都体现新制氯水的漂白性 溶液孔穴中,都体现新制氯水的漂白性 |
B.生锈铁屑加入过量稀硫酸反应后,若加入 后溶液褪色,说明该溶液中有 后溶液褪色,说明该溶液中有 存在 存在 |
C. 固体中滴加 固体中滴加 溶液后最终为白色沉淀 溶液后最终为白色沉淀 |
| D.生锈铁屑加入足量稀硫酸后,若加入KSCN溶液,溶液一定变血红色 |
您最近一年使用:0次
2023-10-03更新
|
639次组卷
|
11卷引用:第07练 铁及其化合物-2023年高考化学一轮复习小题多维练(全国通用)
(已下线)第07练 铁及其化合物-2023年高考化学一轮复习小题多维练(全国通用)(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(1-10)浙江省北斗联盟2021-2022学年高一下学期期中联考化学试题河北省部分重点高中2023-2024学年高三上学期第一次综合素养测评化学试题广东省河源中学2023-2024学年上学期高三年级一调考试化学试题河北省衡水中学2023-2024学年高三上学期一调考试化学试题河北省石家庄市部分名校2024届高三上学期一调考试化学试题内蒙古赤峰二中2023-2024学年高三上学期第三次月考化学试题辽宁省沈阳市第二中学2023-2024学年高三上学期期末模拟考试化学试题河北省唐山市第二十三中2023-2024学年高三上学期期中考试化学试题河北省石家庄二中实验学校2023-2024学年高一上学期12月月考化学试题
9 . 下列物质转化在给定条件下能实现的是
①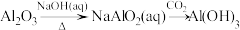
②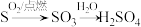
③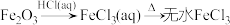
④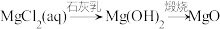
①
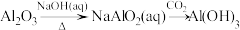
②
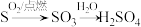
③
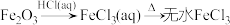
④
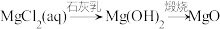
| A.①③ | B.②③ | C.②④ | D.①④ |
您最近一年使用:0次
名校
解题方法
10 . 合理应用和处理氮的化合物,在生产生活中有重要意义。
Ⅰ.NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2,反应产物还有另外两种盐。完成下列填空:
(1)写出上述化学方程式___________ 。
(2)上述反应恰好完全后,所得溶液呈弱碱性,则溶液中各离子浓度大小关系是___________ (不考虑二氧化碳的溶解)。
Ⅱ.氰化钠(NaCN)属于剧毒物质,可用双氧水或硫代硫酸钠处理。
(3)用双氧水处理,发生的反应为:NaCN+H2O2+H2O→A+NH3↑(已配平),则A的化学式为___________ 。
(4)NaCN与Na2S2O3二者等物质的量反应后的溶液中,大量存在的阴离子只有两种且都含硫元素,其中一种遇到Fe3+显血红色,该离子是___________ ,另一种离子是___________ 。
Ⅰ.NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2,反应产物还有另外两种盐。完成下列填空:
(1)写出上述化学方程式
(2)上述反应恰好完全后,所得溶液呈弱碱性,则溶液中各离子浓度大小关系是
Ⅱ.氰化钠(NaCN)属于剧毒物质,可用双氧水或硫代硫酸钠处理。
(3)用双氧水处理,发生的反应为:NaCN+H2O2+H2O→A+NH3↑(已配平),则A的化学式为
(4)NaCN与Na2S2O3二者等物质的量反应后的溶液中,大量存在的阴离子只有两种且都含硫元素,其中一种遇到Fe3+显血红色,该离子是
您最近一年使用:0次



