1 . 下列有关物质的性质与用途不具有对应关系的是
| A.干冰升华时吸热,可用作人工降雨 |
B. 吸收 吸收 产生 产生 ,可用作呼吸面具供氧剂 ,可用作呼吸面具供氧剂 |
C. 溶液显酸性,可蚀刻印刷电路板上的Cu 溶液显酸性,可蚀刻印刷电路板上的Cu |
D. 固体受热分解产生 固体受热分解产生 ,可用作膨松剂 ,可用作膨松剂 |
您最近一年使用:0次
2 . 下列实验对应的解释或结论正确的是
| 选项 | 实验 | 解释或结论 |
| A | 室温下,向含少量 的 的 溶液中加入铜屑,充分搅拌,过滤,得蓝色溶液 溶液中加入铜屑,充分搅拌,过滤,得蓝色溶液 | 杂质 被除去,得到纯净的 被除去,得到纯净的 溶液 溶液 |
| B |  晶体溶于稀硫酸,滴加 晶体溶于稀硫酸,滴加 溶液,溶液变红 溶液,溶液变红 |  晶体已变质 晶体已变质 |
| C | 向铅丹 中滴加浓盐酸,生成黄绿色气体 中滴加浓盐酸,生成黄绿色气体 | 氧化性: |
| D | 将铁的氧化物溶于过量稀盐酸中,再滴加几滴酸性 溶液,紫红色褪去 溶液,紫红色褪去 | 铁的氧化物含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列实验设计不能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 证明氧化性Cl2>Br2>I2 | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 |
| B | 比较水和乙醇中氢的活泼性 | 分别将少量钠投入到盛有水和乙醇的烧杯中 |
| C | 检验溶液中FeSO4是否被氧化 | 取少量待测液,滴加KSCN溶液,观察溶液颜色变化 |
| D | 工业酒精制备无水乙醇 | 工业酒精中加生石灰,蒸馏 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 氯化铁和氯化亚铁都是铁的重要化合物,下列说法错误的是
| A.饱和氯化铁溶液可制备氢氧化铁胶体 |
| B.氯化铁溶液可腐蚀覆铜板 |
| C.氯化亚铁可由化合反应制得 |
D.向5mL混有少量泥土的浑浊水中加入2mL饱和 溶液,静置5min,溶液变澄清 溶液,静置5min,溶液变澄清 |
您最近一年使用:0次
5 . 由硫铁矿烧渣(主要含Fe2O3、Al2O3、SiO2)制取绿矾的流程如下:
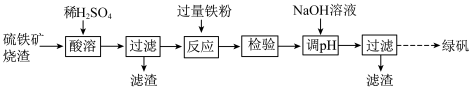
下列有关说法不正确的是

下列有关说法不正确的是
| A.“酸溶”时先将烧渣粉碎并不断搅拌,可提高铁元素的浸出率 |
| B.“反应”时发生的主要反应为2Fe3++Fe=3Fe2+ |
| C.“检验”时可用K4[Fe(CN)6]溶液检验上一步“反应”是否进行完全 |
| D.将第二次“过滤"所得滤液加热,经蒸发结晶可以制得绿矾 |
您最近一年使用:0次
6 . 下列实验操作过程中不会形成配位键的是
A. 溶于 溶于 中形成紫红色的溶液 中形成紫红色的溶液 |
B. 粉末溶于水形成蓝色的溶液 粉末溶于水形成蓝色的溶液 |
C.将硫氰化铵溶液滴加到含 的溶液中检验 的溶液中检验 |
D.向 溶液中加入过量的氨水 溶液中加入过量的氨水 |
您最近一年使用:0次
2024-03-29更新
|
322次组卷
|
3卷引用:湖南省岳阳市湘阴县知源高级中学等多校2023-2024学年高三上学期11月月考化学试题
7 . 分别依据下列实验事实,得出的结论正确的是
| 实验事实 | 结论 | |
| A | 向某钾盐溶液中加入浓盐酸产生的气体能使品红褪色 | 该钾盐只能是K2SO3或KHSO3 |
| B | 铝热剂加入盐酸后再加入KSCN溶液,溶液变红色 | 铝热剂中一定含有氧化铁 |
| C | 铜放入稀硫酸中,无明显现象,再加入硝酸钠固体,溶液变蓝,有明显的气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 向2mL0.1mol/L的硝酸银溶液中加入2mL0.1mol/LNaCl溶液,出现白色沉淀,再加入几滴0.1mol/LNa2S溶液,有黑色沉淀生成 | 氯化银的溶解度大于硫化银 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 某研究小组设计了如下流程以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。已知:氯化亚砜(
。已知:氯化亚砜( )熔点
)熔点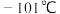 ,沸点
,沸点 ,易水解。
,易水解。
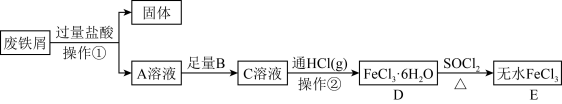
(1)为避免引入新的杂质,试剂 可以选用_________________(填编号)。
可以选用_________________(填编号)。
(2)操作②是蒸发结晶,加热的同时通入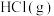 的目的是
的目的是_________________ 。
(3)取少量 晶体,溶于水并滴加
晶体,溶于水并滴加 溶液,现象是
溶液,现象是_________________ 。
(4)反应 的化学方程式为
的化学方程式为_________________ 。
(5)由 转化成
转化成 的过程中可能产生少量亚铁盐,写出一种可能的还原剂
的过程中可能产生少量亚铁盐,写出一种可能的还原剂_________________ ,并设计实验验证是该还原剂将 还原
还原_________________ 。
 杂质)为原料制备无水
杂质)为原料制备无水 。已知:氯化亚砜(
。已知:氯化亚砜( )熔点
)熔点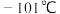 ,沸点
,沸点 ,易水解。
,易水解。
(1)为避免引入新的杂质,试剂
 可以选用_________________(填编号)。
可以选用_________________(填编号)。A. 溶液 溶液 | B.氯水 | C.溴水 | D. 溶液 溶液 |
(2)操作②是蒸发结晶,加热的同时通入
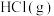 的目的是
的目的是(3)取少量
 晶体,溶于水并滴加
晶体,溶于水并滴加 溶液,现象是
溶液,现象是(4)反应
 的化学方程式为
的化学方程式为(5)由
 转化成
转化成 的过程中可能产生少量亚铁盐,写出一种可能的还原剂
的过程中可能产生少量亚铁盐,写出一种可能的还原剂 还原
还原
您最近一年使用:0次
解题方法
9 . 化学是以实验为基础的科学。下列实验方案不能达到实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 用铂丝蘸取待测液进行灼烧,透过蓝色钴玻璃观察焰色 | 检验待测液中是否含有 |
| B | 向盛有淀粉-KI溶液的试管中滴加几滴 溶液,振荡,观察溶液颜色变化 溶液,振荡,观察溶液颜色变化 | 检验 是否具有氧化性 是否具有氧化性 |
| C | 向KBr溶液中滴加几滴氯水,振荡,观察溶液颜色变化 | 验证 的氧化性比 的氧化性比 强 强 |
| D | 将铁粉溶于盐酸中,滴加KSCN溶液,观察溶液颜色变化 | 检验铁粉是否被氧化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-18更新
|
88次组卷
|
2卷引用:湖南省岳阳市湘阴县知源高级中学等多校2023-2024学年高三上学期11月月考化学试题
解题方法
10 . 铁及其化合物与生产、生活关系密切
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为__________
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是__________ (用化学方程式表示)
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:
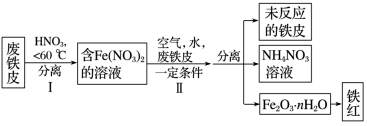
①步骤Ⅰ若要检验是否有Fe3+生成,方法是__________
②步骤Ⅱ中发生反应: ,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是
,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是__________ (任写一项)。
(4) Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4
______ Fe2O3+______NaClO+______KOH ______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
①K2FeO4中铁元素的化合价__________ ;配平上述反应__________ 。此过程中氧化剂是__________ (填化学式)。
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是__________ 、__________ 。
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤Ⅰ若要检验是否有Fe3+生成,方法是
②步骤Ⅱ中发生反应:
 ,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是
,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是(4) Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4
______ Fe2O3+______NaClO+______KOH
 ______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O①K2FeO4中铁元素的化合价
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是
您最近一年使用:0次



