解题方法
1 . 加碘盐的推广让我国基本杜绝了“碘缺乏症”,我国在部分缺铁人群中又推广了“加铁盐”。某学习小组进行实验探究一种加铁盐(成分表中加铁成分为FeSO4,加碘成分为KIO3)的成分。
(1)配制溶液:准确称量10.00g该加铁盐,配制100mL加铁盐溶液。需要使用的玻璃仪器:烧杯、玻璃棒、____ 、____ 。
(2)离子检验:
①用洁净的铂丝蘸取溶液,灼烧铂丝,直接观察火焰呈黄色,甲同学认为含Na+,盐中未加KIO3,该加铁盐与宣传不符。“但乙同学进行实验,____ ,观察到火焰呈紫色,否定了甲同学的观点。
②另取适量溶液于试管中,先加入____ ,静置,用胶头滴管取上层清液于另一试管中,加足量稀硝酸和几滴____ 溶液,有白色沉淀,说明溶液中有Cl-。
(3)检验加铁成分:实验小组设计了以下实验,请完成表格。
(4)加铁盐国标是:含铁量为600-1000毫克每千克,含碘量不小于40毫克每千克。
定量测定:取20mL所配溶液,加入足量NaOH溶液,现象是____ ,充分反应后过滤,加热固体至质量不再变化,用分析天平称量剩余红色固体2.40mg,通过计算说明该加铁盐含铁量是否达标____ (请在答题卡写出计算过程)。
(1)配制溶液:准确称量10.00g该加铁盐,配制100mL加铁盐溶液。需要使用的玻璃仪器:烧杯、玻璃棒、
(2)离子检验:
①用洁净的铂丝蘸取溶液,灼烧铂丝,直接观察火焰呈黄色,甲同学认为含Na+,盐中未加KIO3,该加铁盐与宣传不符。“但乙同学进行实验,
②另取适量溶液于试管中,先加入
(3)检验加铁成分:实验小组设计了以下实验,请完成表格。
| 步骤 | 操作 | 现象 | 结论 |
| 步骤1 | 取所配溶液,加入 | 无明显现象 | 溶液中存在Fe2+,且未变质 |
| 步骤2 | 继续向溶液中加入 |
定量测定:取20mL所配溶液,加入足量NaOH溶液,现象是
您最近一年使用:0次
解题方法
2 . 测定菠菜中铁元素的实验步骤包括菠菜脱水干燥、焙烧、酸浸、过滤、取滤液检验下列实验操作正确的是
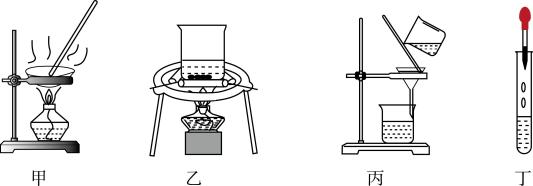

| A.装置甲焙烧 | B.装置乙酸浸 | C.装置丙过滤 | D.装置丁检验Fe3+ |
您最近一年使用:0次
名校
解题方法
3 . 回答下列问题:
(1)某同学写出以下三个化学方程式(未配平):
①
②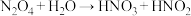
③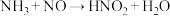
其中你认为一定不可能实现的是_______ (填序号)。
(2)下列三个氧化还原反应中
①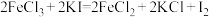
②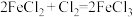
③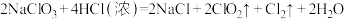
若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除Cl2单质外,还可以用上述反应中的_______ 做氧化剂。
(3)HNO2是一种弱酸,且不稳定,易分解生成NO和NO2,其中NO难溶于水,NO2易溶于水且能与水反应产生NO;HNO2是一种还原剂,能被常见的强氧化剂氧化,但在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+(还原性I->Fe2+)。AgNO2是一种难溶于水,易溶于酸的化合物。试回答下列问题:
①下列方法中,不能用来区分NaNO2和NaCl的是_______ (填序号)
A.加入稀硫酸,观察是否有气泡产生
B.在酸性条件下加入KI-淀粉溶液,观察溶液颜色
C.加入AgNO3溶液,观察是否有沉淀产生
②某同学把氯气通入到NaNO2溶液中,生成NaNO3和一种无氧酸,请写出反应的化学方程式:_______ 。
(4) Cl2、HClO、Ca(ClO)2、Na2O2等是中学教材中常见强氧化剂,已知+4价的硫既具氧化性又具还原性,以还原性为主。在次氯酸钙溶液中通入过量的SO2,有白色沉淀生成,其离子方程式为_______ 。
(1)某同学写出以下三个化学方程式(未配平):
①

②
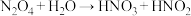
③
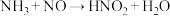
其中你认为一定不可能实现的是
(2)下列三个氧化还原反应中
①
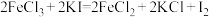
②
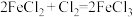
③
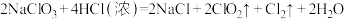
若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除Cl2单质外,还可以用上述反应中的
(3)HNO2是一种弱酸,且不稳定,易分解生成NO和NO2,其中NO难溶于水,NO2易溶于水且能与水反应产生NO;HNO2是一种还原剂,能被常见的强氧化剂氧化,但在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+(还原性I->Fe2+)。AgNO2是一种难溶于水,易溶于酸的化合物。试回答下列问题:
①下列方法中,不能用来区分NaNO2和NaCl的是
A.加入稀硫酸,观察是否有气泡产生
B.在酸性条件下加入KI-淀粉溶液,观察溶液颜色
C.加入AgNO3溶液,观察是否有沉淀产生
②某同学把氯气通入到NaNO2溶液中,生成NaNO3和一种无氧酸,请写出反应的化学方程式:
(4) Cl2、HClO、Ca(ClO)2、Na2O2等是中学教材中常见强氧化剂,已知+4价的硫既具氧化性又具还原性,以还原性为主。在次氯酸钙溶液中通入过量的SO2,有白色沉淀生成,其离子方程式为
您最近一年使用:0次
解题方法
4 . 某小组研究Cu和Fe(NO3)3溶液的反应原理。
(1)配制100mL 0.600mol·L-1 Fe(NO3)3溶液,需使用的仪器有_______(填标号)。
(2)提出假设
假设i:Fe(NO3)3溶液中的Fe3+将Cu氧化,反应的离子方程式为_______ ;
假设ii:Fe(NO3)3溶液中的NO 将Cu氧化,反应的离子方程式为3Cu+2NO
将Cu氧化,反应的离子方程式为3Cu+2NO +8H+=3Cu2++2NO↑+4H2O。
+8H+=3Cu2++2NO↑+4H2O。
(3)实验探究
实验Ⅰ:向0.600mol·L-1 Fe(NO3)3溶液中加入稍过量铜粉并不断振荡,溶液变成深棕色,无气泡产生。向上层清液中滴加2滴K3Fe(CN)6溶液,出现_______ ,说明有Fe2+生成。
实验Ⅱ:向0.200mol·L-1 HNO3溶液中加入稍过量铜粉并不断振荡,未见到明显淡蓝色。
已知:常温下,0.600mol·L-1 Fe(NO3)3溶液中的c(H+ )<0.200mol·L-1。
综合“实验Ⅰ”和“实验Ⅱ”,假设_______ (填 “i” 或 “ii” )一定成立。
(4)为探究“实验Ⅰ”中溶液变成深棕色的原因,设计了以下方案。请完成下表中的内容。
经分析推测,“实验I”中还存在以下反应:①3Fe2+ +NO +4H+=3Fe3+ +NO↑+2H2O;
+4H+=3Fe3+ +NO↑+2H2O;
②Fe2++NO=[Fe(NO)]2+(深棕色)。无气泡产生的原因是反应_______ (填“①”或“②”)的速率较快。
(1)配制100mL 0.600mol·L-1 Fe(NO3)3溶液,需使用的仪器有_______(填标号)。
A. | B. | C. | D.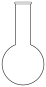 |
假设i:Fe(NO3)3溶液中的Fe3+将Cu氧化,反应的离子方程式为
假设ii:Fe(NO3)3溶液中的NO
 将Cu氧化,反应的离子方程式为3Cu+2NO
将Cu氧化,反应的离子方程式为3Cu+2NO +8H+=3Cu2++2NO↑+4H2O。
+8H+=3Cu2++2NO↑+4H2O。(3)实验探究
实验Ⅰ:向0.600mol·L-1 Fe(NO3)3溶液中加入稍过量铜粉并不断振荡,溶液变成深棕色,无气泡产生。向上层清液中滴加2滴K3Fe(CN)6溶液,出现
实验Ⅱ:向0.200mol·L-1 HNO3溶液中加入稍过量铜粉并不断振荡,未见到明显淡蓝色。
已知:常温下,0.600mol·L-1 Fe(NO3)3溶液中的c(H+ )<0.200mol·L-1。
综合“实验Ⅰ”和“实验Ⅱ”,假设
(4)为探究“实验Ⅰ”中溶液变成深棕色的原因,设计了以下方案。请完成下表中的内容。
| 序号 | 操作 | 现象 | 结论 |
| 实验Ⅲ | 向 | 溶液变成蓝色 | |
| 实验Ⅳ | 向0.600mol·L-1 Fe(NO3)3溶液中加入稍过量铜粉并不断振荡,用传感器检测反应过程中c(NO )的变化情况 )的变化情况 | 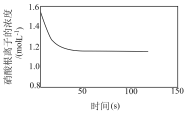 |
 +4H+=3Fe3+ +NO↑+2H2O;
+4H+=3Fe3+ +NO↑+2H2O;②Fe2++NO=[Fe(NO)]2+(深棕色)。无气泡产生的原因是反应
您最近一年使用:0次
解题方法
5 . 金属材料研究机构中测试工程师利用化学检测方法对金属材料组成进行分析,下列试剂可用来与金属材料反应检测出有铁单质的是
A. 溶液 溶液 | B.NaOH溶液 |
| C.KSCN溶液 | D.稀硫酸、 溶液 溶液 |
您最近一年使用:0次
6 . 黑色固体X为2种物质的混合物,共含有3种常见元素。取两份质量均为ag的试样X分别进行实验,反应过程和现象如下图所示。溶液E中滴加KSCN溶液不变色,放置在空气中会慢慢变为血红色。

请回答:
(1)X中含有的3种元素是O、_______ ,生成血红色物质的化学式是_______ 。
(2)生成红色固体单质D的离子方程式为_______ 。
(3)检验气体C成分的方法是_______ 。
(4)若又知固体D的质量是bg,用a、b表示试样X中两种物质的质量比_______ 。

请回答:
(1)X中含有的3种元素是O、
(2)生成红色固体单质D的离子方程式为
(3)检验气体C成分的方法是
(4)若又知固体D的质量是bg,用a、b表示试样X中两种物质的质量比
您最近一年使用:0次
7 . 下列说法正确的是
| A.金属钠着火时可用泡沫灭火器灭火 |
| B.做焰色试验的铂丝需用盐酸洗净,并在火焰上灼烧至与原火焰颜色相同 |
C.为除去 溶液中的 溶液中的 杂质,可加入足量铜粉充分反应后过滤 杂质,可加入足量铜粉充分反应后过滤 |
D.纯净的 能在 能在 中安静燃烧,发出苍白色火焰,集气瓶口有白烟 中安静燃烧,发出苍白色火焰,集气瓶口有白烟 |
您最近一年使用:0次
名校
解题方法
8 . 下列有关 的说法正确的是
的说法正确的是
 的说法正确的是
的说法正确的是A. 溶液可做刻制印刷电路板的“腐蚀液” 溶液可做刻制印刷电路板的“腐蚀液” |
B.向 溶液滴加几滴 溶液滴加几滴 溶液,产生红褐色沉淀和臭鸡蛋气味气体 溶液,产生红褐色沉淀和臭鸡蛋气味气体 |
C.蒸干 溶液可制得 溶液可制得 固体 固体 |
D. 溶液的配制是将其固体加入硫酸中抑制其水解 溶液的配制是将其固体加入硫酸中抑制其水解 |
您最近一年使用:0次
9 . 利用生物浸出黄铜矿(主要成分CuFeS2,含有少量SiO2杂质)回收其中铁和铜的工艺流程如图:
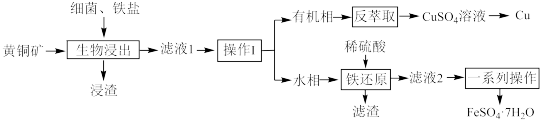
回答下列问题:
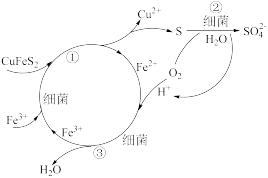
(1)Cu2+的生物浸出原理如图:浸出温度不宜过高,其原因是_____ ,反应①的离子方程式为____ 。
(2)浸渣的主要成分为____ (填化学式),操作1的名称为____ 。
(3)分离Cu2+的原理如下:Cu2++2(HR)org (CuR2)org+2H+。根据流程,反萃取加入的试剂应该为
(CuR2)org+2H+。根据流程,反萃取加入的试剂应该为_____ (填化学式)。
(4)检验滤液2中是否存在Fe3+,可选用_____ (填标号)。
(5)“一系列操作”包括_____ 、洗涤、干燥。

回答下列问题:
(1)Cu2+的生物浸出原理如图:浸出温度不宜过高,其原因是

(2)浸渣的主要成分为
(3)分离Cu2+的原理如下:Cu2++2(HR)org
 (CuR2)org+2H+。根据流程,反萃取加入的试剂应该为
(CuR2)org+2H+。根据流程,反萃取加入的试剂应该为(4)检验滤液2中是否存在Fe3+,可选用
| A.KSCN溶液 | B.K4[Fe(CN)6]溶液 | C.K3[Fe(CN)6]溶液 | D.KMnO4溶液 |
(5)“一系列操作”包括
您最近一年使用:0次
10 . 回答下列问题。
(1)实验室常用如图所示装置来制取和观察 在空气中被氧化时颜色的变化。
在空气中被氧化时颜色的变化。
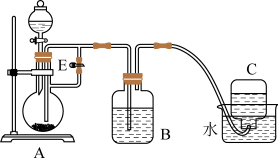
实验时在A中加入铁屑和稀硫酸,B中加入一定量的NaOH溶液,则A中发生的反应的离子方程式是:_________________ 。实验开始时先将活塞E___________ (填“打开”或“关闭”),C中收集到气体的主要成分是__________ 。实验结束后拔去装置B中的橡皮塞,使空气进入,装置B中发生的现象为_________________________ 。
(2)从制造印刷电路板的腐蚀废液(主要含 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,处理流程如图所示:
溶液,处理流程如图所示:
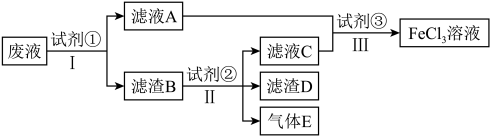
已知试剂①为铁,试剂②为稀盐酸,则滤渣B的成分为___________ ,若试剂③为氯水,则步骤Ⅱ的离子反应方程式为___________ ,检验废液中 存在的最佳试剂是
存在的最佳试剂是___________ (填标号),检验时实验现象为___________ 。
A.氢氧化钠溶液 B.酸性 溶液 C.氯水 D.KSCN溶液
溶液 C.氯水 D.KSCN溶液
(1)实验室常用如图所示装置来制取和观察
 在空气中被氧化时颜色的变化。
在空气中被氧化时颜色的变化。
实验时在A中加入铁屑和稀硫酸,B中加入一定量的NaOH溶液,则A中发生的反应的离子方程式是:
(2)从制造印刷电路板的腐蚀废液(主要含
 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,处理流程如图所示:
溶液,处理流程如图所示:
已知试剂①为铁,试剂②为稀盐酸,则滤渣B的成分为
 存在的最佳试剂是
存在的最佳试剂是A.氢氧化钠溶液 B.酸性
 溶液 C.氯水 D.KSCN溶液
溶液 C.氯水 D.KSCN溶液
您最近一年使用:0次



