名校
解题方法
1 . 合理应用和处理氮的化合物,在生产生活中有重要意义。
Ⅰ.NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2,反应产物还有另外两种盐。完成下列填空:
(1)写出上述化学方程式___________ 。
(2)上述反应恰好完全后,所得溶液呈弱碱性,则溶液中各离子浓度大小关系是___________ (不考虑二氧化碳的溶解)。
Ⅱ.氰化钠(NaCN)属于剧毒物质,可用双氧水或硫代硫酸钠处理。
(3)用双氧水处理,发生的反应为:NaCN+H2O2+H2O→A+NH3↑(已配平),则A的化学式为___________ 。
(4)NaCN与Na2S2O3二者等物质的量反应后的溶液中,大量存在的阴离子只有两种且都含硫元素,其中一种遇到Fe3+显血红色,该离子是___________ ,另一种离子是___________ 。
Ⅰ.NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2,反应产物还有另外两种盐。完成下列填空:
(1)写出上述化学方程式
(2)上述反应恰好完全后,所得溶液呈弱碱性,则溶液中各离子浓度大小关系是
Ⅱ.氰化钠(NaCN)属于剧毒物质,可用双氧水或硫代硫酸钠处理。
(3)用双氧水处理,发生的反应为:NaCN+H2O2+H2O→A+NH3↑(已配平),则A的化学式为
(4)NaCN与Na2S2O3二者等物质的量反应后的溶液中,大量存在的阴离子只有两种且都含硫元素,其中一种遇到Fe3+显血红色,该离子是
您最近一年使用:0次
2 . 翡翠手镯(如图)的主要成分是硬玉,硬玉化学式为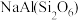 ,下列推测不合理的是
,下列推测不合理的是

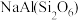 ,下列推测不合理的是
,下列推测不合理的是
A.硬玉与氢氧化钠溶液反应生成 、 、 和 和 |
| B.翡翠硬度大,熔点高,受到猛烈撞击不容易断裂或粉碎 |
C.碳酸钠与氧化铝、二氧化硅在高温熔融的条件下能制取硬玉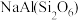 |
D.翡翠中含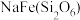 ,高温分解翡翠,产物溶于氢碘酸加 ,高温分解翡翠,产物溶于氢碘酸加 萃取,有机层呈紫红色 萃取,有机层呈紫红色 |
您最近一年使用:0次
3 . 下列有关说法正确的是
| A.二氧化硫与双氧水反应生成三氧化硫 |
| B.铝粉与氧化镁反应可制得镁 |
C.通过化合反应可制得 |
D.氨气通入溶有 的饱和氯化钠溶液可析出碳酸氢钠 的饱和氯化钠溶液可析出碳酸氢钠 |
您最近一年使用:0次
4 . 下列方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 证明 和 和 光照下发生取代反应 光照下发生取代反应 | 将装有干燥 的集气瓶倒扣在装有干燥 的集气瓶倒扣在装有干燥 的集气瓶上,抽出玻璃片,置于光照条件下反应 的集气瓶上,抽出玻璃片,置于光照条件下反应 | 观察到集气瓶内出现白雾,则可证明 和 和 光照下发生取代反应 光照下发生取代反应 |
| B | 检验 溶液中是否含有 溶液中是否含有 | 将 溶液滴入到酸性 溶液滴入到酸性 溶液中 溶液中 | 观察到 溶液由紫红色变无色,证明 溶液由紫红色变无色,证明 溶液中含有 溶液中含有 |
| C | 探究 、 、 、 、 的氧化性强弱 的氧化性强弱 | ①向NaBr溶液中通入足量 ②将①通入  后的溶液加入KI淀粉溶液中 后的溶液加入KI淀粉溶液中 | NaBr溶液变橙黄色,KI淀粉溶液变蓝色,证明氧化性 |
| D | 探究 、 、 对 对 分解的催化效果 分解的催化效果 | 在a、b两支试管中各加 溶液,分别滴入 溶液,分别滴入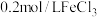 溶液和 溶液和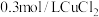 溶液各5滴 溶液各5滴 | a中产生气泡速率快于b中,说明 的催化效果要好于 的催化效果要好于 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-23更新
|
238次组卷
|
2卷引用:浙江省9+1高中联盟2022-2023学年高二上学期11月期中联考化学试题
5 . 某小组模拟工业制备KSCN,其原理如下: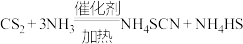 ;
;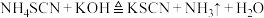 。回答下列问题:
。回答下列问题:
(1)向三颈瓶中滴加KOH溶液的仪器名称是_______ 。
(2)试剂1可能是_______ (填标号,下同),试剂2可能是_______ 。(不考虑其他反应的发生)
a.稀硫酸 b.四氯化碳
(3)步骤②和③中都要“保温”,其目的是_______ 。
(4)分离提纯粗产品的操作包括过滤、蒸发浓缩、降温结晶、过滤、冷水洗涤、干燥。用冷水洗涤,不用热水洗涤,其主要目的是_______ 。如果 过量,在第一次过滤和蒸发浓缩之间增加实验操作
过量,在第一次过滤和蒸发浓缩之间增加实验操作_______ (填名称)。
(5)为了探究 和
和 氧化性的相对强弱,设计如下实验:在
氧化性的相对强弱,设计如下实验:在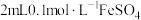 溶液中加入过量的
溶液中加入过量的 的
的 溶液,再向溶液中加入适量戊醇和KSCN溶液,戊醇层变蓝色。写出发生氧化还原反应的离子方程式:
溶液,再向溶液中加入适量戊醇和KSCN溶液,戊醇层变蓝色。写出发生氧化还原反应的离子方程式:_______ 。(已知在 溶液中加入戊醇,再滴加KSCN溶液,戊醇层变蓝色)
溶液中加入戊醇,再滴加KSCN溶液,戊醇层变蓝色)
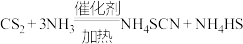 ;
;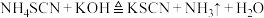 。回答下列问题:
。回答下列问题:
(1)向三颈瓶中滴加KOH溶液的仪器名称是
(2)试剂1可能是
a.稀硫酸 b.四氯化碳
(3)步骤②和③中都要“保温”,其目的是
(4)分离提纯粗产品的操作包括过滤、蒸发浓缩、降温结晶、过滤、冷水洗涤、干燥。用冷水洗涤,不用热水洗涤,其主要目的是
 过量,在第一次过滤和蒸发浓缩之间增加实验操作
过量,在第一次过滤和蒸发浓缩之间增加实验操作(5)为了探究
 和
和 氧化性的相对强弱,设计如下实验:在
氧化性的相对强弱,设计如下实验:在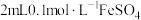 溶液中加入过量的
溶液中加入过量的 的
的 溶液,再向溶液中加入适量戊醇和KSCN溶液,戊醇层变蓝色。写出发生氧化还原反应的离子方程式:
溶液,再向溶液中加入适量戊醇和KSCN溶液,戊醇层变蓝色。写出发生氧化还原反应的离子方程式: 溶液中加入戊醇,再滴加KSCN溶液,戊醇层变蓝色)
溶液中加入戊醇,再滴加KSCN溶液,戊醇层变蓝色)
您最近一年使用:0次
2023-06-08更新
|
65次组卷
|
2卷引用:广东省2023届高三8月大联考化学试题(二)
解题方法
6 . 检验芹菜中铁元素的实验操作有:①剪碎芹菜,研磨;②取少量滤液,滴加稀 ;③加入蒸馏水,搅拌,过滤;④滴加几滴KSCN溶液,振荡,观察。正确操作顺序为
;③加入蒸馏水,搅拌,过滤;④滴加几滴KSCN溶液,振荡,观察。正确操作顺序为
 ;③加入蒸馏水,搅拌,过滤;④滴加几滴KSCN溶液,振荡,观察。正确操作顺序为
;③加入蒸馏水,搅拌,过滤;④滴加几滴KSCN溶液,振荡,观察。正确操作顺序为| A.③①④② | B.①②③④ | C.②①④③ | D.①③②④ |
您最近一年使用:0次
2023-06-02更新
|
274次组卷
|
4卷引用:2022年广东省高中学业平合格考试(新课标)化学试题
7 . 某小组探究一袋 “硫酸亚铁园艺精品肥料”的花肥是否变质并研究其相关性质。首先对该花肥的成分提出假设:
假设I:只含Fe2+;假设II:_______;假设III:只含Fe3+。
(1)假设II是_______ ,假设的依据是_______ (用文字表述)。
取适量花肥于试管中,加入适量稀硫酸溶解得到X溶液,进行如下实验:
(2)实验①发生反应的离子方程式为_______ 。
(3)由实验②可知,X溶液中一定含有_______ (填离子符号)。
为进一步验证假设,该小组又进行如下实验:
(4)通过实验③④可知,假设_______ (填“I”“II”或“III”)成立。
(5)该小组同学根据所学化学知识认为将变质的花肥与维生素C混合后溶于水,仍能正常使用。这是利用了维生素C的_______ (填“氧化性”或“还原性”)。
假设I:只含Fe2+;假设II:_______;假设III:只含Fe3+。
(1)假设II是
取适量花肥于试管中,加入适量稀硫酸溶解得到X溶液,进行如下实验:
| 实验序号 | 实验操作 | 实验现象 |
| ① | 取2 mL X溶液于试管中,滴加几滴酸性KMnO4溶液 | 溶液紫色褪去 |
| ② | 取2 mL X溶液于试管中,滴入1滴KSCN溶液 | 溶液显红色 |
(3)由实验②可知,X溶液中一定含有
为进一步验证假设,该小组又进行如下实验:
| 实验序号 | 实验操作 | 实验现象 |
| ③ | 取2 mL X溶液于试管中,加入1滴KSCN溶液,再加入1 mL H2O | 溶液显红色 |
| ④ | 取2 mL X溶液于试管中,加入1滴KSCN溶液,再加入1 mL新制氯水 | 溶液显红色,且比实验③中的红色深 |
(5)该小组同学根据所学化学知识认为将变质的花肥与维生素C混合后溶于水,仍能正常使用。这是利用了维生素C的
您最近一年使用:0次
2023-05-16更新
|
444次组卷
|
2卷引用:山东省烟台市2022-2023学年高一上学期期末考试化学试题
解题方法
8 . 铁、铝、铜是制造潜艇必不可少的重要金属材料。下列说法正确的是
| A.三种金属形成的氧化物均为碱性氧化物 |
| B.Cu不能与AlCl3溶液、FeCl3溶液发生反应 |
| C.任何情况下,三种金属都不能与水反应 |
| D.用惰性电极电解含有Fe3+、Al3+、Cu2+的混合溶液时Fe3+优先放电 |
您最近一年使用:0次
解题方法
9 . 以炼锌厂的烟道灰(主要成分ZnO,另含少量FeO、Fe2O3、SiO2等)为原料可以生产草酸锌晶体(ZnC2O4•2H2O)。

(1)为了提高“酸浸”时锌元素的浸出率,可以采取的措施有______ 。
(2)“氧化”后,需将溶液中过量的H2O2除去。除去H2O2的简便方法是______ 。
(3)“调pH”的目的是为了除去溶液中的Fe3+,可用______ (填试剂名称)检验Fe3+是否除净。
(4)已知H2C2O4溶液中部分微粒的物质的量分数随pH的变化曲线如图所示,ZnC2O4•2H2O微溶于水,不溶于乙醇。
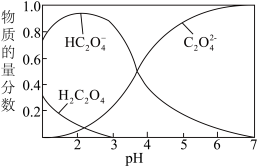
请补充完整由Zn(HC2O4)2溶液制备ZnC2O4•2H2O的实验方案:在搅拌下向Zn(HC2O4)2溶液中分批加入Zn(OH)2固体,至pH约为______ 时,停止加入Zn(OH)2固体,静置后过滤,用______ (填试剂名称)洗涤滤渣2-3次,干燥,密封包装。
(5)准确称取草酸锌晶体样品4.000g放置于锥形瓶中,加入足量的稀H2SO4溶液和适量蒸馏水,用0.5000mol/L的KMnO4溶液滴定至终点,消耗KMnO4溶液16.00mL。计算样品中ZnC2O4•2H2O的质量分数______ (写出计算过程)。(已知:2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O)

(1)为了提高“酸浸”时锌元素的浸出率,可以采取的措施有
| A.适当增加硫酸的浓度 | B.缩短酸浸的时间 |
| C.降低酸浸时的温度 | D.加快搅拌的速率 |
(3)“调pH”的目的是为了除去溶液中的Fe3+,可用
(4)已知H2C2O4溶液中部分微粒的物质的量分数随pH的变化曲线如图所示,ZnC2O4•2H2O微溶于水,不溶于乙醇。

请补充完整由Zn(HC2O4)2溶液制备ZnC2O4•2H2O的实验方案:在搅拌下向Zn(HC2O4)2溶液中分批加入Zn(OH)2固体,至pH约为
(5)准确称取草酸锌晶体样品4.000g放置于锥形瓶中,加入足量的稀H2SO4溶液和适量蒸馏水,用0.5000mol/L的KMnO4溶液滴定至终点,消耗KMnO4溶液16.00mL。计算样品中ZnC2O4•2H2O的质量分数
您最近一年使用:0次
22-23高一上·四川绵阳·期末
10 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 在空气中点燃氢气,然后把导管伸入盛满氯气的集气瓶中 | 氢气安静地燃烧,发出淡蓝色火焰 | 燃烧反应不一定要有氧气参加 |
| B | 将一小块钠投入盛有 溶液的烧杯中 溶液的烧杯中 | 烧杯底部析出红色固体 | 金属活动性: |
| C | 向 溶液中逐滴加入少量稀 溶液中逐滴加入少量稀 | 溶液导电能力不断减弱 | 生成的 不能发生电离 不能发生电离 |
| D | 向盛有 溶液的试管中滴加无色的维生素C溶液 溶液的试管中滴加无色的维生素C溶液 | 溶液黄色褪去 | 维生素 具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-18更新
|
340次组卷
|
3卷引用:2022年重庆高考真题化学试题变式题(选择题6-10)



