1 . 对Ⅰ~Ⅳ的实验操作现象判断不正确的是
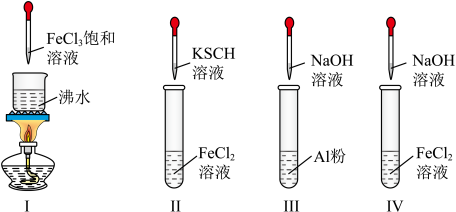
| A.实验Ⅰ:液体变为红褐色 |
| B.实验Ⅱ:溶液颜色变红 |
| C.实验Ⅲ:放出大量气体 |
| D.实验Ⅳ:先出现白色沉淀,迅速变成灰绿色,最后变成红褐色 |
您最近一年使用:0次
名校
解题方法
2 . 现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式: F_____________ 。
(2)反应⑤的离子方程式为_______________________________ 。
(3)反应①-⑦的7个反应属于氧化还原反应反应的有 (填选项代号)。
(4)向纯碱溶液中通入气体乙,可制得某种生产生活中常用的漂白、消毒的物质,同时有小苏打生成。该反应的化学方程式为___________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式: F
(2)反应⑤的离子方程式为
(3)反应①-⑦的7个反应属于氧化还原反应反应的有 (填选项代号)。
| A.①②④⑤⑥ | B.②③④⑥⑦ | C.①②③④⑤⑦ | D.全部 |
(4)向纯碱溶液中通入气体乙,可制得某种生产生活中常用的漂白、消毒的物质,同时有小苏打生成。该反应的化学方程式为
您最近一年使用:0次
名校
3 . 已知A常温常压下为无色液体,A为气体时与R反应生成B和E,M、R是两种常见的金属,M是地壳中含量最多的金属元素的单质,T是淡黄色固体,B. C是无色无味的气体,E是具有磁性的黑色晶体,H是红褐色固体。
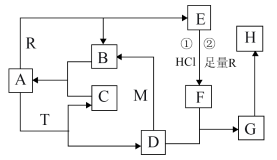
(1)物质T的化学式为___________ 。15.6g T与足量的A反应电子转移数为___________ 个(已知:阿伏伽德罗常数为NA)。
(2)D和M在溶液中反应生成B的离子反应方程式为___________ 。
(3)G在潮湿空气中转化为H的化学方程式为___________ 。
(4)T和F反应只生成C、H和一种盐,其离子反应方程式为_________ 。
(5)若向E和R的混合物中加入100mL 2mol/L的盐酸,恰好使混合物完全溶解,放出448mL(标准状况)气体,向所得溶液中加入KSCN溶液,无血红色出现。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为___________ g。

(1)物质T的化学式为
(2)D和M在溶液中反应生成B的离子反应方程式为
(3)G在潮湿空气中转化为H的化学方程式为
(4)T和F反应只生成C、H和一种盐,其离子反应方程式为
(5)若向E和R的混合物中加入100mL 2mol/L的盐酸,恰好使混合物完全溶解,放出448mL(标准状况)气体,向所得溶液中加入KSCN溶液,无血红色出现。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为
您最近一年使用:0次
2023-12-15更新
|
410次组卷
|
2卷引用:辽宁省实验中学2023-2024学年高一上学期12月化学试卷
名校
解题方法
4 . 下列关于钠、铁、氯及其化合物的说法错误的是
| A.钠着火时不能使用泡沫灭火器灭火 |
B. 与足量Fe反应,转移的电子的物质的量为2mol 与足量Fe反应,转移的电子的物质的量为2mol |
C.可用澄清石灰水鉴别 溶液和 溶液和 溶液 溶液 |
D. 和 和 均能通过化合反应制得 均能通过化合反应制得 |
您最近一年使用:0次
2023-12-13更新
|
442次组卷
|
2卷引用:辽宁省丹东市2023-2024学年高三上学期11月阶段测试化学试题
5 . 下列变化过程中不涉及氧化还原反应的是
A. 溶液使淀粉碘化钾试纸变蓝 溶液使淀粉碘化钾试纸变蓝 |
B.白色的 沉淀先变成灰绿色,后变成红褐色 沉淀先变成灰绿色,后变成红褐色 |
| C.将石蕊溶液滴入氯水中,溶液变红,随后迅速褪色 |
D.向 溶液中加入NaOH溶液,先产生白色沉淀,随后沉淀溶解 溶液中加入NaOH溶液,先产生白色沉淀,随后沉淀溶解 |
您最近一年使用:0次
2023-12-12更新
|
324次组卷
|
4卷引用:辽宁省部分学校2023-2024学年高一上学期12月月考化学试题
名校
解题方法
6 . 某小组用下图所示装置来制取 ,并观察其在空气中被氧化过程的颜色变化.实验时所使用的试剂有:铁屑、稀硫酸和氢氧化钠溶液.请完成下列问题:
,并观察其在空气中被氧化过程的颜色变化.实验时所使用的试剂有:铁屑、稀硫酸和氢氧化钠溶液.请完成下列问题:
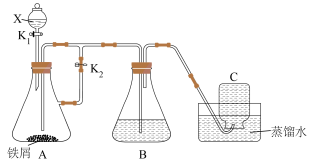
(1)仪器X的名称为___________ ;B中盛装的试剂为___________ .
(2)A中主要反应的离子方程式为___________ .
(3)配制氢氧化钠溶液时,为除去蒸馏水中溶解的 ,常采用的方法是
,常采用的方法是___________ .
(4)实验开始时应先将
___________ (填“关闭”或“打开”),再打开 .
.
(5)实验完毕后,取下装置B的橡胶塞,B瓶中可观察到的现象为___________ ,发生反应的化学方程式为___________ .
(6)实验中产生 的作用有
的作用有___________ (填序号).
A.排出装置内的空气
B.将A中溶液压入B中
C.保护 不被空气氧化
不被空气氧化
 ,并观察其在空气中被氧化过程的颜色变化.实验时所使用的试剂有:铁屑、稀硫酸和氢氧化钠溶液.请完成下列问题:
,并观察其在空气中被氧化过程的颜色变化.实验时所使用的试剂有:铁屑、稀硫酸和氢氧化钠溶液.请完成下列问题:
(1)仪器X的名称为
(2)A中主要反应的离子方程式为
(3)配制氢氧化钠溶液时,为除去蒸馏水中溶解的
 ,常采用的方法是
,常采用的方法是(4)实验开始时应先将

 .
.(5)实验完毕后,取下装置B的橡胶塞,B瓶中可观察到的现象为
(6)实验中产生
 的作用有
的作用有A.排出装置内的空气
B.将A中溶液压入B中
C.保护
 不被空气氧化
不被空气氧化
您最近一年使用:0次
2023-12-06更新
|
227次组卷
|
2卷引用:辽宁省丹东市2023-2024学年高一上学期期中教学质量调研测试化学试题
名校
7 . 向一定量的Fe、FeO、Fe2O3的混合物中,加入100mL1.0mol·L-1的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,假设溶液体积不变,所得溶液中加入KSCN溶液无血红色出现。请回答下列问题:
(1)生成气体的物质的量为___________ ;
(2)所得溶液中溶质的物质的量浓度为___________ ;
(3)若向溶液中加入氢氧化钠溶液震荡,现象是___________ ;原因是(用方程式表示)___________ ;
(4)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为___________ ;
(5)原混合物的总质量为___________ 。
(1)生成气体的物质的量为
(2)所得溶液中溶质的物质的量浓度为
(3)若向溶液中加入氢氧化钠溶液震荡,现象是
(4)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为
(5)原混合物的总质量为
您最近一年使用:0次
2023-10-04更新
|
280次组卷
|
2卷引用:辽宁省沈阳市第十五中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
8 . 铁黄 是一种优质颜料。制备铁黄晶种时,向精制
是一种优质颜料。制备铁黄晶种时,向精制 溶液中滴加氨水(弱碱),先出现白色沉淀,后变为灰绿色。加氨水至
溶液中滴加氨水(弱碱),先出现白色沉淀,后变为灰绿色。加氨水至 时,开始通入空气,溶液
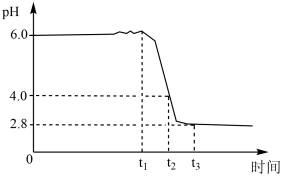
时,开始通入空气,溶液 随时间的变化曲线如图。下列分析不正确的是
随时间的变化曲线如图。下列分析不正确的是
 是一种优质颜料。制备铁黄晶种时,向精制
是一种优质颜料。制备铁黄晶种时,向精制 溶液中滴加氨水(弱碱),先出现白色沉淀,后变为灰绿色。加氨水至
溶液中滴加氨水(弱碱),先出现白色沉淀,后变为灰绿色。加氨水至 时,开始通入空气,溶液
时,开始通入空气,溶液 随时间的变化曲线如图。下列分析不正确的是
随时间的变化曲线如图。下列分析不正确的是
A.产生白色沉淀的离子方程式为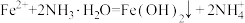 |
B. 发生的主要反应为 发生的主要反应为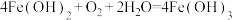 |
C. 发生的主要反应为 发生的主要反应为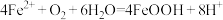 |
D. 后仅发生反应4Fe2++O2+4H+=4Fe3++2H2O 后仅发生反应4Fe2++O2+4H+=4Fe3++2H2O |
您最近一年使用:0次
2023-02-26更新
|
420次组卷
|
4卷引用:辽宁省大连市第十二中学2023-2024学年高一上学期12月学情反馈化学试题
名校
9 . 铁及其化合物在生产和生活中起到重要的作用。请回答下列问题:
(1)人体对 的吸收效果更好,但人体中时刻进行着
的吸收效果更好,但人体中时刻进行着 、
、 的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起
的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起_______ 剂。
(2)钢铁烤蓝是在钢铁表面形成一层一定厚度和强度的致密氧化膜,古代铁匠常用红热的铁浸入水中形成烤蓝,体现该反应原理的化学方程式为_______ 。
(3)实验室中储存 溶液时,为了防止其被空气中氧气氧化变质,会在溶液中加入一定量的
溶液时,为了防止其被空气中氧气氧化变质,会在溶液中加入一定量的_______ 。
(4)某小组同学欲用废铁屑(主要成分为Fe,还含有少量 )制备
)制备 。操作过程如下:
。操作过程如下:
i.用稀盐酸溶解废铁屑。
ii.在所得溶液中先加入过量氧化剂 ,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得
,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得 。
。
①步骤ii中加入过量氧化剂 的目的是
的目的是_______ 。离子方程式为_______ 。
②设计实验验证操作i所得溶液中不含 ,简述实验操作及现象:
,简述实验操作及现象:_______ 。
③该小组同学认为即使操作i所得溶液中不含 ,也不需要加入
,也不需要加入 ,若直接加入NaOH溶液可观察到的实验现象为
,若直接加入NaOH溶液可观察到的实验现象为_______ 。
(5)羟基氧化铁 是一种重要的化工原料,一种以工厂废料(含FeO、
是一种重要的化工原料,一种以工厂废料(含FeO、 、
、 、CuO)为原料生产
、CuO)为原料生产 的工艺流程如下:
的工艺流程如下:
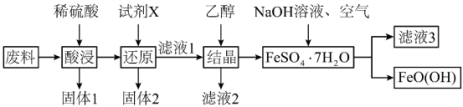
已知: 为酸性氧化物,不与硫酸等强酸反应;
为酸性氧化物,不与硫酸等强酸反应; 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。
①“固体1”的主要成分是_______ 。
②“酸浸”时CuO与硫酸发生反应的离子方程式为_______ 。“试剂X”宜选择的是_______ 。
A.双氧水 B.铜粉 C.铁粉 D.钠块
(1)人体对
 的吸收效果更好,但人体中时刻进行着
的吸收效果更好,但人体中时刻进行着 、
、 的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起
的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起(2)钢铁烤蓝是在钢铁表面形成一层一定厚度和强度的致密氧化膜,古代铁匠常用红热的铁浸入水中形成烤蓝,体现该反应原理的化学方程式为
(3)实验室中储存
 溶液时,为了防止其被空气中氧气氧化变质,会在溶液中加入一定量的
溶液时,为了防止其被空气中氧气氧化变质,会在溶液中加入一定量的(4)某小组同学欲用废铁屑(主要成分为Fe,还含有少量
 )制备
)制备 。操作过程如下:
。操作过程如下:i.用稀盐酸溶解废铁屑。
ii.在所得溶液中先加入过量氧化剂
 ,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得
,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得 。
。①步骤ii中加入过量氧化剂
 的目的是
的目的是②设计实验验证操作i所得溶液中不含
 ,简述实验操作及现象:
,简述实验操作及现象:③该小组同学认为即使操作i所得溶液中不含
 ,也不需要加入
,也不需要加入 ,若直接加入NaOH溶液可观察到的实验现象为
,若直接加入NaOH溶液可观察到的实验现象为(5)羟基氧化铁
 是一种重要的化工原料,一种以工厂废料(含FeO、
是一种重要的化工原料,一种以工厂废料(含FeO、 、
、 、CuO)为原料生产
、CuO)为原料生产 的工艺流程如下:
的工艺流程如下:
已知:
 为酸性氧化物,不与硫酸等强酸反应;
为酸性氧化物,不与硫酸等强酸反应; 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。①“固体1”的主要成分是
②“酸浸”时CuO与硫酸发生反应的离子方程式为
A.双氧水 B.铜粉 C.铁粉 D.钠块
您最近一年使用:0次
解题方法
10 . Ⅰ.碳酸亚铁在空气中灼烧得到铁的氧化物A和一种气体。某学习小组为了探究该氧化物A的组成设计如下实验方案:
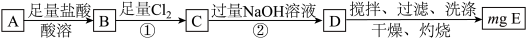
(1)若该方案中①通入 不足量,小组成员认为可以通过在空气中充分搅拌D而最终实现准确测定,他的依据是
不足量,小组成员认为可以通过在空气中充分搅拌D而最终实现准确测定,他的依据是_______ (用化学方程式表示)。
(2)若氧化物A的质量是7.84g,E的质量为8.00g,根据数据计算化合物A的化学式为_______ 。
Ⅱ.高铁酸钾( )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,已知
)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,已知 在
在 催化下会分解,在强碱性条件下稳定。高铁酸钾(
催化下会分解,在强碱性条件下稳定。高铁酸钾( )生产流程如下:
)生产流程如下:
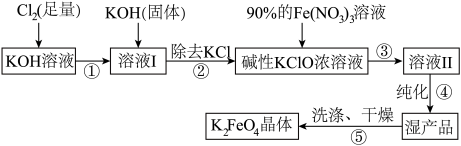
(3)在溶液Ⅰ中加入KOH固体的目的是_______。
(4)写出③反应的离子方程式_______ 。
(5)制备 时,将90%的
时,将90%的 溶液缓缓滴加到碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是
溶液缓缓滴加到碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是_______ 。
(6) 在酸性或弱碱性条件下能与水反应生成一种胶体和一种氧化性气体单质,该气体单质为
在酸性或弱碱性条件下能与水反应生成一种胶体和一种氧化性气体单质,该气体单质为_______ (写出化学式)。
(7) 净水时能吸附悬浮物的原因是
净水时能吸附悬浮物的原因是_______ 。
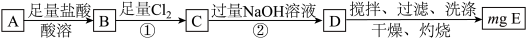
(1)若该方案中①通入
 不足量,小组成员认为可以通过在空气中充分搅拌D而最终实现准确测定,他的依据是
不足量,小组成员认为可以通过在空气中充分搅拌D而最终实现准确测定,他的依据是(2)若氧化物A的质量是7.84g,E的质量为8.00g,根据数据计算化合物A的化学式为
Ⅱ.高铁酸钾(
 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,已知
)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,已知 在
在 催化下会分解,在强碱性条件下稳定。高铁酸钾(
催化下会分解,在强碱性条件下稳定。高铁酸钾( )生产流程如下:
)生产流程如下:
(3)在溶液Ⅰ中加入KOH固体的目的是_______。
A.与溶液Ⅰ中过量的 继续反应,生成更多的KClO 继续反应,生成更多的KClO |
| B.KOH固体溶解时会放出较多的热量,有利于提高KClO产率 |
| C.为下一步反应提供碱性的环境 |
D.使 转化为KClO 转化为KClO |
(5)制备
 时,将90%的
时,将90%的 溶液缓缓滴加到碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是
溶液缓缓滴加到碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是(6)
 在酸性或弱碱性条件下能与水反应生成一种胶体和一种氧化性气体单质,该气体单质为
在酸性或弱碱性条件下能与水反应生成一种胶体和一种氧化性气体单质,该气体单质为(7)
 净水时能吸附悬浮物的原因是
净水时能吸附悬浮物的原因是
您最近一年使用:0次
2023-01-04更新
|
512次组卷
|
3卷引用:辽宁省重点高中2022-2023学年高一上学期期末联考化学试题



