1 . 胆矾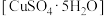 可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在
可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在 时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
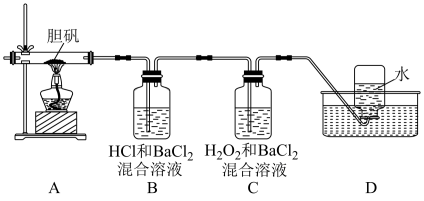
(1)B装置中 的作用是
的作用是___________ 。
(2)实验中,观察到B中有白色沉淀生成,C中无明显变化,可确定产物中一定有___________ 气体产生,写出B中发生反应的离子方程式___________ 。
(3)推测D中收集到的气体是___________ ,其检验方法为___________ 。
(4)A中固体完全分解后变为红色粉末,某同学设计实验验证固体残留物仅为 ,而不含
,而不含 ,请帮他完成表中内容。已知:
,请帮他完成表中内容。已知: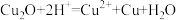 (试剂,仪器和用品自选)。
(试剂,仪器和用品自选)。
(5)结合上述实验现象,写出胆矾在 时隔绝空气加热完全分解的化学方程式
时隔绝空气加热完全分解的化学方程式____ 。
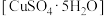 可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在
可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在 时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
(1)B装置中
 的作用是
的作用是(2)实验中,观察到B中有白色沉淀生成,C中无明显变化,可确定产物中一定有
(3)推测D中收集到的气体是
(4)A中固体完全分解后变为红色粉末,某同学设计实验验证固体残留物仅为
 ,而不含
,而不含 ,请帮他完成表中内容。已知:
,请帮他完成表中内容。已知: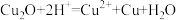 (试剂,仪器和用品自选)。
(试剂,仪器和用品自选)。| 实验步骤 | 实验预期 | 实验结论 |
准确称取 红色固体,加入足量 红色固体,加入足量 | 固体残留物仅为 |
 时隔绝空气加热完全分解的化学方程式
时隔绝空气加热完全分解的化学方程式
您最近一年使用:0次
2 . 由五种元素组成的化合物X,某学习小组按如图流程进行探究实验。
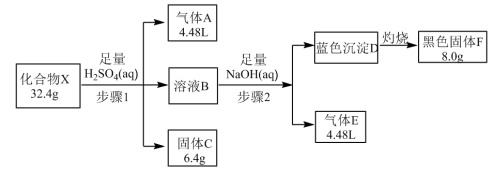
已知:化合物X难溶于水;气体体积均在标准状况下测定,气体A能使品红溶液褪色,气体E在标况下的密度为0.76g/L,固体C呈紫红色。
请回答:
(1)写出气体E的结构式___ ;溶液B中含有的溶质(除了H2SO4)有___ (用化学式表示)。
(2)化合物X含有的元素有Cu、H、___ (写出另外三种元素)。写出步骤1反应的化学方程式___ 。
(3)一定条件下,往溶液B中通入气体A和E,可制备化合物X,写出该反应的离子方程式___ 。
(4)气体E可将Fe2O3还原得到黑色固体(不含Fe3O4),请设计实验验证黑色固体的成分___ 。

已知:化合物X难溶于水;气体体积均在标准状况下测定,气体A能使品红溶液褪色,气体E在标况下的密度为0.76g/L,固体C呈紫红色。
请回答:
(1)写出气体E的结构式
(2)化合物X含有的元素有Cu、H、
(3)一定条件下,往溶液B中通入气体A和E,可制备化合物X,写出该反应的离子方程式
(4)气体E可将Fe2O3还原得到黑色固体(不含Fe3O4),请设计实验验证黑色固体的成分
您最近一年使用:0次
3 . 固体化合物由两种元素组成,某小组开展如下探究实验,其中气体A有刺激性气味,能使湿润的红色石蕊试纸变蓝。为探究X的组成,某研究小组进行如下实验:

(1)X的化学式是_______ ;刺激性气体分子电子式_______ ;
(2)X在纯氧中加强热的化学方程式_______ ;
(3)X与稀硫酸的离子反应方程式:_______ ;
(4)为探究固体丙是否是纯净物,请设计简单的实验方案:_______ 。

(1)X的化学式是
(2)X在纯氧中加强热的化学方程式
(3)X与稀硫酸的离子反应方程式:
(4)为探究固体丙是否是纯净物,请设计简单的实验方案:
您最近一年使用:0次
4 . CuCl2是常见的化学试剂,某学习小组利用废铜屑“湿法”制备CuCl2·2H2O。
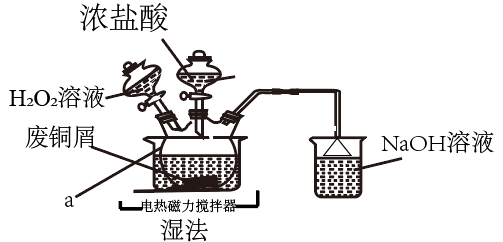
氯化铜在不同温度下结晶形成的结晶水合物
回答下列问题:
(1)仪器 的名称为
的名称为___________ , 溶液的作用是
溶液的作用是___________ 。
(2)“湿法”制备 的离子方程式为
的离子方程式为___________ ,实验中, 的实际用量要大于理论用量,原因是
的实际用量要大于理论用量,原因是___________ 。
(3)为得到纯净的 晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入
晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入 气体,加热蒸发浓缩,
气体,加热蒸发浓缩,___________ ,过滤,洗涤,低温干燥。其中,持续通入 的作用是
的作用是___________ 。
(4)用“间接碘量法”测定 废铜屑的利用率。取所得试样溶于水配成
废铜屑的利用率。取所得试样溶于水配成 ,取出
,取出 ,向其中加入过量
,向其中加入过量 固体,充分反应,生成白色
固体,充分反应,生成白色 沉淀,滴入几滴淀粉溶液作指示剂,用
沉淀,滴入几滴淀粉溶液作指示剂,用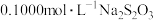 标准溶液滴定,到达滴定终点时,消耗
标准溶液滴定,到达滴定终点时,消耗 标准溶液
标准溶液 。(涉及到的反应为:
。(涉及到的反应为: ,
, )
)
①滴定终点的判断:当滴入最后一滴标准液,溶液恰好___________ (填颜色变化),且半分钟不再发生变化。
②废铜屑中铜的百分含量为___________ 。
(5)查阅资料: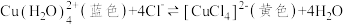 ,等量黄色与蓝色混合呈绿色。设计实验证明
,等量黄色与蓝色混合呈绿色。设计实验证明 溶液中存在上述平衡;取少量蓝色
溶液中存在上述平衡;取少量蓝色 稀溶液于试管中,
稀溶液于试管中,___________ 。

氯化铜在不同温度下结晶形成的结晶水合物
| 温度 | 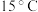 以下 以下 | 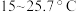 |  |  以上 以上 |
| 结晶水合物 | 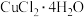 |  |  | 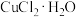 |
(1)仪器
 的名称为
的名称为 溶液的作用是
溶液的作用是(2)“湿法”制备
 的离子方程式为
的离子方程式为 的实际用量要大于理论用量,原因是
的实际用量要大于理论用量,原因是(3)为得到纯净的
 晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入
晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入 气体,加热蒸发浓缩,
气体,加热蒸发浓缩, 的作用是
的作用是(4)用“间接碘量法”测定
 废铜屑的利用率。取所得试样溶于水配成
废铜屑的利用率。取所得试样溶于水配成 ,取出
,取出 ,向其中加入过量
,向其中加入过量 固体,充分反应,生成白色
固体,充分反应,生成白色 沉淀,滴入几滴淀粉溶液作指示剂,用
沉淀,滴入几滴淀粉溶液作指示剂,用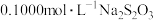 标准溶液滴定,到达滴定终点时,消耗
标准溶液滴定,到达滴定终点时,消耗 标准溶液
标准溶液 。(涉及到的反应为:
。(涉及到的反应为: ,
, )
)①滴定终点的判断:当滴入最后一滴标准液,溶液恰好
②废铜屑中铜的百分含量为
(5)查阅资料:
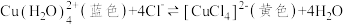 ,等量黄色与蓝色混合呈绿色。设计实验证明
,等量黄色与蓝色混合呈绿色。设计实验证明 溶液中存在上述平衡;取少量蓝色
溶液中存在上述平衡;取少量蓝色 稀溶液于试管中,
稀溶液于试管中,
您最近一年使用:0次
2021-10-23更新
|
1250次组卷
|
5卷引用:广东省广州市天河区2022届高三一模化学试题
广东省广州市天河区2022届高三一模化学试题(已下线)备战2022年高考化学精准检测卷【全国卷】15河北省衡水中学2022-2023学年高三上学期四调考试化学试题湖南省宁乡市第一高级中学2023届高三第七次月考化学试题湖南省邵阳市第一中学2023届高三第七次月考化学试题
5 . A、B、C、D、E五种物质间的转化关系如下:
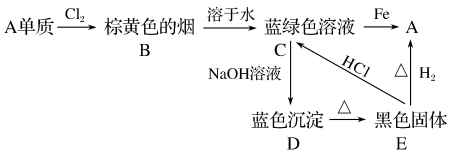
(1)写出A、E的化学式:A___________ 、E___________ 。
(2)写出下列各步反应的化学方程式:
C→A___________ ;
C→D___________ ;
E→A___________ ;
E→C___________ 。

(1)写出A、E的化学式:A
(2)写出下列各步反应的化学方程式:
C→A
C→D
E→A
E→C
您最近一年使用:0次
名校
解题方法
6 . 由四种常见元素组成的化合物X,按如下流程进行实验。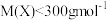 。
。
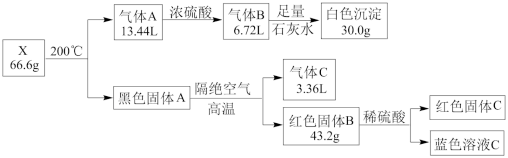
已知:固体A、B、C均为纯净物,且C为单质。气体C是单质,且能使带火星的木条复燃。气体体积已折算成标准状况。请回答:
(1)组成X的四种元素是___________ (填元素符号)。
(2)化合物X在空气中加热发生反应的化学方程式___________ 。
(3)黑色固体A与乙醇在加热条件下也可以得到红色固体C,该反应的化学方程式:___________ 。
(4)写出红色固体B与稀硫酸反应的离子方程式:___________ 。
(5)某兴趣小组用气体 还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:___________ 。
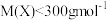 。
。
已知:固体A、B、C均为纯净物,且C为单质。气体C是单质,且能使带火星的木条复燃。气体体积已折算成标准状况。请回答:
(1)组成X的四种元素是
(2)化合物X在空气中加热发生反应的化学方程式
(3)黑色固体A与乙醇在加热条件下也可以得到红色固体C,该反应的化学方程式:
(4)写出红色固体B与稀硫酸反应的离子方程式:
(5)某兴趣小组用气体
 还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
您最近一年使用:0次
2021-07-07更新
|
281次组卷
|
3卷引用:单科化学-2021年秋季高三开学摸底考试卷03(课标全国专用)
(已下线)单科化学-2021年秋季高三开学摸底考试卷03(课标全国专用)浙江省”共美联盟“2020-2021学年高二下学期期末模拟化学试题江西省吉安市永丰县永丰中学2022-2023学年高一上学期期末考试化学(B班)试题
解题方法
7 . 最近我国有人报道,将0.1 mol· L-1的硫化钠溶液装进一只掏空洗净的鸡蛋壳里,将蛋壳开口朝上,部分浸入盛有0.1 mol· L-1的氯化铜溶液的烧杯中,在静置一周的过程中,蛋壳外表面逐渐出现金属铜,同时烧杯中的溶液渐渐褪色,并变得浑浊。
(1)设此装置中发生的是铜离子和硫离子直接相遇的反应,已知 (Cu2+/Cu)和
(Cu2+/Cu)和 (S/S2-)分别为0.345 V和-0.476V, nF
(S/S2-)分别为0.345 V和-0.476V, nF =RTlnK,
=RTlnK, 表示反应的标准电动势,n为该反应得失电子数。计算25°C下硫离子和铜离子反应得到铜的反应平衡常数
表示反应的标准电动势,n为该反应得失电子数。计算25°C下硫离子和铜离子反应得到铜的反应平衡常数____ ,写出平衡常数表达式______ 。
(2)金属铜和浑浊现象均出现在蛋壳外,这意味着____ 。
(3)该报道未提及硫离子与铜离子相遇时溶液的pH。现设pH=6,写出反应的离子方程式______ 。
(4)请对此实验结果作一简短评论____ 。
(1)设此装置中发生的是铜离子和硫离子直接相遇的反应,已知
 (Cu2+/Cu)和
(Cu2+/Cu)和 (S/S2-)分别为0.345 V和-0.476V, nF
(S/S2-)分别为0.345 V和-0.476V, nF =RTlnK,
=RTlnK, 表示反应的标准电动势,n为该反应得失电子数。计算25°C下硫离子和铜离子反应得到铜的反应平衡常数
表示反应的标准电动势,n为该反应得失电子数。计算25°C下硫离子和铜离子反应得到铜的反应平衡常数(2)金属铜和浑浊现象均出现在蛋壳外,这意味着
(3)该报道未提及硫离子与铜离子相遇时溶液的pH。现设pH=6,写出反应的离子方程式
(4)请对此实验结果作一简短评论
您最近一年使用:0次
8 . M为常见金属,不溶于盐酸和稀硫酸,质地坚韧,富延展性。将M溶于硝酸后蒸发、浓缩、冷却得到A的水合盐。A受热分解得到黑色固体B。B溶于盐酸,经蒸发、浓缩、冷却得到绿色晶体C。 B溶于稀硫酸后经蒸发、浓缩、冷却得到蓝色晶体D。D在270°C恒温下生成白色粉末E。E经600°C恒温后生成B。
(1)写出A、B、 C和E的化学式________ 、________ 、________ 、________ 。
(2)将E溶于水,加入过量的碘化钾溶液充分反应,其后缓慢滴加硫代硫酸钠溶液至过量。简述反应过程中发生的现象,写出相关反应的离子方程式________ 。
(3)A的熔点较低,真空时易升华,这与一般离子晶体的性质不相符。简述理由________ 。
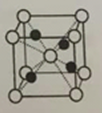
(4) M在一定温度下与氧作用得到固体G。G属立方品系,其正当晶胞如图所示,密度为6.00 g·cm-3。通过计算给出M-O的距离________ 。
(1)写出A、B、 C和E的化学式
(2)将E溶于水,加入过量的碘化钾溶液充分反应,其后缓慢滴加硫代硫酸钠溶液至过量。简述反应过程中发生的现象,写出相关反应的离子方程式
(3)A的熔点较低,真空时易升华,这与一般离子晶体的性质不相符。简述理由
(4) M在一定温度下与氧作用得到固体G。G属立方品系,其正当晶胞如图所示,密度为6.00 g·cm-3。通过计算给出M-O的距离

您最近一年使用:0次
9 . 胆矾( )易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的
)易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的 (杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
(杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
(1)制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的仪器有_______ (填标号)。
A.烧杯 B.容量瓶 C.蒸发皿 D.移液管
(2)将 加入到适量的稀硫酸中,加热,其主要反应的化学方程式为
加入到适量的稀硫酸中,加热,其主要反应的化学方程式为_______ ,与直接用废铜和浓硫酸反应相比,该方法的优点是_______ 。
(3)待 完全反应后停止加热,边搅拌边加入适量
完全反应后停止加热,边搅拌边加入适量 ,冷却后用
,冷却后用 调
调 为3.5~4,再煮沸
为3.5~4,再煮沸 ,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、
,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、_______ 、乙醇洗涤、_______ ,得到胆矾。其中,控制溶液 为3.5~4的目的是
为3.5~4的目的是_______ ,煮沸 的作用是
的作用是_______ 。
(4)结晶水测定:称量干燥坩埚的质量为 ,加入胆矾后总质量为
,加入胆矾后总质量为 ,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为
,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为 。根据实验数据,胆矾分子中结晶水的个数为
。根据实验数据,胆矾分子中结晶水的个数为_______ (写表达式)。
(5)下列操作中,会导致结晶水数目测定值偏高的是_______ (填标号)。
①胆矾未充分干燥 ②坩埚未置于干燥器中冷却 ③加热时有少量胆矾迸溅出来
 )易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的
)易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的 (杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
(杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:(1)制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的仪器有
A.烧杯 B.容量瓶 C.蒸发皿 D.移液管
(2)将
 加入到适量的稀硫酸中,加热,其主要反应的化学方程式为
加入到适量的稀硫酸中,加热,其主要反应的化学方程式为(3)待
 完全反应后停止加热,边搅拌边加入适量
完全反应后停止加热,边搅拌边加入适量 ,冷却后用
,冷却后用 调
调 为3.5~4,再煮沸
为3.5~4,再煮沸 ,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、
,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、 为3.5~4的目的是
为3.5~4的目的是 的作用是
的作用是(4)结晶水测定:称量干燥坩埚的质量为
 ,加入胆矾后总质量为
,加入胆矾后总质量为 ,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为
,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为 。根据实验数据,胆矾分子中结晶水的个数为
。根据实验数据,胆矾分子中结晶水的个数为(5)下列操作中,会导致结晶水数目测定值偏高的是
①胆矾未充分干燥 ②坩埚未置于干燥器中冷却 ③加热时有少量胆矾迸溅出来
您最近一年使用:0次
2021-06-11更新
|
18892次组卷
|
29卷引用:2021年高考全国甲卷化学真题
2021年高考全国甲卷化学真题河南省三门峡市实验高中2020-2021学年高二下学期6月月考化学试题(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)第8讲 金属材料(不锈钢、铝合金、合金)(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题13 化学实验-备战2022年高考化学学霸纠错(全国通用)(已下线)2021年高考全国甲卷化学试题变式题(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题10 化学实验综合—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押全国卷理综第26题 实验综合-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点10 实验方案的设计与评价-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题17化学实验综合题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)河北省保定市唐县第一中学2021-2022学年高二下学期期中考试化学试题(已下线)考点52 定量分析-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第08讲 金属材料(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第28讲 定性、定量实验(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题45 定量测量类综合实验-备战2023年高考化学一轮复习考点微专题(已下线)专题26 定量测定类综合性实验题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 大题突破2 综合实验题题型研究(已下线)专题03 化学实验专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)考点16 铜及其金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点12 金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点46 定量分析实验(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)河南省驻马店市“逐梦计划”大联考2023-2024学年高二上学期12月期末考试化学试题(已下线)专题一 化学式的确定(含热重分析) (练)(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)江西省重点校2022-2023学年高三上学期第二次联考化学试题.
10 . 从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:
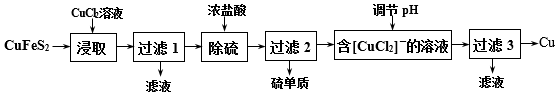
(1)“浸取”时,将黄铜矿进行粉碎的目的是___ 。
(2)“浸取”时,反应生成CuCl、FeCl2和S,该反应化学方程式为____ 。
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是____ 。
(4)“过滤3”所得滤液中可以循环使用的物质有___ 和____ ;为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为___ mol。
(5)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,化学方程式为:6CuFeS2+13O2 3Cu2S+2Fe3O4+9SO2、Cu2S+O2
3Cu2S+2Fe3O4+9SO2、Cu2S+O2 2Cu+SO2,此工艺与上述工艺相比,主要缺点有
2Cu+SO2,此工艺与上述工艺相比,主要缺点有_____ 。

(1)“浸取”时,将黄铜矿进行粉碎的目的是
(2)“浸取”时,反应生成CuCl、FeCl2和S,该反应化学方程式为
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是
(4)“过滤3”所得滤液中可以循环使用的物质有
(5)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,化学方程式为:6CuFeS2+13O2
 3Cu2S+2Fe3O4+9SO2、Cu2S+O2
3Cu2S+2Fe3O4+9SO2、Cu2S+O2 2Cu+SO2,此工艺与上述工艺相比,主要缺点有
2Cu+SO2,此工艺与上述工艺相比,主要缺点有
您最近一年使用:0次



