解题方法
1 . 部分含铜物质的分类与相应化合价关系如图所示。下列推断错误的是


A.d的代表物质高铜酸钾 具有强氧化性 具有强氧化性 | B.将c加入浓碱液中可制得e的胶体 |
C. 的转化可用于检验葡萄糖 的转化可用于检验葡萄糖 | D.存在 的转化关系 的转化关系 |
您最近一年使用:0次
2022-04-14更新
|
871次组卷
|
5卷引用:广东省佛山市普通高中2022届高三教学质量检测(二)化学试题
广东省佛山市普通高中2022届高三教学质量检测(二)化学试题广东省佛山市2022届高三下学期4月第二次教学质量监测(二模)化学试题(已下线)押广东卷化学第10题 元素及其化合物-备战2022年高考化学临考题号押题(广东卷)(已下线)专题06 物质的转化-备战2023年高考化学母题题源解密(广东卷)(已下线)第3讲 氧化还原反应
2 . 实验室利用废弃黄铜(主要成分为Zn和Cu)回收Cu并制备ZnO的部分实验过程如图所示:
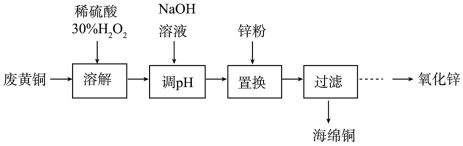
(1)为提高溶解速率,可以采取的措施有_______ (写2种)。
(2)“溶解”操作中一段时间后反应现象突然加剧,同时产生大量气体。
①反应过程中溶液的温度升高,其原因是_______ 。
②产生该现象的原因是(不考虑温度升高的影响)_______ 。
(3)相比用稀硝酸溶解废黄铜,该实验采用稀硫酸和H2O2溶解废黄铜的优点是_______ 。
(4)置换操作置换出铜单质,分离铜和锌。
①加入锌粉发生主要反应的离子方程式为_______ 。
②若没有“调pH”操作,对“置换”操作的影响是_______ 。

(1)为提高溶解速率,可以采取的措施有
(2)“溶解”操作中一段时间后反应现象突然加剧,同时产生大量气体。
①反应过程中溶液的温度升高,其原因是
②产生该现象的原因是(不考虑温度升高的影响)
(3)相比用稀硝酸溶解废黄铜,该实验采用稀硫酸和H2O2溶解废黄铜的优点是
(4)置换操作置换出铜单质,分离铜和锌。
①加入锌粉发生主要反应的离子方程式为
②若没有“调pH”操作,对“置换”操作的影响是
您最近一年使用:0次
名校
解题方法
3 . 下列物质的化学式与俗名不相对应的是
| A.FeSO4·7H2O皓矾 | B.CuSO4·5H2O胆矾 |
| C.Na2SO4·10H2O芒硝 | D.KAl(SO4)2·12H2O明矾 |
您最近一年使用:0次
名校
解题方法
4 . 碱式氯化铜[CuaClb(OH)c·xH2O]是一种重要的无机杀虫剂,它的制备流程如下,下列有关说法正确的是


| A.FeCl3的作用是增强盐酸的氧化性 |
| B.加入少量CuO目的是为了除去Fe3+ |
| C.石灰乳可用纯碱代替 |
| D.若制备1mol的CuCl2,理论上消耗11.2L空气 |
您最近一年使用:0次
2022-04-09更新
|
783次组卷
|
6卷引用:重庆市2022届高三模拟调研卷(三)化学试题
重庆市2022届高三模拟调研卷(三)化学试题(已下线)秘籍10 金属元素及化合物的相互转化与推断-备战2022年高考化学抢分秘籍(全国通用)湖南省株洲市第一中学2021-2022学年高三下学期期中考试化学试题(已下线)专题13 物质的反应和转化-2022年高考真题模拟题分项汇编(已下线)微专题15 铜及其化合物的性质、制备与实验探究-备战2023年高考化学一轮复习考点微专题(已下线)第10讲 金属材料及金属矿物的开发利用(讲)-2023年高考化学一轮复习讲练测(全国通用)
名校
解题方法
5 . 从价类二维的角度认识化学物质是一种高效的学习方法,铜元素的价类二维图如下,根据要求回答有关问题:
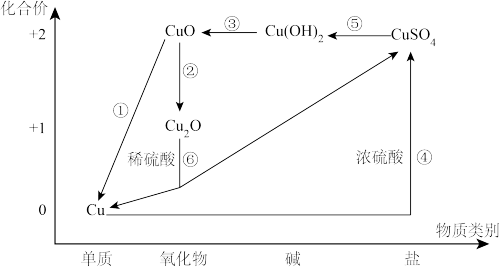
(1)Cu2(OH)2CO3是铜绿的主要成分,其属于_______ (填序号)。
a、碱b、正盐c、碱式盐d、酸式盐e、碳酸盐
(2)转化②中铜元素被_______ (填“氧化”或“还原”)。
(3)转化④的化学方程式为_______ 。
(4)转化⑤的反应类型为_______ (填基本反应类型),Cu(OH)2为_______ (填“强”、“弱”或“非”)电解质。
(5)已知Cu2O为砖红色不溶于水的固体,转化⑥可生成Cu、CuSO4溶液和另一种物质,则转化⑥的离子方程式为_______ 。
(6)Cu2O与稀HNO3可以发生氧化还原反应,完成并配平下列方程式:_______ 。
_______Cu2O+_______HNO3=_______Cu(NO3)2+_______NO↑+_______

(1)Cu2(OH)2CO3是铜绿的主要成分,其属于
a、碱b、正盐c、碱式盐d、酸式盐e、碳酸盐
(2)转化②中铜元素被
(3)转化④的化学方程式为
(4)转化⑤的反应类型为
(5)已知Cu2O为砖红色不溶于水的固体,转化⑥可生成Cu、CuSO4溶液和另一种物质,则转化⑥的离子方程式为
(6)Cu2O与稀HNO3可以发生氧化还原反应,完成并配平下列方程式:
_______Cu2O+_______HNO3=_______Cu(NO3)2+_______NO↑+_______
您最近一年使用:0次
2022-04-06更新
|
262次组卷
|
3卷引用:福建省龙岩第一中学2021-2022学年高一下学期第一次月考化学试题
解题方法
6 . 宋代绢画《千里江山图》以“赭石为基底,孔雀石做重彩,蓝铜矿染青山,砗磲白填人形”。下列说法正确的是
| A.绢的主要成分是蚕丝,属于纤维素 |
| B.红棕色赭石的主要成分是Fe3O4 |
| C.孔雀石[主要成分为Cu2CO3(OH)2]耐高温,受热不分解 |
| D.蓝铜矿[主要成分为Cu3(CO3)2(OH)2]遇强酸会产生气体 |
您最近一年使用:0次
名校
解题方法
7 . 下列离子方程式正确的是
A.向含有1mol  的溶液中加入2mol 的溶液中加入2mol  : : |
B.向 溶液中加入适量 溶液中加入适量 : :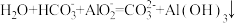 |
C. 溶液与稀硫酸的反应: 溶液与稀硫酸的反应: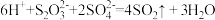 |
D.向硫酸铜溶液中加入过量的氨水: |
您最近一年使用:0次
2022-03-29更新
|
691次组卷
|
3卷引用:辽宁省沈阳市第二中学2021-2022学年高三下学期第二次模拟考试化学试题
名校
解题方法
8 . 用粗铜精炼工业中产生的铜阳极泥(主要含Cu2Se、Ag2Se、金和铂等)为原料,回收并制备硝酸铜和硒的工艺流程如图:
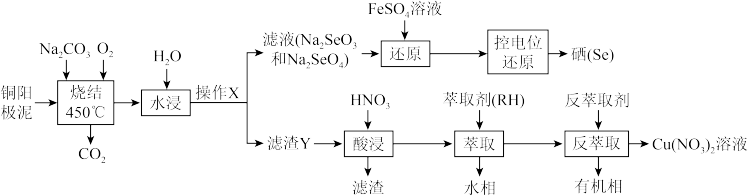
(1)“烧结”时发生如下反应,请完善该反应方程式:___________ 。
 ___
___ _____
_____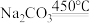 ___
___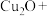 ______
______ _____
_____
工业上,采用通入高压氧气使铜阳极泥处于“沸腾”状态,其目的是___________ 。
(2)在实验室,操作X的名称为___________ 。
(3)滤渣Y的成分有Ag2O、_____ (填化学式,下同);已知萃取与反萃取原理为:2RH+Cu2+→R2Cu+2H+,则“反萃取”时反萃取剂最好选用_____ 溶液。
(4)FeSO4的作用是“还原”Na2SeO4制备Na2SeO3,每摩尔Na2SeO4消耗FeSO4的物质的量为___________ mol;常温下,H2SeO3的Ka1=1.0x10-3,Ka2=1.0x10-7;当常温下溶液的pH=4.4时,Na2SeO3溶液中最主要的含Se粒子是___________ 。
(5)“控电位还原”是指在一定电压下,电位高的氧化剂优先被还原,电位低的氧化剂保留在溶液中,以达到硒与杂质金属的分离;下表为一些氧化剂的电位(A/B:A代表氧化剂,B代表还原产物)。
则SeO 、Fe3+和Cu2+的氧化性由强到弱的顺序为
、Fe3+和Cu2+的氧化性由强到弱的顺序为___________ ,在0.740V时Fe3+优先被还原,其还原反应(半反应)式为___________ 。

(1)“烧结”时发生如下反应,请完善该反应方程式:
 ___
___ _____
_____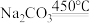 ___
___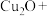 ______
______ _____
_____
工业上,采用通入高压氧气使铜阳极泥处于“沸腾”状态,其目的是
(2)在实验室,操作X的名称为
(3)滤渣Y的成分有Ag2O、
(4)FeSO4的作用是“还原”Na2SeO4制备Na2SeO3,每摩尔Na2SeO4消耗FeSO4的物质的量为
(5)“控电位还原”是指在一定电压下,电位高的氧化剂优先被还原,电位低的氧化剂保留在溶液中,以达到硒与杂质金属的分离;下表为一些氧化剂的电位(A/B:A代表氧化剂,B代表还原产物)。
| 名称 | 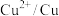 | 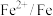 |  |  |
| 电位/V | 0.345 | 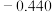 | 0.770 | 0.740 |
 、Fe3+和Cu2+的氧化性由强到弱的顺序为
、Fe3+和Cu2+的氧化性由强到弱的顺序为
您最近一年使用:0次
2022-03-25更新
|
927次组卷
|
4卷引用:四川省遂宁市2022届高三第二次诊断性考试(二模)理综化学试题
四川省遂宁市2022届高三第二次诊断性考试(二模)理综化学试题四川省内江市2022届高三下学期第二次模拟考试理科综合化学试题(已下线)微专题15 铜及其化合物的性质、制备与实验探究-备战2023年高考化学一轮复习考点微专题四川省泸县第一中学2023-2024学年高三上学期期末考试理综试题-高中化学
名校
9 . 下列化合物的俗称与化学式不对应的是
| A.水玻璃:Na2SiO3水溶液 | B.绿矾:FeSO4·7H2O |
| C.明矾:Al2(SO4)3·12H2O | D.胆矾:CuSO4·5H2O |
您最近一年使用:0次
2022-03-22更新
|
282次组卷
|
4卷引用:宁夏银川一中2021-2022学年高一上学期期末考试化学试题
10 . 将过量的Na2CO3溶液滴入到一定量CuSO4溶液中得到蓝色固体。某研究性学习小组对蓝色固体的成分进行了如下探究。
(一)猜想与假设:
猜想一:固体为CuCO3,理由:___________ (用化学反应方程式表示)。
猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈___________ (填“酸”或“碱”)性。
猜想三:固体为Cu(OH)2和CuCO3的混合物。
(二)资料查阅:
①Cu(OH)2和CuCO3晶体均不带结晶水;
②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物。
(三)设计与实验:
I.固体的获取:
(1)将反应后的固、液混合物经_______ 、洗涤、低温烘干得蓝色固体。
(2)判断固体已洗净的方法及现象______
II.用下图所示装置,定性探究固体的成分。

(3)若用装置A、B组合进行实验,B中无现象,则猜想________ 正确;
(4)若用装置A、C组合进行实验,C中无现象,则猜想_______ 正确;
(5)小组同学将装置按A、_______ 、______ (填“B”、“C”)的顺序组合进行实验,验证出猜想三是正确的,实验中:B中的现象为_______ ,C中的现象为_______ 。
结论:固体为Cu(OH)2和CuCO3的混合物。
III.固体成分定量测定:
已知Cu(OH)2的分解温度为66℃∽68℃,CuCO3的分解温度为200℃∽220℃。设固体的组成为aCu(OH)2•bCuCO3.小组同学用热分析仪对固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如图,

请根据图示回答下列问题:
(6)写出AB、CD段发生反应的化学方程式:
AB段:________ ;
CD段:_______ ;
(7)通过计算可得:a∶b=_______ 。
(8)若将24.0g剩余固体继续加热到更高的温度,发现固体质量减少了2.4g后质量不再改变,写出此过程中可能发生反应的化学方程式:_______ 。
(一)猜想与假设:
猜想一:固体为CuCO3,理由:
猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈
猜想三:固体为Cu(OH)2和CuCO3的混合物。
(二)资料查阅:
①Cu(OH)2和CuCO3晶体均不带结晶水;
②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物。
(三)设计与实验:
I.固体的获取:
(1)将反应后的固、液混合物经
(2)判断固体已洗净的方法及现象
II.用下图所示装置,定性探究固体的成分。

(3)若用装置A、B组合进行实验,B中无现象,则猜想
(4)若用装置A、C组合进行实验,C中无现象,则猜想
(5)小组同学将装置按A、
结论:固体为Cu(OH)2和CuCO3的混合物。
III.固体成分定量测定:
已知Cu(OH)2的分解温度为66℃∽68℃,CuCO3的分解温度为200℃∽220℃。设固体的组成为aCu(OH)2•bCuCO3.小组同学用热分析仪对固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如图,

请根据图示回答下列问题:
(6)写出AB、CD段发生反应的化学方程式:
AB段:
CD段:
(7)通过计算可得:a∶b=
(8)若将24.0g剩余固体继续加热到更高的温度,发现固体质量减少了2.4g后质量不再改变,写出此过程中可能发生反应的化学方程式:
您最近一年使用:0次



