名校
解题方法
1 . 将1mol固体A置于体积不变的真空密闭容器中(固体试样体积忽略不计),在恒定温度下使其分解:A(s) 2B(g)+C(g),下列可以判断该反应已达到化学平衡状态的是
2B(g)+C(g),下列可以判断该反应已达到化学平衡状态的是
 2B(g)+C(g),下列可以判断该反应已达到化学平衡状态的是
2B(g)+C(g),下列可以判断该反应已达到化学平衡状态的是| A.物质的浓度:c(B)=2c(C) | B.混合气体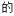 密度保持不变 密度保持不变 |
| C.B的体积分数不变 | D.混合气体的平均摩尔质量保持不变 |
您最近一年使用:0次
2024-04-29更新
|
374次组卷
|
2卷引用:福建省福州九县(区、市)一中(高中)2023-2024学年高一下学期4月期中联考化学试题
2024高三下·全国·专题练习
解题方法
2 . 某工厂采用辉铋矿(主要成分为 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制各
)联合焙烧法制各 和
和 ,工艺流程如下:
,工艺流程如下: 分解为
分解为 ,
, 转变为
转变为 ;
;
②金属活动性: ;
;
③相关金属离子形成氢氧化物的 范围如下:
范围如下:
为提高焙烧效率,可采取的措施为_______ 。
a.进一步粉碎矿石 b.鼓入适当过量的空气 c.降低焙烧温度
 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制各
)联合焙烧法制各 和
和 ,工艺流程如下:
,工艺流程如下:
 分解为
分解为 ,
, 转变为
转变为 ;
;②金属活动性:
 ;
;③相关金属离子形成氢氧化物的
 范围如下:
范围如下:开始沉淀 | 完全沉淀 | |
 | 6.5 | 8.3 |
 | 1.6 | 2.8 |
 | 8.1 | 10.1 |
a.进一步粉碎矿石 b.鼓入适当过量的空气 c.降低焙烧温度
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
3 . 工业以软锰矿(主要成分是 ,含有
,含有 、
、 等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(
等少量杂质)为主要原料制备高性能的磁性材料碳酸锰( )。其工业流程如下:
)。其工业流程如下: 生成,温度对“浸锰”反应的影响如图所示:
生成,温度对“浸锰”反应的影响如图所示: 的生成,“浸锰”的适宜温度是
的生成,“浸锰”的适宜温度是___________ 。
 ,含有
,含有 、
、 等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(
等少量杂质)为主要原料制备高性能的磁性材料碳酸锰( )。其工业流程如下:
)。其工业流程如下: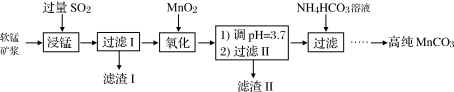
 生成,温度对“浸锰”反应的影响如图所示:
生成,温度对“浸锰”反应的影响如图所示: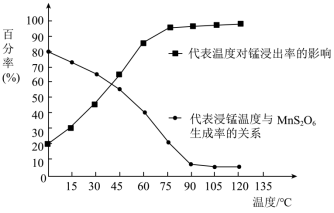
 的生成,“浸锰”的适宜温度是
的生成,“浸锰”的适宜温度是
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
4 . CO2-CH4干气重整反应制合成气(H2、CO)是CO2资源化利用的重要研究方向。其反应主要包括:
反应I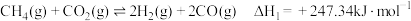
反应II
(1)已知 H2(g)、CO(g)的燃烧热分别为285.8 kJ∙mol-1和283kJ∙mol-1,水的汽化热为44kJ∙mol-1,则 =
=___________ kJ∙mol-1;能同时提高CH4(g)的平衡转化率和反应速率的措施为___________ (写一条即可)。
反应I
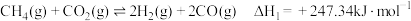
反应II

(1)已知 H2(g)、CO(g)的燃烧热分别为285.8 kJ∙mol-1和283kJ∙mol-1,水的汽化热为44kJ∙mol-1,则
 =
=
您最近一年使用:0次
5 . 下列实验事实不能 用平衡移动原理解释的是
A.将NO2球浸泡在冷水和热水中 |
B.排饱和食盐水收集Cl2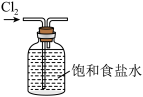 |
C.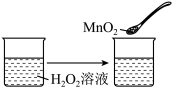 |
D.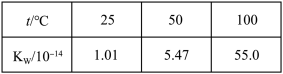 |
您最近一年使用:0次
解题方法
6 . 可逆反应,在一定条件下达到化学平衡,说明
A. (正)= (正)= (逆)=0 (逆)=0 | B.正逆反应停止 |
C. (正)= (正)= (逆)≠0 (逆)≠0 | D. (正)> (正)> (逆) (逆) |
您最近一年使用:0次
2024-03-08更新
|
465次组卷
|
2卷引用:6.2.2 化学反应的限度 随堂练习
7 . 在可逆反应中,以下叙述正确的是
| A.正反应先发生 |
| B.逆反应先发生 |
| C.正反应和逆反应同时发生 |
| D.正反应和逆反应谁先发生,由反应条件决定 |
您最近一年使用:0次
2024-03-08更新
|
227次组卷
|
2卷引用:6.2.2 化学反应的限度 随堂练习
22-23高一下·新疆巴音郭楞·期末
8 . 化学反应速率是
| A.即时速率 | B.平均速率 | C.匀速速率 | D.平均速度 |
您最近一年使用:0次
2024-03-08更新
|
333次组卷
|
3卷引用:6.2.1化学反应的速率课后作业巩固篇
解题方法
9 . 证据推理是化学学科重要的核心素养。下列证据与推理均正确的是
| 选项 | 证据 | 推理 |
| A | 将 晶体溶于稀硫酸中,滴入几滴KSCN溶液,溶液呈红色 晶体溶于稀硫酸中,滴入几滴KSCN溶液,溶液呈红色 |  晶体已变质 晶体已变质 |
| B | 等pH、等体积的HB和HA分别与NaOH溶液反应,HB消耗的NaOH溶液体积多 | HA是强酸 |
| C | 室温下,用pH试纸测0.1 的 的 溶液的pH约为5 溶液的pH约为5 |  的电离大于其水解 的电离大于其水解 |
| D | 向2mL 30%的 溶液中滴加浓硫酸,产生气体的速率加快 溶液中滴加浓硫酸,产生气体的速率加快 |  对 对 的分解具有催化作用 的分解具有催化作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024高三下·全国·专题练习
10 . 甲醇是重要的化工原料,又可作燃料。利用CO生产甲醇的反应为2H2(g)+CO(g) CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
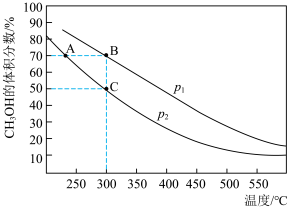
(1)该反应的ΔH______ 0(填“>”或“<”);B点与C点的平衡常数关系为KB______ KC(填“>”“<”或“=”)。向平衡体系中加入高效催化剂, 将
将______ (填“增大”“减小”或“不变”);再次增大体系压强,k正-k逆的值将______ (填“增大”“减小”或“不变”)。
(2)C点对应的平衡常数Kp=______ (Kp为以分压表示的平衡常数,气体分压=气体总压×体积分数)。
(3)一定温度下,将H2和CO按物质的量之比为1∶1、1∶2和2∶1进行初始投料。则达到平衡后,初始投料比为______ 时,H2转化率最大。
 CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
(1)该反应的ΔH
 将
将(2)C点对应的平衡常数Kp=
(3)一定温度下,将H2和CO按物质的量之比为1∶1、1∶2和2∶1进行初始投料。则达到平衡后,初始投料比为
您最近一年使用:0次



