解题方法
1 . 回答下列问题:
(1)2023年9月23日20时许,第19届亚运会在杭州奥体中心“大莲花”盛大开幕。此次杭州亚运会主火炬的燃料首次使用废碳再生的绿色甲醇,实现了循环内的零排放。我国科学家在含铂高效催化剂作用下把二氧化碳高效转化为清洁液态燃料——甲醇。
(1)该法利用 制取甲醇的有关化学反应如下:
制取甲醇的有关化学反应如下:
①

②
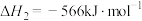
③
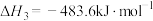
已知反应①中相关的化学键键能数据如下:
由此计算断开1molC=O键需要吸收_______ kJ的能量(甲醇的结构式为 );
);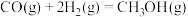

_______  。
。
(2)甲醇燃烧时发生如下反应(a、b、c、d均大于0):
①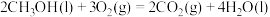
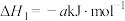
②

③
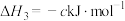
④

由此知,a、b、c、d由小到大的排序为_______ 。
(3)甲烷、氢气、乙烯、乙炔也是常用的燃料物质。已知:①101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量叫做该物质的标准燃烧热。常温常压下,几种可燃物的燃烧热如下表所示:
①甲烷不完全燃烧的能量变化如图所示。CO燃烧的热化学方程式是_______ 。

②在相同条件下,等质量的下列气体完全燃烧生成二氧化碳气体和液态水时,放出的热量最多的是_______ (填字母)。
A. B.
B. C.
C. D.
D.
③家用灶具有进气口和进风口。使用煤气(主要成分是氢气和CO的混合物,其中CO的体积分数是0.8)灶具改为使用天然气燃料。要调整好空气进气孔,调整的方法是_______ 。
④ 将是未来最好的绿色燃料,使用氢气作燃料的优点是
将是未来最好的绿色燃料,使用氢气作燃料的优点是_______ (回答两点即可)。
(1)2023年9月23日20时许,第19届亚运会在杭州奥体中心“大莲花”盛大开幕。此次杭州亚运会主火炬的燃料首次使用废碳再生的绿色甲醇,实现了循环内的零排放。我国科学家在含铂高效催化剂作用下把二氧化碳高效转化为清洁液态燃料——甲醇。
(1)该法利用
 制取甲醇的有关化学反应如下:
制取甲醇的有关化学反应如下:①


②

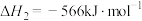
③

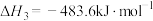
已知反应①中相关的化学键键能数据如下:
| 化学键 | C-C | C-H | H-H | C-O | H-O |
键能 | 348 | 413 | 436 | 358 | 463 |
 );
);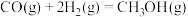

 。
。(2)甲醇燃烧时发生如下反应(a、b、c、d均大于0):
①
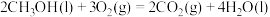
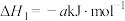
②


③

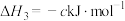
④


由此知,a、b、c、d由小到大的排序为
(3)甲烷、氢气、乙烯、乙炔也是常用的燃料物质。已知:①101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量叫做该物质的标准燃烧热。常温常压下,几种可燃物的燃烧热如下表所示:
| 可燃物 |  |  |  | 甲烷 |
燃烧热( )/ )/ | -285.8 | -1411.0 | -1299.6 | -890.3 |
①甲烷不完全燃烧的能量变化如图所示。CO燃烧的热化学方程式是

②在相同条件下,等质量的下列气体完全燃烧生成二氧化碳气体和液态水时,放出的热量最多的是
A.
 B.
B. C.
C. D.
D.
③家用灶具有进气口和进风口。使用煤气(主要成分是氢气和CO的混合物,其中CO的体积分数是0.8)灶具改为使用天然气燃料。要调整好空气进气孔,调整的方法是
④
 将是未来最好的绿色燃料,使用氢气作燃料的优点是
将是未来最好的绿色燃料,使用氢气作燃料的优点是
您最近一年使用:0次
2023-10-20更新
|
261次组卷
|
2卷引用:广西河池市八校2023-2024学年高二上学期10月联考化学试题
2 . 下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多 |
| B.电解氯化镁溶液阴极生成镁 |
C.已知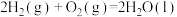 ; ;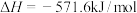 , , 的燃烧热为285.8kJ 的燃烧热为285.8kJ |
D.在稀溶液中,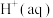  ; ;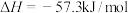 ,若将含0.5mol ,若将含0.5mol 的浓硫酸与含1mol NaOH的溶液混合,放出的热大于57.3kJ 的浓硫酸与含1mol NaOH的溶液混合,放出的热大于57.3kJ |
您最近一年使用:0次
解题方法
3 . 下列有关反应热的说法不正确的是
A.在稀溶液中: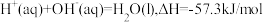 ,若将含0.5 mol H2SO4的稀硫酸与含 ,若将含0.5 mol H2SO4的稀硫酸与含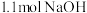 的稀溶液混合,放出的热量等于57.3 kJ 的稀溶液混合,放出的热量等于57.3 kJ |
B.甲烷的燃烧热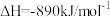 ,则甲烷燃烧的热化学方程式为: ,则甲烷燃烧的热化学方程式为: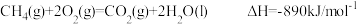 |
C. 键、 键、 键和 键和 键的键能分别为 键的键能分别为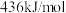 , ,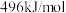 和 和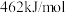 ,则反应 ,则反应 的 的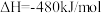 |
D. ,石墨比金刚石稳定 ,石墨比金刚石稳定 |
您最近一年使用:0次
4 . AlH3是一种储氢材料,可作为固体火箭推进剂。通过激光加热引发AlH3的燃烧反应,燃烧时温度和时间的变化关系如图所示。

燃烧不同阶段发生的主要变化为:
①2AlH3(s)=2Al(s)+3H2(g) ∆H1
②H2(g)+1/2O2(g)=H2O(g) ∆H2
③Al(s)=Al(g) ∆H3
④Al(g)+3/4O2(g)=1/2Al2O3(s) ∆H4
下列说法不正确的是

燃烧不同阶段发生的主要变化为:
①2AlH3(s)=2Al(s)+3H2(g) ∆H1
②H2(g)+1/2O2(g)=H2O(g) ∆H2
③Al(s)=Al(g) ∆H3
④Al(g)+3/4O2(g)=1/2Al2O3(s) ∆H4
下列说法不正确的是
| A.2AlH3(s)+3O2(g)=Al2O3(s)+3H2O(g) ∆H=∆H1+3∆H2+2∆H3+2∆H4 |
| B.其他条件相同时,等物质的量的Al(g)燃烧放出的热量大于Al(s)燃烧放出的热量 |
| C.氢气的燃烧热为∆H2 |
| D.b-c阶段温度不变的可能原因是反应②放出的热量被铝气化时吸收 |
您最近一年使用:0次
2021-09-14更新
|
273次组卷
|
3卷引用:广西河池市八校2021-2022学年高二上学期第一次联考化学试题
名校
5 . 2008年北京奥会“祥云“奥运火炬所用环保型燃料为丙烷,悉尼奥运会所用火炬燃料为65%丁烷和35%丙烷,已知丙烷的燃烧热为2221.5kJ/mol;正丁烷的燃烧热为2878kJ/mol;异丁烷的燃烧热为2869.6kJ/mol;下列有关说法正确的是
| A.丙烷燃烧的热化学方程式为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(g) △H=-2221.5kJ/mol |
| B.相同质量的正丁烷和异丁烷分别完全燃烧,前者需要的氧气多,产生的热量也多 |
| C.正丁烷比异丁烷稳定 |
| D.奥运火炬燃烧时主要是将化学能转变为热能和光能 |
您最近一年使用:0次
2017-12-12更新
|
164次组卷
|
2卷引用:广西河池市高级中学2017-2018学年高二上学期第二次月考化学试题
名校
6 . 下列推论正确的是
| A.S(g)+O2(g)=SO2(g) △H1;S(s)+O2(g)=SO2(g) △H2,则:△H1>△H2 |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)D △H1,NaOH(s)+HCl(aq)=NaCl(aq)+H2O(l)△H2则:△H1<△H2 |
| C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.3kJ/mol,则: 含20gNaOH的稀溶液与稀盐酸完全反应,放的热量为28.65kJ |
| D.2C(s)+O2(g)=2CO(g) △H=-221kJ/mol,则碳的燃烧热等于110.5kJ/mol |
您最近一年使用:0次
7 . 下列说法正确的是
| A.在25℃、101KPa,1molS(s)和2molS(s)的燃烧热相等 |
| B.1molH2SO4(浓)与1molBa(OH)2完全中和所放出的热量为中和热 |
| C.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,所以CO的燃烧反应一定是吸热反应 |
| D.101KPa时,1molH2燃烧所放出的热量为氢气的燃烧热 |
您最近一年使用:0次
2017-11-27更新
|
534次组卷
|
8卷引用:广西河池市高级中学2017-2018学年高二上学期期末考试化学试题
8 . 已知:
2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) ΔH=-266 kJ·mol-1
O2(g) ΔH=-266 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是
2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)=Na2CO3(s)+
 O2(g) ΔH=-266 kJ·mol-1
O2(g) ΔH=-266 kJ·mol-1根据以上热化学方程式判断,下列说法正确的是
| A.CO的燃烧热为283 kJ |
B.下图可表示由CO生成CO2的反应过程和能量关系 |
| C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-532 kJ·mol-1 |
| D.CO(g)与Na2O2(s)反应放出549 kJ热量时,电子转移数为6.02×1023 |
您最近一年使用:0次
2016-10-31更新
|
558次组卷
|
31卷引用:广西河池市高级中学2017-2018学年高二上学期第二次月考化学试题
广西河池市高级中学2017-2018学年高二上学期第二次月考化学试题(已下线)2013-2014黑龙江省哈六中学高一下学期期中考试化学试卷(已下线)2014-2015学年甘肃天水市第一中学高二上第一阶段考试题化学试卷2015-2016学年安徽省安庆一中高二上学期期末化学试卷2016-2017学年云南省曲靖市沾益一中高二上第一次月考化学卷2017届河北省石家庄辛集中学高三上期中化学试卷2016-2017学年山西省大同一中高二上期中化学试卷2016-2017学年江西省南昌市第二中学高二上学期期末考试化学试卷河北省衡水中学2016-2017学年高一下学期期中考试化学试题黑龙江省鹤岗第一中学2016-2017学年高一下学期期中考试化学试卷宁夏石嘴山市第三中学2016-2017学年高二下学期期中考试化学试题四川省简阳市2016-2017学年高一下学期期末考试化学试题湖南省益阳市箴言中学2016-2017学年高一下学期期末化学试题山西省朔州市第一中学2017-2018学年高二8月月考化学试题河南省南阳市第一中学2017-2018学年高二上学期第一次月考化学试题山西省大同市第一中学2017-2018学年高二上学期期中考试化学试题河南省安阳市第三十六中学2017-2018学年高二上学期期中考试化学试题内蒙古巴彦淖尔市第一中学2017-2018学年高二上学期期中考试(A卷)化学试题河北省承德市第二中学2017-2018学年高二上学期第一次月考化学试题湖南省醴陵市第一中学2018-2019学年高二上学期入学考试化学试题山西省朔州市平鲁区李林中学2018-2019学年高二上学期第一次月考化学试题(已下线)2018年10月21日 《每日一题》人教选修4-每周一测四川省成都外国语学校2018-2019学年高二上学期半期考试化学试题新疆维吾尔自治区伊宁市生产建设兵团四师一中2018-2019学年高二上学期期中考试化学试题【全国百强校】内蒙古巴彦淖尔一中2018-2019学年高二上学期期中考试化学试题【全国百强校】贵州省铜仁市第一中学2018-2019学年高二下学期开学考试化学试题江西省南昌市八一中学、洪都中学、十七中三校2019-2020学年高二10月联考化学试题河北承德第一中学2020-2021学年高一下学期第三次月考化学试题湖北省石首市第一中学2021-2022学年高二上学期10月月考化学试题云南省宣威市第三中学2021-2022学年高二上学期期末考试化学试题宁夏石嘴山市第三中学2022-2023学年高二下学期第一次月考化学(理)试题



